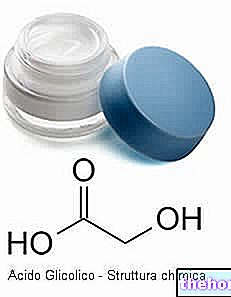
Actieve ingrediënten: Zonisamide
Zonegran 25 mg, 50 mg en 100 mg harde capsules
Waarom wordt Zonegran gebruikt? Waar is het voor?
Zonegran bevat de werkzame stof zonisamide en wordt gebruikt als anti-epilepticum.
Zonegran wordt gebruikt voor de behandeling van aanvallen die een deel van de hersenen aantasten (partiële aanvallen), al dan niet gevolgd door een aanval die de hele hersenen aantast (secundaire generalisatie).
Zonegran kan worden gebruikt:
- alleen voor de behandeling van aanvallen bij volwassenen
- met andere anti-epileptica voor de behandeling van aanvallen bij volwassenen, adolescenten en kinderen vanaf 6 jaar.
Contra-indicaties Wanneer Zonegran niet mag worden gebruikt
Gebruik Zonegran niet
- als u allergisch bent voor zonisamide of voor één van de andere bestanddelen van dit geneesmiddel (vermeld in rubriek 6),
- als u allergisch bent voor andere sulfonamidegeneesmiddelen, bijvoorbeeld: sulfonamide-antibiotica, thiazidediuretica en op sulfonylureumderivaten gebaseerde diabetesgeneesmiddelen.
Voorzorgen bij gebruik Wat u moet weten voordat u Zonegran inneemt
Zonegran behoort tot een groep geneesmiddelen (sulfonamiden) die ernstige allergische reacties, ernstige huiduitslag en bloedstoornissen kunnen veroorzaken, die in zeer zeldzame gevallen tot de dood kunnen leiden (zie rubriek 4. Mogelijke bijwerkingen).
Ernstige huiduitslag komt voor in combinatie met Zonegran-therapie, waaronder gevallen van Stevens-Johnson-syndroom.
Neem contact op met uw arts of apotheker voordat u Zonegran inneemt als:
- jonger bent dan 12 jaar omdat u mogelijk een verhoogd risico loopt op minder zweten, zonnesteek, longontsteking en leverproblemen. Als u jonger bent dan 6 jaar, wordt Zonegran niet aanbevolen voor u.
- u bejaard bent, omdat uw dosis Zonegran mogelijk moet worden aangepast en omdat u meer kans heeft op het ontwikkelen van een allergische reactie, ernstige huiduitslag, zwelling van de voeten en benen en jeuk wanneer u Zonegran gebruikt (zie rubriek 4 Mogelijke bijwerkingen).
- als u leverproblemen heeft, omdat uw dosis Zonegran mogelijk moet worden aangepast.
- oogproblemen heeft, zoals glaucoom.
- nierproblemen heeft, omdat uw dosis Zonegran mogelijk moet worden aangepast.
- in het verleden aan nierstenen heeft geleden, omdat er een verhoogd risico bestaat dat ze zich opnieuw ontwikkelen. Drink voldoende water om het risico op nierstenen te verkleinen.
- woont of op vakantie is op een plek waar het warm weer is. Zonegran kan een afname van zweten veroorzaken, wat kan leiden tot een stijging van de lichaamstemperatuur. Om het risico op een overmatige stijging van de lichaamstemperatuur te verminderen, moet u voldoende water drinken en proberen koel te blijven.
- ondergewicht hebt of veel bent afgevallen, aangezien Zonegran ervoor kan zorgen dat u verder afvalt. Vertel het uw arts, aangezien dit mogelijk moet worden nageleefd. Als een van deze waarschuwingen op u van toepassing is, vertel dit dan aan uw arts voordat u Zonegran inneemt.
Kinderen en adolescenten
Praat met uw arts over de volgende risico's:
Preventie van hitte en uitdroging bij kinderen
Zonegran kan het zweetniveau van uw kind verminderen en leiden tot hitte en als uw kind niet op de juiste manier wordt behandeld, kan het hersenbeschadiging en de dood veroorzaken. Vooral bij zeer warm weer lopen kinderen het meeste risico.
Terwijl zijn zoon Zonegran opneemt:
- Houd je kind koel, vooral bij erg warm weer
- Uw kind moet elke inspannende lichamelijke activiteit vermijden, vooral als het erg warm is
- Geef je kind voldoende koud water te drinken
- Uw kind mag deze geneesmiddelen niet gebruiken:
- koolzuuranhydraseremmers (zoals topiramaat en acetazolamide) en anticholinergica (zoals clomipramine, hydroxyzine, difenhydramine, haloperidol, imipramine en oxybutynine).
Als de huid van uw kind erg heet is, maar weinig of geen transpiratie heeft, als uw kind zich verward voelt, als hij spierkrampen heeft, of als zijn hartslag of ademhaling sneller gaat:
- Breng je kind naar een koele, schaduwrijke plek
- Je veegt de huid van je kind af met een spons gedrenkt in koud (maar niet koud) water
- Geef je kind koud water te drinken
- Neem dringend contact op met uw arts.
Lichaamsgewicht: Controleer elke maand het gewicht van uw kind en ga zo snel mogelijk naar uw arts als het gewicht van uw kind niet genoeg aankomt. Zonegran wordt niet aanbevolen voor kinderen met een lage eetlust of een laag gewicht en moet met voorzichtigheid worden gebruikt bij kinderen die minder dan 20 kg wegen.
Verhoogd zuurgehalte in het bloed en nierstenen: verklein deze risico's door ervoor te zorgen dat uw kind voldoende water drinkt en geen andere geneesmiddelen gebruikt die nierstenen kunnen veroorzaken (zie Andere geneesmiddelen). Uw arts zal de bicarbonaatspiegels in het bloed en de nieren van uw kind controleren (zie ook rubriek 4).
Geef dit geneesmiddel niet aan kinderen jonger dan 6 jaar, aangezien het bij deze leeftijdsgroep niet bekend is of de mogelijke voordelen opwegen tegen de risico's.
Interacties Welke medicijnen of voedingsmiddelen kunnen het effect van Zonegran veranderen
Vertel uw arts of apotheker als u andere geneesmiddelen gebruikt, kort geleden heeft gebruikt of in de nabije toekomst gaat gebruiken. Dit geldt ook voor geneesmiddelen die u zonder voorschrift kunt krijgen.
- Zonegran moet met voorzichtigheid worden gebruikt bij volwassenen, wanneer zij ook geneesmiddelen gebruiken die nierstenen kunnen veroorzaken, zoals topiramaat of acetazolamide. Bij kinderen wordt deze combinatie niet aanbevolen.
- Zonegran kan de spiegels van sommige geneesmiddelen, zoals digoxine en kinidine, in het bloed verhogen; daarom moet hun dosis mogelijk worden verlaagd.
- Andere geneesmiddelen, zoals fenytoïne, carbamazepine, fenobarbital en rifampicine, kunnen de spiegels van Zonegran in het bloed verlagen. Dit kan een aanpassing van de Zonegran-dosering vereisen.
Waarop moet u letten met eten en drinken?
Zonegran kan met of zonder voedsel worden ingenomen.
Waarschuwingen Het is belangrijk om te weten dat:
Zwangerschap, borstvoeding en vruchtbaarheid
Als u een vrouw bent die zwanger kan worden, moet u adequate anticonceptie gebruiken tijdens het gebruik van Zonegran en gedurende één maand na het stoppen ervan.
Als u zwanger bent of borstvoeding geeft, denkt zwanger te zijn of zwanger wilt worden, vraag dan uw arts om advies voordat u dit geneesmiddel inneemt.
U mag Zonegran alleen tijdens de zwangerschap innemen als uw arts u dat heeft verteld. Onderzoek heeft een verhoogd risico op geboorteafwijkingen aangetoond bij kinderen van vrouwen die worden behandeld met anti-epileptica.
Geef geen borstvoeding tijdens het gebruik van Zonegran of gedurende een maand nadat u bent gestopt met het innemen van Zonegran.
Er zijn geen klinische gegevens beschikbaar over de effecten van zonisamide op de vruchtbaarheid bij de mens Dierproeven hebben veranderingen in vruchtbaarheidsparameters aangetoond.
Rijvaardigheid en het gebruik van machines
Zonegran kan uw concentratie en uw reactie-/reactievermogen beïnvloeden en kan u slaperig maken, vooral aan het begin van de behandeling of na het verhogen van de dosis. Wees extra voorzichtig tijdens het rijden of het gebruik van machines als deze effecten optreden na het innemen van Zonegran.
Belangrijke informatie over enkele componenten van Zonegran
Zonegran bevat zonnegeel FCF (E110) en allurarood AC (E129). Zonegran harde capsules van 100 mg bevatten een gele kleurstof genaamd zonnegeel FCF (E110) en een rode kleurstof genaamd allurarood AC (E129), die allergische reacties kan veroorzaken.
Dosis, wijze en tijdstip van toediening Hoe Zonegran te gebruiken: Dosering
Gebruik dit geneesmiddel altijd precies zoals uw arts u dat heeft verteld. Raadpleeg bij twijfel uw arts of apotheker.
Aanbevolen dosis voor volwassenen
Als u Zonegran alleen gebruikt:
- De startdosering is 100 mg, eenmaal per dag ingenomen.
- Deze dosis kan met tussenpozen van één tot twee weken in stappen van maximaal 100 mg worden verhoogd.
- De aanbevolen dosering is eenmaal daags 300 mg.
Als u Zonegran samen met andere anti-epileptica gebruikt:
- De startdosering is 50 mg per dag, ingenomen in twee gelijke doses van 25 mg.
- Deze dosis kan met tussenpozen van één tot twee weken worden verhoogd tot 100 mg.
- De aanbevolen dagelijkse dosis ligt tussen 300 mg en 500 mg.
- Sommige mensen reageren op lagere doseringen. De dosis kan langzamer worden verhoogd in geval van bijwerkingen, ouderen of nier- of leverproblemen.
Gebruik bij kinderen (6 tot 11 jaar) en adolescenten (12 tot 17 jaar) met een lichaamsgewicht van ten minste 20 kg:
- De startdosering is 1 mg per kg lichaamsgewicht, eenmaal per dag ingenomen.
- Deze dosis kan worden verhoogd met 1 mg per kg lichaamsgewicht, met tussenpozen van één tot twee weken.
- De aanbevolen dagelijkse dosis is 6 tot 8 mg voor een kind dat tot 55 kg weegt of 300 tot 500 mg voor een kind dat meer dan 55 kg weegt (afhankelijk van wat de laagste is), eenmaal daags in te nemen.
Voorbeeld: Een kind dat 25 kg weegt, moet de eerste week eenmaal daags 25 mg innemen en vervolgens de dagelijkse dosis aan het begin van elke week met 25 mg verhogen totdat een dagelijkse dosis tussen 150 en 200 mg is bereikt.
Als u de indruk heeft dat het effect van Zonegran te sterk of te zwak is, neem dan contact op met uw arts of apotheker.
- Zonegran-capsules moeten heel worden doorgeslikt met water.
- Kauw niet op de capsules.
- Zonegran kan één of twee keer per dag worden ingenomen, volgens de instructies van de arts.
- Als u Zonegran tweemaal per dag inneemt, moet de helft van de dagelijkse dosis 's morgens en de andere helft 's avonds worden ingenomen.
Bent u vergeten Zonegran in te nemen?
- Als u een dosis vergeet in te nemen, hoeft u zich geen zorgen te maken en neem de volgende dosis wanneer het tijd is.
- Neem geen dubbele dosis om een vergeten dosis in te halen.
Als u stopt met het innemen van Zonegran
- Zonegran is bedoeld om langdurig te worden ingenomen. Verlaag de dosis niet en stop niet met het gebruik van dit geneesmiddel, tenzij uw arts u dat zegt.
- Als uw arts u adviseert om te stoppen met het gebruik van Zonegran, zal de dosis geleidelijk worden verlaagd om het risico op verdere aanvallen te verminderen.
Als u nog vragen heeft over het gebruik van dit geneesmiddel, neem dan contact op met uw arts of apotheker.
Overdosering Wat moet u doen als u te veel Zonegran heeft ingenomen?
Als het mogelijk is dat u meer Zonegran heeft ingenomen dan u zou mogen, informeer dan onmiddellijk uw verzorger (familielid of vriend), uw arts of apotheker, of neem contact op met de afdeling spoedeisende hulp van het dichtstbijzijnde ziekenhuis waar u het geneesmiddel gebruikt. Een te hoge dosis kan slaperigheid en bewustzijnsverlies veroorzaken.U kunt ook last krijgen van misselijkheid, maagpijn, spiertrekkingen, oogbewegingen, flauwvallen, trage hartslag en verminderde ademhaling en nierfunctie.Probeer niet te rijden.
Bijwerkingen Wat zijn de bijwerkingen van Zonegran
Zoals alle geneesmiddelen kan ook dit geneesmiddel bijwerkingen hebben, al krijgt niet iedereen daarmee te maken.
Zonegran behoort tot een groep geneesmiddelen (sulfonamiden) die ernstige allergische reacties, ernstige huiduitslag en bloedstoornissen kunnen veroorzaken, die in zeer zeldzame gevallen tot de dood kunnen leiden.
Neem onmiddellijk contact op met uw arts als:
- moeite heeft met ademhalen, zwelling van het gezicht, de lippen of de tong of ernstige huiduitslag, aangezien deze symptomen kunnen wijzen op een ernstige allergische reactie.
- tekenen van warmte heeft - verhoogde lichaamstemperatuur maar met weinig of geen zweten, snelle hartslag en snelle ademhaling, spierkrampen en verwardheid.
- gedachten heeft over zelfbeschadiging of zelfmoord. Een klein aantal mensen dat werd behandeld met anti-epileptica zoals Zonegran, heeft gedachten gehad over zelfbeschadiging of zelfmoord.
- spierpijn of een gevoel van zwakte heeft, aangezien dit een teken kan zijn van abnormale spierafbraak, wat kan leiden tot nierproblemen.
- u heeft plotselinge pijn in uw rug of maag, heeft pijn bij het plassen of merkt dat er bloed in uw urine zit, aangezien dit een teken kan zijn van nierstenen.
- visuele problemen, zoals oogpijn of wazig zien, treden op tijdens de behandeling met Zonegran.
Neem zo snel mogelijk contact op met uw arts als:
- er verschijnt een 'onverklaarbare uitslag, omdat deze zich kan ontwikkelen tot een ernstigere' uitslag of vervelling.
- u voelt zich ongewoon moe of koortsig, heeft een zere keel, gezwollen klieren of u merkt dat u snel blauwe plekken krijgt, aangezien dit een 'verandering in bloed' kan betekenen.
- tekenen van verhoogde zuurspiegels in het bloed verschijnen - hoofdpijn, slaperigheid, kortademigheid en verlies van eetlust Dit kan controle of behandeling door uw arts vereisen Uw arts kan besluiten om te stoppen met het gebruik van Zonegran De meest voorkomende bijwerkingen van Zonegran zijn mild Ze treden op tijdens de eerste maand van de behandeling en verdwijnen gewoonlijk bij voortzetting van de behandeling Bij kinderen van 6 tot 17 jaar kwamen de bijwerkingen overeen met de hieronder beschreven bijwerkingen, met de volgende uitzonderingen: longontsteking, uitdroging, verminderd zweten (vaak) en leverfunctiestoornissen. enzymafwijkingen (soms).
Zeer vaak voorkomende bijwerkingen (kunnen voorkomen bij meer dan 1 op de 10 mensen):
- agitatie, prikkelbaarheid, verwardheid, depressie.
- slechte spiercoördinatie, duizeligheid, slecht geheugen, slaperigheid, dubbelzien.
- verlies van eetlust, verlaging van het bicarbonaatgehalte in het bloed (een stof die voorkomt dat het bloed zuur wordt).
Vaak voorkomende bijwerkingen (kunnen voorkomen bij maximaal 1 op de 10 mensen):
- slaapproblemen, vreemde of ongewone gedachten, angst of emotionaliteit.
- vertraagde gedachten, concentratieverlies, spraakstoornissen, abnormaal gevoel op de huid (tintelingen), tremor, onwillekeurige oogbewegingen.
- nierstenen.
- huiduitslag, jeuk, allergische reacties, koorts, vermoeidheid, griepsymptomen, haaruitval.
- blauwe plekken (kleine blauwe plek op de huid veroorzaakt door een bloeding uit een gescheurd bloedvat).
- gewichtsverlies, misselijkheid, indigestie, maagpijn, diarree (dunne ontlasting), constipatie.
- zwelling van de voeten en benen.
Soms voorkomende bijwerkingen (komen voor bij minder dan 1 op de 100 gebruikers):
- woede, agressie, zelfmoordgedachten, zelfmoordpoging.
- Hij kokhalsde.
- ontsteking van de galblaas, galstenen.
- urinestenen.
- longinfectie/ontsteking, urineweginfecties.
- lage kaliumspiegels in het bloed, convulsies/toevallen.
Zeer zelden voorkomende bijwerkingen (kunnen voorkomen bij maximaal 1 op de 10.000 mensen):
- hallucinaties, geheugenverlies, coma, maligne neurolepticasyndroom (onvermogen om te bewegen, zweten, koorts, incontinentie), status epilepticus (langdurige of herhaalde aanvallen).
- ademhalingsproblemen, piepende ademhaling, ontsteking van de longen.
- ontsteking van de alvleesklier (ernstige pijn in de maag of rug).
- leverproblemen, nierfalen, verhoogde niveaus van creatinine (een afvalproduct dat normaal door de nieren wordt uitgescheiden) in het bloed.
- ernstige huiduitslag of vervelling (u kunt zich tegelijkertijd onwel voelen of koorts hebben).
- abnormale spierdegeneratie (u kunt spierpijn of spierzwakte voelen), wat kan leiden tot nierproblemen.
- gezwollen klieren, bloedveranderingen (vermindering van het aantal bloedcellen, waardoor de kans op infecties toeneemt en u er bleek uitziet, zich moe en koortsig voelt en blauwe plekken krijgt).
- verminderd zweten, overmatige verhoging van de lichaamstemperatuur.
- glaucoom, een verstopping van vocht in het oog die een verhoging van de oogdruk veroorzaakt. Oogpijn, wazig zien of verminderd zicht kunnen optreden, wat tekenen kunnen zijn van glaucoom.
Melding van bijwerkingen
Krijgt u last van bijwerkingen, neem dan contact op met uw arts of apotheker.Dit geldt ook voor mogelijke bijwerkingen die niet in deze bijsluiter staan. U kunt bijwerkingen ook rechtstreeks melden via het nationale meldsysteem zoals vermeld in aanhangsel V. Door bijwerkingen te melden, kunt u ons helpen meer informatie te verkrijgen over de veiligheid van dit geneesmiddel.
Vervaldatum en retentie
Buiten het zicht en bereik van kinderen houden.
Gebruik dit geneesmiddel niet meer na de uiterste houdbaarheidsdatum. Die is te vinden op de blisterverpakking en de doos na EXP/EXP. De vervaldatum verwijst naar de laatste dag van die maand.
Niet bewaren boven 30°C.
Gebruik dit geneesmiddel niet als u beschadiging van de capsules, blisterverpakking of doos of zichtbare tekenen van bederf van het geneesmiddel opmerkt. Breng de verpakking terug naar uw apotheker.
Gooi geneesmiddelen niet weg via het afvalwater of met huishoudelijk afval. Vraag uw apotheker wat u met geneesmiddelen moet doen die u niet meer gebruikt. Dit helpt het milieu te beschermen.
Andere informatie
Wat bevat Zonegran
De werkzame stof in Zonegran is zonisamide.
Zonegran 25 mg harde capsules bevatten 25 mg zonisamide. Zonegran 50 mg harde capsules bevatten 50 mg zonisamide. Zonegran 100 mg harde capsules bevatten 100 mg zonisamide.
- De andere ingrediënten in de capsule zijn microkristallijne cellulose, gehydrogeneerde plantaardige olie en natriumlaurylsulfaat.
- Het capsuleomhulsel bevat gelatine, titaniumdioxide (E171), schellak, propyleenglycol, kaliumhydroxide, zwart ijzeroxide (E172).Daarnaast bevat het capsuleomhulsel van 100 mg zonnegeel FCF (E110) en rode allura (E129).
Zie rubriek 2 voor belangrijke informatie over de hulpstoffen: zonnegeel FCF (E110) en allurarood AC (E129).
Hoe ziet Zonegran eruit en hoeveel zit er in een verpakking?
- Zonegran 25 mg harde capsules hebben een witte ondoorzichtige romp en een witte ondoorzichtige dop, bedrukt met een logo en "ZONEGRAN 25" in het zwart.
- Zonegran 50 mg harde capsules hebben een witte ondoorzichtige romp en een grijze ondoorzichtige dop, bedrukt met een logo en "ZONEGRAN 50" in het zwart.
- Zonegran 100 mg harde capsules hebben een witte ondoorzichtige romp en een rode ondoorzichtige dop, bedrukt met een logo en "ZONEGRAN 100" in het zwart.
Zonegran harde capsules zijn verpakt in blisterverpakkingen, geleverd in verpakkingen met:
- 25 mg: 14, 28, 56 en 84 capsules
- 50 mg: 14, 28, 56 en 84 capsules
- 100 mg: 28, 56, 84, 98 en 196 capsules.
Mogelijk zijn niet alle verpakkingsgrootten beschikbaar.
Bron Bijsluiter: AIFA (Italiaans Geneesmiddelenbureau). Inhoud gepubliceerd in januari 2016. De aanwezige informatie is mogelijk niet up-to-date.
Om toegang te hebben tot de meest actuele versie, is het raadzaam om de website van AIFA (Italian Medicines Agency) te bezoeken. Disclaimer en nuttige informatie.
01.0 NAAM VAN HET GENEESMIDDEL
ZONEGRAN 25 MG HARDE CAPSULES
02.0 KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
Elke harde capsule bevat 25 mg zonisamide.
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1.
03.0 FARMACEUTISCHE VORM
Harde capsule.
Witte ondoorzichtige body en witte ondoorzichtige kop, in reliëf gemaakt met een logo en "ZONEGRAN 25" in zwart.
04.0 KLINISCHE INFORMATIE
04.1 Therapeutische indicaties
Zonegran wordt aangeduid als:
• monotherapie bij de behandeling van partiële aanvallen, met of zonder secundaire generalisatie, bij volwassenen met nieuw gediagnosticeerde epilepsie (zie rubriek 5.1);
• adjuvante therapie bij de behandeling van partiële aanvallen, met of zonder secundaire generalisatie, bij volwassenen, adolescenten en kinderen vanaf 6 jaar.
04.2 Dosering en wijze van toediening
Dosering - Volwassenen
Verhoging van de dosis en onderhoudsdosis
Zonegran kan alleen worden ingenomen of worden toegevoegd aan een bestaande therapie bij volwassenen. De dosis moet worden getitreerd op basis van het klinische effect Aanbevolen dosisverhogingen en onderhoudsdoses worden weergegeven in tabel 1. Sommige patiënten, vooral degenen die geen CYP3A4-inducerende middelen gebruiken, kunnen reageren op lagere doses.
Oponthoud
Als het nodig is om de behandeling met Zonegran te staken, moet deze geleidelijk worden stopgezet (zie rubriek 4.4). In klinische onderzoeken bij volwassen patiënten werd een dosisverlaging van 100 mg met wekelijkse intervallen toegepast, met gelijktijdige dosisaanpassingen van de andere anti-epileptica (indien nodig).
Tabel 1. Volwassenen - Aanbevolen dosisverhoging en onderhoudsschema
Algemene doseringsaanbevelingen voor Zonegran bij speciale patiëntenpopulaties
Pediatrische patiënten (vanaf 6 jaar) Dosisverhoging en onderhoudsdosis
Zonegran moet worden toegevoegd aan bestaande therapie bij pediatrische patiënten vanaf 6 jaar. De dosis moet worden getitreerd op basis van het klinische effect.De aanbevolen dosisverhogingen en onderhoudsdoses worden weergegeven in tabel 2. Sommige patiënten, vooral degenen die geen CYP3A4-inducerende middelen gebruiken, kunnen reageren op lagere doses.
Artsen dienen de rubriek 'Patiëntwaarschuwing' (in de bijsluiter) onder de aandacht te brengen van pediatrische patiënten en hun ouders/verzorgers met betrekking tot de preventie van een zonnesteek (zie rubriek 4.4: Pediatrische patiënten).
Tabel 2. Pediatrische patiënten (vanaf 6 jaar) - Verhoging van de dosis en het regime van onderhoud aanbevolen
Opmerking:
tot. Om een adequate therapeutische dosis te behouden, is het noodzakelijk om het lichaamsgewicht van het kind te controleren en de dosis bij elke verandering aan te passen, tot een lichaamsgewicht van 55 kg. De dosering is 6-8 mg / kg / dag tot een maximale dosis van 500 mg / dag.
De veiligheid en werkzaamheid van Zonegran bij kinderen jonger dan 6 jaar of met een lichaamsgewicht van minder dan 20 kg zijn nog niet vastgesteld.
Er zijn beperkte gegevens in klinische onderzoeken bij patiënten die minder dan 20 kg wegen. Daarom moeten kinderen vanaf 6 jaar en die minder dan 20 kg wegen met voorzichtigheid worden behandeld.
Oponthoud
Als het nodig is om de behandeling met Zonegran te staken, moet deze geleidelijk worden stopgezet (zie rubriek 4.4). In klinische onderzoeken bij pediatrische patiënten werd het afbouwen van de dosis voltooid door de dosis wekelijks te verlagen in verlagingen van ongeveer 2 mg/kg (d.w.z. in overeenstemming met het schema weergegeven in tabel 3).
Tabel 3. Pediatrische patiënten (vanaf 6 jaar) - Programma voor geleidelijke afbouw van de aanbevolen dosis
Opmerking:
* Alle doses zijn bedoeld eenmaal per dag.
Bejaarden
Voorzichtigheid is geboden bij het starten van de behandeling met Zonegran bij oudere patiënten, aangezien er beperkte informatie is over het gebruik van Zonegran bij deze patiënten. Voorschrijvende artsen dienen ook rekening te houden met het veiligheidsprofiel van Zonegran (zie rubriek 4.8).
Patiënten met een verminderde nierfunctie
Voorzichtigheid is geboden bij de behandeling van patiënten met een gestoorde nierfunctie met Zonegran, aangezien er beperkte informatie over dergelijke patiënten is en langzamere titratie nodig kan zijn.Aangezien zonisamide en zijn metabolieten via de nieren worden uitgescheiden, dient de behandeling te worden gestaakt bij patiënten die acuut nierfalen ontwikkelen of bij wie een aanhoudende, klinisch significante stijging van het serumcreatinine wordt waargenomen.
Bij proefpersonen met een verminderde nierfunctie was de renale klaring van enkelvoudige doses zonisamide positief gecorreleerd met de creatinineklaring. De plasma-AUC van zonisamide was met 35% verhoogd bij proefpersonen met creatinineklaring
Patiënten met een verminderde leverfunctie
Het gebruik bij patiënten met een leverfunctiestoornis is niet onderzocht, daarom wordt het gebruik bij patiënten met een ernstige leverfunctiestoornis niet aanbevolen. Voorzichtigheid is geboden bij de behandeling van patiënten met een lichte tot matige leverfunctiestoornis bij wie een langzamere titratie van Zonegran nodig kan zijn.
Wijze van toediening
Zonegran harde capsules zijn voor oraal gebruik.
Effect van voedsel
Zonegran kan met of zonder voedsel worden ingenomen (zie rubriek 5.2).
04.3 Contra-indicaties
Overgevoeligheid voor de werkzame stof, voor één van de in rubriek 6.1 vermelde hulpstoffen of voor sulfonamiden.
04.4 Bijzondere waarschuwingen en passende voorzorgen bij gebruik
Uitslag van onverklaarbare aard
Ernstige huiduitslag, waaronder gevallen van Stevens-Johnson-syndroom, kan optreden in combinatie met Zonegran-therapie.
De mogelijkheid om de toediening van Zonegran stop te zetten bij patiënten die huiduitslag van onverklaarbare aard ontwikkelen, moet worden overwogen. Alle patiënten die huiduitslag ontwikkelen tijdens het gebruik van Zonegran moeten zorgvuldig worden geobserveerd, met bijzondere aandacht voor patiënten die gelijktijdig anti-epileptica krijgen die onafhankelijk van elkaar huiduitslag kunnen veroorzaken.
Toevallen op het moment van intrekking
In overeenstemming met de huidige klinische praktijk moet het staken van Zonegran bij patiënten met epilepsie gebeuren door middel van een geleidelijke dosisverlaging om de kans op aanvallen na het stoppen te verminderen Er zijn onvoldoende gegevens over het stopzetten van andere gelijktijdige anti-epileptica, zodra de aanval onder controle is bereikt met Zonegran als adjuvans, om monotherapie met Zonegran te bereiken. Gelijktijdige anti-epileptica moeten daarom met voorzichtigheid worden stopgezet.
Reacties op sulfonamiden
Zonegran is een benzisoxazolderivaat dat een sulfonamidegroep bevat. Ernstige immuungerelateerde bijwerkingen die in verband worden gebracht met geneesmiddelen die een sulfonamidegroep bevatten, zijn onder meer huiduitslag, allergische reacties en belangrijke hematologische afwijkingen, waaronder aplastische anemie, die in zeer zeldzame gevallen fataal zijn.
Gevallen van agranulocytose, trombocytopenie, leukopenie, aplastische anemie, pancytopenie en leukocytose zijn gemeld. Er is onvoldoende informatie om de mogelijke relatie tussen dosis/duur van de behandeling en deze gebeurtenissen te beoordelen.
Suïcidale gedachten en gedrag
Zelfmoordgedachten en zelfmoordgedrag zijn gemeld bij patiënten die voor verschillende indicaties werden behandeld met anti-epileptica. Een meta-analyse van placebogecontroleerde, gerandomiseerde klinische onderzoeken met anti-epileptica toonde ook een licht verhoogd risico op zelfmoordgedachten en zelfmoordgedrag aan. Het mechanisme van dit risico is niet bekend en de beschikbare gegevens sluiten de mogelijkheid van een verhoogd risico voor Zonegran niet uit.
Patiënten moeten daarom worden gecontroleerd op tekenen van zelfmoordgedachten en -gedrag en indien nodig moet een passende behandeling worden overwogen. Patiënten (en hun verzorgers) moeten worden geïnformeerd over de noodzaak om hun arts te raadplegen als er tekenen van zelfmoordgedachten of zelfmoordgedrag optreden.
Nierstenen
Bij sommige patiënten, vooral bij patiënten met aanleg voor het ontwikkelen van nefrolithiase, kan er een verhoogd risico zijn op nierstenen en gerelateerde tekenen en symptomen, zoals nierkoliek, nierpijn of pijn in de flank. Nefrolithiasis kan chronische nierschade veroorzaken. Risicofactoren voor nefrolithiasis zijn onder meer eerdere steenvorming, familiegeschiedenis van nefrolithiasis en hypercalciurie. Geen van deze risicofactoren kan een betrouwbare voorspeller zijn van het optreden van stenen tijdens de behandeling met zonisamide Patiënten die andere therapieën gebruiken met een risico op het ontwikkelen van nefrolithiase lopen mogelijk een verhoogd risico Verhoogde vochtinname en diurese Dit kan het risico op niersteenvorming helpen verminderen , vooral bij mensen met predisponerende risicofactoren.
Metabole acidose
Behandeling met Zonegran gaat gepaard met non-anion gap hyperchloremische metabole acidose (d.w.z. een afname van serumbicarbonaat tot onder het normale bereik in afwezigheid van chronische respiratoire alkalose). Deze metabole acidose wordt veroorzaakt door nierverlies van bicarbonaat als gevolg van het remmende effect van zonisamide op koolzuuranhydrase. Deze verstoring van de elektrolytenbalans is waargenomen bij het gebruik van Zonegran in placebogecontroleerde klinische onderzoeken en in de postmarketingperiode.Zonisamide-geïnduceerde metabole acidose treedt over het algemeen op bij het begin van de behandeling, hoewel gevallen zich op elk moment in de loop van de behandeling kunnen voordoen. Behandeling De verlaging van de bicarbonaatspiegels is gewoonlijk licht tot matig (gemiddelde verlaging van ongeveer 3,5 mEq/l bij een dagelijkse dosis van 300 mg bij volwassenen); ernstigere verlagingen kunnen zelden optreden bij patiënten acidose (zoals nierziekte, ernstige ademhalingsstoornissen) , status epilepticus, diarree, operatie, ketogeen dieet of medicijnen) kunnen de bicarbonaatverlagende effecten van zonisamide versterken.
Het risico op zonisamide-geïnduceerde metabole acidose lijkt frequenter en ernstiger te zijn bij jongere patiënten. Serumbicarbonaatspiegels moeten naar behoren worden beoordeeld en gecontroleerd bij patiënten die worden behandeld met zonisamide en die klinische aandoeningen hebben die predisponeren voor een verhoogd risico op acidose, bij patiënten met een verhoogd risico op het ontwikkelen van bijwerkingen van metabole acidose en bij patiënten met symptomen die wijzen op metabole acidose. ontwikkeling en persistentie van metabole acidose, moet worden overwogen de dosis te verlagen of Zonegran te staken (met een geleidelijke afbouw van het geneesmiddel), aangezien dit kan leiden tot de ontwikkeling van osteopenie.
Als besloten wordt om de toediening van Zonegran voort te zetten ondanks aanhoudende acidose, moet behandeling met alkali worden overwogen.
Zonegran moet met voorzichtigheid worden gebruikt bij volwassen patiënten die gelijktijdig worden behandeld met koolzuuranhydraseremmers, zoals topiramaat of acetazolamide, aangezien er onvoldoende gegevens zijn om een farmacodynamische interactie uit te sluiten (zie ook rubriek 4.4 Pediatrische patiënten en rubriek 4.5).
Zonnesteek
Gevallen van verminderd zweten en verhoogde lichaamstemperatuur zijn voornamelijk gemeld bij pediatrische patiënten (zie rubriek 4.4 Pediatrische patiënten voor volledige waarschuwing).
Voorzichtigheid is geboden bij volwassenen wanneer Zonegran gelijktijdig wordt voorgeschreven met andere geneesmiddelen die patiënten vatbaar maken voor hittegerelateerde aandoeningen; deze omvatten koolzuuranhydraseremmers en geneesmiddelen met anticholinerge activiteit (zie ook rubriek 4.4 Pediatrische patiënten).
Pancreatitis
Bij patiënten die Zonegran gebruiken en klinische tekenen en symptomen van pancreatitis ontwikkelen, wordt aanbevolen de pancreaslipase- en amylasespiegels te controleren. Als er aanwijzingen zijn voor pancreatitis, bij gebrek aan een andere duidelijke oorzaak, wordt aanbevolen de stopzetting van Zonegran te overwegen en een passende behandeling in te stellen.
Rabdomyolyse
Bij patiënten die Zonegran gebruiken en die ernstige spierpijn en/of spierzwakte ontwikkelen, met of zonder koorts, wordt evaluatie van markers van spierbeschadiging aanbevolen, waaronder serumcreatinefosfokinase- en aldolasespiegels. In het geval van een verhoging van deze parameters, bij afwezigheid van een andere duidelijke oorzaak, zoals een trauma of een grand mal aanval, wordt aanbevolen de stopzetting van Zonegran te overwegen en een passende behandeling in te stellen.
Vrouwen in de vruchtbare leeftijd
Vrouwen die zwanger kunnen worden, moeten adequate anticonceptie gebruiken tijdens de behandeling met Zonegran en gedurende één maand na het staken ervan (zie rubriek 4.6). Artsen die patiënten met Zonegran behandelen, moeten ervoor zorgen dat geschikte anticonceptie wordt gebruikt en moeten op basis van klinisch oordeel beoordelen of orale anticonceptiva of doseringen van orale anticonceptiva geschikt zijn voor de klinische toestand van de individuele patiënt.
Lichaamsgewicht
Zonegran kan gewichtsverlies veroorzaken. Een voedingssupplement of een verhoogde inname via de voeding kan worden overwogen als de patiënt tijdens de behandeling gewichtsverlies vertoont of ondergewicht heeft.Als er significant ongewenst gewichtsverlies optreedt, moet worden overwogen de behandeling met Zonegran te staken. Gewichtsverlies is mogelijk ernstiger bij kinderen (zie rubriek 4.4 Pediatrische patiënten).
Pediatrische populatie
Bovenstaande waarschuwingen en voorzorgen zijn ook van toepassing op adolescente en pediatrische patiënten. De volgende waarschuwingen en zorgen zijn meer relevant voor pediatrische en adolescente patiënten.
Hitteberoerte en uitdroging
Preventie van hyperthermie en uitdroging bij kinderen
Zonegran kan het zweten bij kinderen verminderen en tot hyperthermie leiden, en als het kind niet goed wordt behandeld, kan het hersenbeschadiging en de dood veroorzaken. Kinderen lopen het meeste risico, vooral als de buitentemperatuur hoog is.
Terwijl een kind Zonegran gebruikt:
Het kind moet koel blijven, vooral bij zeer hoge temperaturen
Het kind moet elke inspannende lichamelijke activiteit vermijden, vooral in het geval van hoge temperaturen
Het kind moet veel koud water drinken
Het kind mag deze geneesmiddelen niet gebruiken:
koolzuuranhydraseremmers (zoals topiramaat en acetazolamide) en anticholinergica (zoals clomipramine, hydroxyzine, difenhydramine, haloperidol, imipramine en oxybutynine).
IN AANWEZIGHEID VAN EEN VAN DE VOLGENDE SITUATIES, HEEFT HET KIND DRINGEND MEDISCHE HULP NODIG:
De huid is erg heet, maar er is weinig of geen transpiratie, of het kind voelt zich verward, of spierkrampen of zijn hartslag of ademhaling is snel.
Breng de baby naar een koele, schaduwrijke plek
Houd de babyhuid koel met wat water
Geef de baby koud water te drinken
Gevallen van verminderd zweten en verhoogde lichaamstemperatuur zijn voornamelijk gemeld bij pediatrische patiënten. In sommige gevallen werd een hitteberoerte vastgesteld, waarvoor behandeling in het ziekenhuis nodig was. Er werd melding gemaakt van een zonnesteek die klinische behandeling vereiste en de dood tot gevolg had. De meeste meldingen deden zich voor tijdens periodes van hitte.Artsen moeten met patiënten of zorgverleners de mogelijke ernst van een zonnesteek bespreken, de situaties waarin ze kunnen optreden en welke stappen moeten worden genomen in het geval van tekenen of symptomen.Patiënten of zorgverleners moeten worden gewaarschuwd voor de noodzaak om de hydratatie te handhaven en te vermijden blootstelling aan hoge temperaturen en zware lichamelijke inspanning, afhankelijk van de toestand van de patiënt Voorschrijvers dienen de aandacht en zorg van pediatrische patiënten aan hun ouders / verzorgers te vestigen op het advies in de bijsluiter met betrekking tot de preventie van zonnesteek en hyperthermie bij kinderen. van tekenen of symptomen van uitdroging, oligohydrose of hoge lichaamstemperaturen, overweeg dan de "onderbreking van Zonegran.
Zonegran mag bij pediatrische patiënten niet gelijktijdig worden gebruikt met andere geneesmiddelen die patiënten vatbaar maken voor hittegerelateerde aandoeningen; deze omvatten koolzuuranhydraseremmers en geneesmiddelen met anticholinerge activiteit.
Lichaamsgewicht
Gewichtsverlies, resulterend in een verslechtering van de algemene toestand en het niet innemen van anti-epileptica, is in verband gebracht met een fatale afloop (zie rubriek 4.8). Zonegran wordt niet aanbevolen bij pediatrische patiënten met ondergewicht (definitie in overeenstemming met WHO-categorieën voor voor leeftijd gecorrigeerde BMI) of ongeschikt.
De incidentie van gewichtsverlies is consistent in alle leeftijdsgroepen (zie rubriek 4.8). Gezien de mogelijke ernst van het verlies van lichaamsgewicht bij kinderen, is gewichtscontrole bij deze populatie echter vereist. Overweeg toediening van voedingssupplementen of een verhoogde voedselinname als het gewicht van de patiënt neemt niet congruent toe met groeigrafieken, anders moet Zonegran worden stopgezet.
Er zijn beperkte gegevens uit klinische onderzoeken bij patiënten met een lichaamsgewicht van minder dan 20 kg. Daarom moeten kinderen vanaf 6 jaar met een lichaamsgewicht van minder dan 20 kg voorzichtig worden behandeld. Het langetermijneffect van gewichtsverlies op de groei en ontwikkeling bij pediatrische patiënten is niet bekend.
Metabole acidose
Het risico op zonisamide-geïnduceerde metabole acidose lijkt frequenter en ernstiger te zijn bij pediatrische en adolescente patiënten. Passende beoordeling en controle van de serumbicarbonaatspiegels bij deze populatie is vereist (zie rubriek 4.4 - Metabole acidose voor volledige waarschuwing; zie rubriek 4.8 voor incidentie van lage bicarbonaatspiegels). Niet bekend. "langetermijneffect van lage bicarbonaatspiegels op groei en ontwikkeling.
Zonegran mag bij pediatrische patiënten niet gelijktijdig worden gebruikt met andere koolzuuranhydraseremmers zoals topiramaat en acetazolamide (zie rubriek 4.5).
Nierstenen
Stenen zijn opgetreden bij pediatrische patiënten (zie rubriek 4.4 Nierstenen voor de volledige waarschuwing). pijn Nefrolithiasis kan chronische nierschade veroorzaken Risicofactoren voor nefrolithiasis zijn eerdere steenvorming, familiegeschiedenis van nefrolithiasis en hypercalciurie Geen van deze risicofactoren kan een betrouwbare voorspeller zijn van het optreden van steen tijdens behandeling met zonisamide.
Een verhoogde vochtinname en uitscheiding via de urine kunnen het risico op stenen helpen verminderen, vooral bij patiënten met predisponerende risicofactoren.Renale echografie moet naar goeddunken van de arts worden uitgevoerd. Als er nierstenen worden gevonden, stop dan met de behandeling met Zonegran.
Leverfunctiestoornis
Verhoogde niveaus van hepatobiliaire parameters zoals alanineaminotransferase (ALAT), aspartaataminotransferase (AST), gamma-glutamyltransferase (GGT) en bilirubine zijn waargenomen bij pediatrische en adolescente patiënten, zonder consistent patroon in observaties van waarden boven de bovenste grens van normaal. . Als er echter een leveraandoening wordt vermoed, moet u de leverfunctie evalueren en overwegen om met Zonegran te stoppen.
Cognitie
Cognitieve stoornissen bij epileptische patiënten zijn in verband gebracht met de onderliggende ziekte en/of toediening van anti-epileptische therapieën. In een placebogecontroleerd onderzoek naar de toediening van zonisamide aan pediatrische en adolescente patiënten, was het aantal patiënten met cognitieve stoornissen numeriek hoger in de zonisamidegroep dan in de placebogroep.
04.5 Interacties met andere geneesmiddelen en andere vormen van interactie
Effect van Zonegran op cytochroom P450-enzymen
In vitro-onderzoeken met humane levermicrosomen hebben geen of slechte farmacokinetiek aangetoond (farmacokinetiek van andere geneesmiddelen via cytochroom P450-gemedieerde mechanismen, zoals in vivo aangetoond voor carbamazepine, fenytoïne, ethinylestradiol en desipramine.
Potentieel van Zonegran om andere geneesmiddelen te beïnvloeden
Anti-epileptica
Bij epileptische patiënten, toediening aan de stabiele toestand van Zonegran had geen klinisch relevante farmacokinetische effecten op carbamazepine, lamotrigine, fenytoïne of natriumvalproaat.
Orale anticonceptiva
In klinische onderzoeken bij gezonde proefpersonen had de steady-state toediening van Zonegran geen invloed op de serumconcentraties van ethinylestradiol of norethisteron in een gecombineerd oraal anticonceptivum.
Koolzuuranhydraseremmers
Zonegran moet met voorzichtigheid worden gebruikt bij volwassen patiënten die gelijktijdig worden behandeld met koolzuuranhydraseremmers, zoals topiramaat en acetazolamide, aangezien er onvoldoende gegevens zijn om een mogelijke farmacodynamische interactie uit te sluiten (zie rubriek 4.4).
Zonegran mag bij pediatrische patiënten niet gelijktijdig worden gebruikt met andere koolzuuranhydraseremmers zoals topiramaat en acetazolamide (zie rubriek 4.4 Pediatrische patiënten).
Substraten van P-gp
Een in-vitro-onderzoek toont aan dat zonisamide een zwakke remmer van P-gp (MDR1) is met een CI50 van 267 mol/l en er is een theoretische mogelijkheid dat zonisamide de farmacokinetiek beïnvloedt van stoffen die substraten zijn van P-gp. Voorzichtigheid is geboden bij het starten of stoppen van de behandeling met zonisamide of bij het veranderen van de dosis zonisamide bij patiënten die ook geneesmiddelen gebruiken die P-gp-substraten zijn (bijv. digoxine, kinidine).
Mogelijke geneesmiddelinteracties die van invloed zijn op Zonegran
In klinische onderzoeken had gelijktijdige toediening van lamotrigine geen duidelijk effect op de farmacokinetiek van zonisamide. De combinatie van Zonegran met andere geneesmiddelen die al een risico op urolithiasis inhouden, kan dit risico versterken, daarom dient gelijktijdige toediening van dergelijke geneesmiddelen te worden vermeden.
Zonisamide wordt gedeeltelijk gemetaboliseerd door CYP3A4 (reductieve splitsing) en ook door N-acetyltransferase en conjugatie met glucuronzuur; daarom kunnen stoffen die deze enzymen kunnen induceren of remmen de farmacokinetiek van zonisamide beïnvloeden:
Enzym-inductie: blootstelling aan zonisamide is lager bij epileptische patiënten die CYP3A4-inducerende middelen krijgen, zoals fenytoïne, carbamazepine en fenobarbital. Het is onwaarschijnlijk dat deze effecten klinisch significant zijn als Zonegran wordt toegevoegd aan een bestaande therapie. anti-epileptica of andere CYP3A4-inducerende geneesmiddelen worden stopgezet of geïntroduceerd, of hun dosering wordt aangepast; in dit geval kan een dosisaanpassing van Zonegran nodig zijn. Rifampicine is een krachtige inductor van CYP3A4. Als gelijktijdige toediening vereist is, dient de patiënt nauwlettend gevolgd en de dosis Zonegran en andere CYP3A4-substraten indien nodig aangepast.
• CYP3A4-remming: op basis van klinische gegevens lijkt het erop dat bekende remmers van CYP3A4, specifiek en niet-specifiek, geen klinisch relevant effect hebben op de farmacokinetische blootstellingsparameters van zonisamide. Steady-state toediening van ketoconazol (400 mg/dag) of cimetidine (1200 mg/dag) had geen klinisch relevante effecten op de farmacokinetiek van een enkelvoudige dosis zonisamide toegediend aan gezonde proefpersonen. Daarom zou er geen dosisaanpassing van Zonegran nodig moeten zijn bij gelijktijdige toediening met bekende CYP3A4-remmers.
Pediatrische populatie
Interactiestudies zijn alleen bij volwassenen uitgevoerd.
04.6 Zwangerschap en borstvoeding
Vrouwen in de vruchtbare leeftijd
Vrouwen die zwanger kunnen worden, dienen effectieve anticonceptie te gebruiken tijdens de behandeling met Zonegran en gedurende één maand na stopzetting ervan.
Zwangerschap
Er zijn geen toereikende gegevens over het gebruik van zonisamide bij zwangere vrouwen Dierproeven hebben reproductietoxiciteit aangetoond (zie rubriek 5.3) Het potentiële risico voor mensen is niet bekend.
Zonegran mag niet tijdens de zwangerschap worden gebruikt, tenzij het volgens de arts absoluut noodzakelijk is, en alleen als het mogelijke voordeel het risico voor de foetus rechtvaardigt. Bij patiënten die zwanger willen worden, dient rekening te worden gehouden met de noodzaak van een anti-epileptische behandeling. Als Zonegran wordt voorgeschreven, wordt zorgvuldige controle aanbevolen.
Vrouwen die zwanger kunnen worden, moeten deskundig advies krijgen om de optimale behandeling tijdens de zwangerschap te overwegen. Vrouwen die zwanger kunnen worden, dienen specialistisch advies te krijgen over de mogelijke effecten van Zonegran op de foetus en de risico's versus voordelen moeten met de patiënt worden besproken voordat met de behandeling wordt begonnen. Het risico op geboorteafwijkingen was 2 tot 3 keer verhoogd bij de kinderen van moeders die werden behandeld met anti-epileptica. De meest gerapporteerde zijn een hazenlip, cardiovasculaire misvormingen en neurale buisdefecten. Meervoudige therapie met anti-epileptica kan gepaard gaan met een hoger risico op aangeboren afwijkingen dan monotherapie.
Anti-epileptische therapie mag niet plotseling worden stopgezet, omdat dit kan leiden tot herhaling van de aanvallen, wat ernstige gevolgen kan hebben voor moeder en baby.
Voedertijd
Zonisamide wordt uitgescheiden in de moedermelk; de concentratie in moedermelk is vergelijkbaar met die in maternaal plasma. Er moet worden besloten of de borstvoeding moet worden gestaakt of dat de behandeling met Zonegran moet worden gestaakt/afgezien.Vanwege de lange retentietijd van zonisamide in het lichaam, mag de borstvoeding pas één maand na voltooiing van de behandeling met Zonegran worden hervat.
Vruchtbaarheid
Er zijn geen klinische gegevens beschikbaar over de effecten van zonisamide op de vruchtbaarheid bij de mens Dierstudies hebben veranderingen in vruchtbaarheidsparameters aangetoond (zie rubriek 5.3).
04.7 Beïnvloeding van de rijvaardigheid en het vermogen om machines te bedienen
Er is geen onderzoek gedaan naar de rijvaardigheid en het vermogen om machines te bedienen.Aangezien sommige patiënten echter slaperig kunnen worden of zich moeilijk kunnen concentreren, met name in de eerste fase van de behandeling of na een dosisverhoging, moeten patiënten worden geïnformeerd over de noodzaak om voorzichtig te zijn tijdens activiteiten die een hoge mate van alertheid vereisen, bijv. voertuigen besturen of machines bedienen.
04.8 Bijwerkingen
Samenvatting van het veiligheidsprofiel
Zonegran is in klinische onderzoeken aan meer dan 1200 patiënten gegeven, van wie er meer dan 400 Zonegran gedurende ten minste 1 jaar hebben gebruikt. Daarnaast is er uitgebreide postmarketingervaring met zonisamide in Japan sinds 1989 en in de Verenigde Staten sinds 2000.
Opgemerkt moet worden dat Zonegran een benzisoxazolderivaat is dat een sulfonamidegroep bevat. Ernstige immuungerelateerde bijwerkingen die in verband worden gebracht met geneesmiddelen die een sulfonamidegroep bevatten, zijn onder meer huiduitslag, allergische reacties en belangrijke hematologische afwijkingen, waaronder aplastische anemie, die in zeer zeldzame gevallen fataal kan zijn (zie rubriek 4.4).
De meest voorkomende bijwerkingen in gecontroleerde onderzoeken naar aanvullende therapie waren slaperigheid, duizeligheid en anorexia. De meest voorkomende bijwerkingen die werden waargenomen in een gerandomiseerde, gecontroleerde klinische studie met monotherapie waarin zonisamide werd vergeleken met carbamazepine met verlengde afgifte, waren verlaagde bicarbonaatspiegels, verminderde eetlust en gewichtsverlies.
17 mEq/l en meer dan 5 mEq/l) was 3,8%. De incidentie van duidelijk gewichtsverlies van 20% of meer was 0,7%.
Lijst van bijwerkingen in tabelvorm
Bijwerkingen die verband houden met Zonegran, verkregen uit klinische onderzoeken en postmarketingsurveillance, zijn samengevat in de onderstaande tabellen. De frequentie wordt gerapporteerd volgens het volgende schema:
zeer vaak ≥1 / 10
gemeenschappelijk ≥1 / 100,
ongewoon ≥1 / 1.000,
zeldzaam ≥1 / 10.000,
erg zeldzaam
niet bekend frequentie kan met de beschikbare gegevens niet worden bepaald
Tabel 4 Bijwerkingen geassocieerd met Zonegran, verkregen uit klinische therapiestudies aanvullend en post-marketing toezicht
Daarnaast zijn er geïsoleerde gevallen geweest van plotseling onverklaarbaar overlijden bij epileptische patiënten (SUDEP) die Zonegran gebruikten.
Tabel 5 Bijwerkingen in een gerandomiseerde gecontroleerde klinische studie met monotherapie, die: vergeleken zonisamide met carbamazepine met verlengde afgifte
† MedDRA versie 13.1
Aanvullende informatie over speciale populaties
Bejaarden
Een "gepoolde analyse van veiligheidsgegevens over 95 oudere proefpersonen toonde een relatief hoger aantal meldingen van perifeer oedeem en pruritus dan bij de volwassen populatie."
Beoordeling van post-marketinggegevens geeft aan dat, vergeleken met de algemene populatie, patiënten van 65 jaar en ouder de volgende voorvallen vaker melden: Stevens-Johnson-syndroom (SJS) en overgevoeligheidssyndroom voor geneesmiddelen (DIHS).
Pediatrische populatie
Het bijwerkingenprofiel van zonisamide bij pediatrische patiënten van 6 tot 17 jaar in placebogecontroleerde klinische onderzoeken was consistent met dat van volwassenen Onder 465 proefpersonen in de pediatrische veiligheidsdatabase (inclusief nog eens 67 proefpersonen uit de uitbreiding van het gecontroleerde klinische onderzoek). , waren er 7 sterfgevallen (1,5%; 14,6 / 1000 persoonsjaren): 2 gevallen van status epilepticus, waarvan één gecorreleerd met ernstig gewichtsverlies (10% binnen 3 maanden) bij een proefpersoon met ondergewicht, en vervolgens het uitblijven van medicamenteuze behandeling ; 1 geval van hoofdletsel/hematoom, en 4 sterfgevallen bij proefpersonen met eerdere functionele neurologische stoornissen, voor verschillende oorzaken (2 gevallen van sepsis veroorzaakt door pneumonie/orgaanfalen, 1 SUDEP en 1 hoofdletsel). In totaal 70,4% van de pediatrische patiënten die ZNS kregen in de gecontroleerde studie, of de open-label extensie, hadden ten minste één tijdens de behandeling optredende bicarbonaatmeting van minder dan 22 mmol/L. De persistentie van lage bicarbonaatspiegels was ook lang (mediaan 188 dagen).
Een "gepoolde analyse van veiligheidsgegevens van 420 pediatrische proefpersonen (183 proefpersonen in de leeftijd van 6 tot 11 jaar en 237 proefpersonen in de leeftijd van 12 tot 16 jaar, met een gemiddelde blootstellingsduur van ongeveer 12 maanden), toonde een relatief hoger aantal meldingen van pneumonie, uitdroging, verminderde transpiratie, abnormale leverfunctietesten, middenoorontsteking, faryngitis, sinusitis en bovenste luchtweginfectie, hoesten, epistaxis en rhinitis, buikpijn, braken, huiduitslag, eczeem en koorts, vergeleken met de volwassen populatie (vooral bij personen van minder dan 12 jaar), en ook een lage incidentie van amnesie, verhoogd creatinine, lymfadenopathie en trombocytopenie. De incidentie van gewichtsverlies van 10% of meer was 10,7% (zie rubriek 4.4). In sommige gevallen van gewichtsverlies was er een vertraging in de overgang naar het volgende Tanner-stadium en in de botrijping.
Melding van vermoedelijke bijwerkingen
Het melden van vermoedelijke bijwerkingen die optreden na toelating van het geneesmiddel is belangrijk omdat het een continue controle van de baten/risicoverhouding van het geneesmiddel mogelijk maakt.Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via het nationale meldsysteem.
04.9 Overdosering
Er zijn gevallen geweest van accidentele en opzettelijke overdosering bij volwassen en pediatrische patiënten. In sommige gevallen was een overdosis asymptomatisch, vooral wanneer braken of maagspoeling op tijd was. In andere gevallen werd de overdosering gevolgd door symptomen zoals slaperigheid, misselijkheid, gastritis, nystagmus, myoclonus, coma, bradycardie, verminderde nierfunctie, hypotensie en ademhalingsdepressie. Ongeveer 31 uur nadat een patiënt Zonegran en clonazepam had ingenomen, werd een zeer hoge plasmaconcentratie van 100,1 mcg/ml zonisamide geregistreerd; de patiënt raakte in coma en kreeg ademhalingsdepressie, maar kwam vijf dagen later weer bij bewustzijn en had geen gevolgen.
Behandeling
Er is geen specifiek antidotum beschikbaar voor een overdosis Zonegran. Na vermoedelijke recente overdosering kan maaglediging door maagspoeling of inductie van braken geïndiceerd zijn, met de gebruikelijke voorzorgsmaatregelen om de luchtwegen te beschermen. Algemene ondersteunende zorg is geïndiceerd, inclusief frequente controle van vitale functies en zorgvuldige observatie. Zonisamide heeft een lange eliminatiehalfwaardetijd, dus de effecten ervan kunnen in de tijd aanhouden. Hoewel het niet formeel is onderzocht voor de behandeling van overdosering, vermindert de "hemodialyse plasmaconcentraties van zonisamide bij een patiënt met een verminderde nierfunctie en kan worden overwogen als een behandeling voor overdosering indien klinisch geïndiceerd.
05.0 FARMACOLOGISCHE EIGENSCHAPPEN
05.1 Farmacodynamische eigenschappen
Farmacotherapeutische categorie: anti-epileptica, overige anti-epileptica, ATC-code: N03AX15
Zonisamide is een benzisoxazolderivaat. Het is een anti-epilepticum met een zwakke koolzuuranhydrase-activiteit in vitro. Het is chemisch niet verwant aan andere anti-epileptica.
Werkingsmechanisme
Het werkingsmechanisme van zonisamide is niet volledig bekend, maar het lijkt in te werken op spanningsafhankelijke natrium- en calciumkanalen, waardoor het gesynchroniseerde neuronale afvuren wordt belemmerd, de verspreiding van epileptische ontladingen wordt verminderd en de daaropvolgende epileptische activiteit wordt belemmerd.Zonisamide heeft ook een modulerend effect op GABA-gemedieerde neuronale remming.
Farmacodynamische effecten
De anticonvulsieve activiteit van zonisamide is geëvalueerd in verschillende modellen, bij verschillende soorten met geïnduceerde of spontane aanvallen, en zonisamide lijkt in deze modellen te werken als een breed spectrum anti-epilepticum. Zonisamide voorkomt maximale elektroshock-aanvallen en beperkt de verspreiding van aanvallen. de verspreiding van aanvallen van de cortex naar subcorticale structuren en onderdrukt de activiteit van de epileptogene focus. In tegenstelling tot fenytoïne en carbamazepine werkt zonisamide echter bij voorkeur bij aanvallen die afkomstig zijn uit de cortex.
Klinische werkzaamheid en veiligheid
Monotherapie bij partiële aanvallen, met of zonder secundaire generalisatie
De werkzaamheid van zonisamide als monotherapie werd vastgesteld in een non-inferioriteit, dubbelblinde vergelijking met parallelle groepen met carbamazepine met verlengde afgifte (RP) bij 583 volwassen proefpersonen met nieuw gediagnosticeerde partiële aanvallen, met of zonder tonische aanvallen secundaire gegeneraliseerde klonen. werden gerandomiseerd naar behandeling met carbamazepine en zonisamide, voor een duur van maximaal 24 maanden, afhankelijk van de respons. De proefpersonen werden getitreerd naar de initiële streefdosis van 600 mg carbamazepine of 300 mg zonisamide. De proefpersonen die een aanval kregen, werden getitreerd naar de volgende streefdosis , dwz 800 mg carbamazepine of 400 mg zonisamide. Proefpersonen die een "verdere aanval kregen, werden getitreerd tot de maximale streefdosis van 1200 mg carbamazepine of 500 mg zonisamide. Epileptische patiënten gedurende 26 weken bij het beoogde dosisniveau bleven deze dosis nog eens 26 weken gebruiken.
De belangrijkste resultaten van dit onderzoek zijn weergegeven in de onderstaande tabel:
Tabel 6 Werkzaamheidsresultaten voor monotherapie-onderzoek 310
PP = Bevolking volgens protocol; ITT = Intentie om de bevolking te behandelen
* Primair eindpunt
Adjuvante therapie bij de behandeling van partiële aanvallen, met of zonder secundaire generalisatie, bij volwassenen
Bij volwassenen werd de werkzaamheid van Zonegran aangetoond in 4 dubbelblinde, placebogecontroleerde onderzoeken met een duur van maximaal 24 weken, die een- of tweemaal daags werden toegediend.Deze onderzoeken tonen aan dat de mediane verlaging van de frequentie van aanvallen gedeeltelijk gerelateerd is aan de dosis Zonegran, met aanhoudende werkzaamheid bij doses van 300-500 mg per dag.
Pediatrische populatie
Adjuvante therapie bij de behandeling van partiële aanvallen, met of zonder secundaire generalisatie, bij adolescente en pediatrische patiënten (vanaf 6 jaar)
Bij pediatrische patiënten (vanaf 6 jaar) werd de werkzaamheid van zonisamide aangetoond in een dubbelblind, placebogecontroleerd onderzoek van 24 weken waaraan 207 proefpersonen deelnamen. Bij 50% van de met zonisamide behandelde proefpersonen en bij 31% van de met placebo behandelde proefpersonen werd een stabiele dosisperiode van een week gevonden.
De specifieke veiligheidsproblemen die naar voren kwamen in de pediatrische onderzoeken waren: verminderde eetlust en gewichtsverlies, verminderde bicarbonaatspiegels, verhoogd risico op nierstenen en uitdroging Al deze effecten, en meer specifiek gewichtsverlies, kunnen pathologische implicaties hebben voor de groei en in het lichaam ontwikkeling en kan leiden tot een algemene verslechtering van de gezondheidstoestand. Over het algemeen zijn langetermijngegevens over groei en ontwikkeling beperkt.
05.2 Farmacokinetische eigenschappen
Absorptie
Zonisamide wordt bijna volledig geabsorbeerd na orale toediening en bereikt doorgaans piekserum- of plasmaconcentraties binnen 2-5 uur na toediening. Aangenomen wordt dat het first-pass metabolisme verwaarloosbaar is. De absolute biologische beschikbaarheid wordt geschat op ongeveer 100%. De orale biologische beschikbaarheid wordt niet beïnvloed door voedsel, hoewel piekplasma- en serumconcentraties vertraagd kunnen worden.
De AUC- en Cmax-waarden van zonisamide stegen bijna lineair na een enkele dosis, over het dosisbereik van 100-800 mg en na meerdere doses over het dosisbereik van 100-400 mg eenmaal daags. De toename bij steady-state was iets groter dan verwacht door de dosis, mogelijk als gevolg van verzadigbare binding van zonisamide aan erytrocyten Steady-state werd bereikt binnen 13 dagen. Er treedt iets meer dan verwachte accumulatie op in vergelijking met enkelvoudige toediening.
Verdeling
Zonisamide wordt tijdens onderzoeken voor 40-50% aan menselijke plasma-eiwitten gebonden in vitro hebben aangetoond dat de aanwezigheid van verschillende anti-epileptica (zoals fenytoïne, fenobarbital, carbamazepine en natriumvalproaat) hier geen invloed op heeft. Het schijnbare distributievolume is ongeveer 1,1 - 1,7 l/kg bij volwassenen, wat aangeeft dat zonisamide wijd verspreid wordt in de weefsels. De verhouding erytrocyten tot plasma is ongeveer 15 bij lage concentraties en ongeveer 3 bij hogere concentraties.
Biotransformatie
Zonisamide wordt voornamelijk gemetaboliseerd door reductieve splitsing van de benzisoxazolring van het oorspronkelijke geneesmiddel door CYP3A4 om 2-sulfamoylacetylfenol (SMAP) te vormen en ook door N-acetylering.Het moedergeneesmiddel en SMAP kunnen ook worden geglucuronideerd.
metabolieten, die niet in plasma werden gedetecteerd, hebben geen anticonvulsieve activiteit. Er is geen bewijs dat zonisamide zijn eigen metabolisme induceert.
Eliminatie
De schijnbare klaring van zonisamide bij steady state na orale toediening is ongeveer 0,70 l/u en de terminale eliminatiehalfwaardetijd is ongeveer 60 uur, bij afwezigheid van CYP3A4-inductoren. De eliminatiehalfwaardetijd is onafhankelijk van de dosis en wordt niet beïnvloed door herhaalde administratie. De fluctuatie in serum- of plasmaconcentraties over een dosisinterval is laag (
Lineariteit / Niet-lineariteit
Blootstelling aan zonisamide neemt in de loop van de tijd toe totdat binnen ongeveer 8 weken steady-state wordt bereikt.Bij vergelijking van hetzelfde dosisniveau lijken proefpersonen met een hoger lichaamsgewicht lagere steady-state-serumconcentraties te hebben, maar dit effect lijkt relatief bescheiden te zijn.Leeftijd (≥ 12 jaar) jaar) en geslacht hebben, na correctie voor de effecten van lichaamsgewicht, geen duidelijk effect op de blootstelling aan zonisamide bij epileptische patiënten tijdens steady-state dosering. Er is geen dosisaanpassing nodig voor anti-epileptica, inclusief CYP3A4-inductoren.
Farmacokinetische / farmacodynamische relatie
Zonisamide vermindert de gemiddelde frequentie van aanvallen gedurende 28 dagen en deze vermindering is evenredig (log-lineair) met de gemiddelde concentratie van zonisamide.
Speciale patiëntengroepen
Bij mensen met een verminderde nierfunctie, renale klaring van enkelvoudige doses zonisamide was positief gecorreleerd met creatinineklaring. De plasma-AUC van zonisamide was met 35% verhoogd bij proefpersonen met creatinineklaring
Patiënten met een verminderde leverfunctie: De farmacokinetiek van zonisamide bij patiënten met een verminderde leverfunctie is niet voldoende onderzocht.
Bejaarden: Er werden geen klinisch significante verschillen in farmacokinetiek waargenomen tussen jonge (21 tot 40 jaar) en oudere (65 tot 75 jaar) proefpersonen.
Kinderen en adolescenten (5-18 jaar): Beperkte gegevens wijzen erop dat de farmacokinetiek bij kinderen en adolescenten bij steady-state doses van 1, 7 of 12 mg/kg per dag in verdeelde doses vergelijkbaar is met die waargenomen bij volwassenen na correctie voor lichaamsgewicht.
05.3 Gegevens uit het preklinisch veiligheidsonderzoek
Resultaten die niet zijn waargenomen in klinische onderzoeken, maar bij honden bij blootstellingsniveaus vergelijkbaar met klinisch gebruik, waren leververanderingen (vergroting, donkerbruine verkleuring, lichte toename van het hepatocytvolume met concentrische lamellaire lichamen in het cytoplasma en cytoplasmatische vacuolisatie) geassocieerd met een toename van het metabolisme .
Zonisamide was niet genotoxisch en heeft geen carcinogeen potentieel.
Zonisamide veroorzaakte afwijkingen in de ontwikkeling bij muizen, ratten en honden en was embryoletaal bij apen wanneer het werd toegediend tijdens de periode van organogenese bij zonisamidedosering en maternale plasmaspiegels vergelijkbaar met of lager dan therapeutische niveaus bij mensen.
In een toxiciteitsonderzoek met herhaalde doses bij jonge ratten, met vergelijkbare blootstellingsniveaus als die waargenomen bij pediatrische patiënten bij de maximaal aanbevolen dosis, werden gewichtsafnames en veranderingen in histopathologische en klinische pathologische parameters van de nieren waargenomen, evenals gedragsstoornissen. Veranderingen van histopathologische en klinische pathologische parameters die de nieren aantasten, zijn gecorreleerd met de remming van koolzuuranhydrase door zonisanide. De effecten bij deze dosis waren omkeerbaar tijdens de herstelperiode. Bij hogere doses (2-3 maal de systemische blootstelling, vergeleken met de therapeutische blootstelling) waren de effecten op de histopathologie van de nieren ernstiger en gedeeltelijk reversibel De meeste bijwerkingen die bij jonge ratten werden waargenomen, waren vergelijkbaar met de bijwerkingen die in onderzoeken werden gevonden. toxiciteit voor zonisamide bij volwassen ratten, maar het ontstaan van hyalinedruppels in niertubuli en transactionele hyperplasie werden alleen waargenomen in het onderzoek bij juveniele ratten Bij deze hogere dosis vertoonden jonge ratten verminderde relatieve parameters groei, leren en ontwikkeling Deze effecten werden waarschijnlijk geacht verband met gewichtsverlies en de krachtige farmacologische effecten van zonisamide bij de maximaal getolereerde dosis.
Bij ratten werden verminderingen van het aantal corpora lutea en implantatieplaatsen waargenomen bij blootstellingsniveaus die gelijk waren aan de maximale therapeutische dosis bij mensen; onregelmatige oestruscycli en een vermindering van het aantal levende foetussen werden waargenomen bij blootstellingsniveaus die driemaal hoger waren.
06.0 FARMACEUTISCHE INFORMATIE
06.1 Hulpstoffen
Capsule inhoud
Microkristallijne cellulose
Gehydrogeneerde plantaardige olie
Natriumlaurylsulfaat
Capsuleomhulsel
Gelei
Titaandioxide (E171)
Schellak
Propyleenglycol
Kaliumhydroxide
Zwart ijzeroxide (E172)
06.2 Incompatibiliteit
Niet relevant.
06.3 Geldigheidsduur
3 jaar.
06.4 Speciale voorzorgsmaatregelen bij bewaren
Niet bewaren boven 30°C.
06.5 Aard van de primaire verpakking en inhoud van de verpakking
PVC/PVDC/aluminium blisterverpakkingen, verpakkingen van 14, 28, 56 en 84 harde capsules.
Mogelijk worden niet alle verpakkingsgrootten in de handel gebracht.
06.6 Instructies voor gebruik en verwerking
Ongebruikte medicijnen en afval afkomstig van dit medicijn moeten worden weggegooid in overeenstemming met de lokale regelgeving.
07.0 HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Eisai Limited
Europees Kenniscentrum
Muggenmanier
Hatfield
Hertfordshire AL10 9SN Verenigd Koninkrijk
08.0 NUMMER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
EU/1/04/307/001
EU / 1/04/307/005
EU/1/04/307/002
EU / 1/04/307/013
036959017
036959029
036959056
09.0 DATUM VAN EERSTE VERGUNNING OF VERLENGING VAN DE VERGUNNING
Datum van eerste vergunning: 10/03/2005
Datum van laatste verlenging: 10/03/2010
10.0 DATUM VAN HERZIENING VAN DE TEKST
D.CCE december 2014