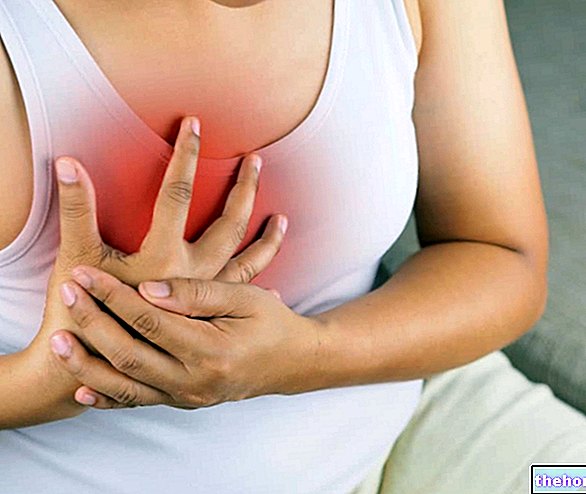
2,3-difosfoglyceraat (2,3 DPG) is een verbinding die is afgeleid van een tussenproduct van glycolyse; het is vooral geconcentreerd op het niveau van de erytrocyten, aangezien de rode bloedcellen - omdat ze geen mitochondriën hebben - het anaërobe melkzuurmetabolisme (homolactische fermentatie van glucose) benutten om energie te verkrijgen.

Hemoglobine is een tetrameer eiwit, dat bestaat uit vier subeenheden, twee alfa- en twee bèta, elk bestaande uit een eiwitgedeelte (globine) en een heem (prothetische groep die zuurstof bindt). Het 2,3-difosfoglyceraat hecht zich aan de bètaketens, waardoor ze worden verdicht en de affiniteit van hemoglobine voor zuurstof wordt verminderd.
De binding van de 2,3 DPG aan de hemoglobine vindt plaats wanneer het in de zuurstofarme vorm is, terwijl het in de longen wordt opgelost door de binding van het hemoglobine aan de zuurstof.In feite, wanneer het hemoglobine de weefsels bereikt, worden de β-ketens zijn de eersten die de zuurstof vrijgeven en dit verlies houdt een verplaatsing van de monomeren uit het centrum in.Zodra de interne hydrofiele holte opengaat, gaat de DPG het tetrameer binnen en bindt het zich aan de vorming van heteropolaire bindingen tussen zijn negatief geladen groepen en de lysine en histidine resten van de ketens Beta, positief geladen De gestabiliseerde structuur kan ook de zuurstof van de twee α-ketens afgeven. In de longen vindt echter het omgekeerde proces plaats; bij hoge zuurstofdruk zijn de α-ketens de eersten die het binden en wordt het DPG "geperst" en uit het tetrameer verdreven, waardoor een gemakkelijkere zuurstof-β-ketenbinding mogelijk is.
Het 2,3-bisfosfoglyceraat kan niet binden aan foetaal hemoglobine, omdat dit molecuul geen B-ketens heeft waarmee het 2,3-DPG bindt. Dit verklaart de grotere affiniteit voor zuurstof van foetaal hemoglobine dan hemoglobine van de moeder, een eigenschap die het foetale bloed in staat stelt om zuurstof uit het moederbloed halen.


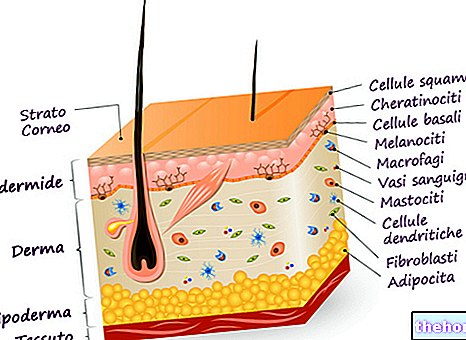








.jpg)