Actieve ingrediënten: naproxen, esomeprazol
VIMOVO 500 mg / 20 mg tabletten met gereguleerde afgifte
Indicaties Waarom wordt Vimovo gebruikt? Waar is het voor?
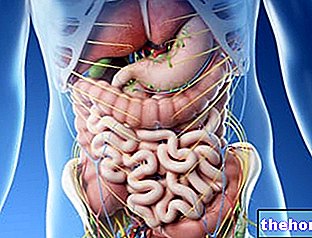
Wat is VIMOVO
VIMOVO bevat twee verschillende geneesmiddelen, naproxen en esomeprazol genaamd. Elk van deze medicijnen werkt anders.
- Naproxen behoort tot een groep geneesmiddelen die 'niet-steroïde anti-inflammatoire geneesmiddelen' (NSAID's) worden genoemd. Vermindert pijn en ontsteking.
- Esomeprazol behoort tot een groep geneesmiddelen die 'protonpompremmers' worden genoemd. Vermindert de hoeveelheid zuur in de maag.
Esomeprazol helpt het risico op het ontwikkelen van zweren en maagproblemen te verminderen bij patiënten die NSAID's gebruiken.
Waar is VIMOVO voor?
VIMOVO wordt gebruikt om de symptomen te verlichten van:
- Artrose.
- Reumatoïde artritis.
- Spondylitis ankylopoetica.
VIMOVO helpt pijn, zwelling, roodheid en warmte (ontsteking) te verlichten.
Dit geneesmiddel zal aan u worden toegediend als het waarschijnlijk wordt geacht dat een lagere dosis NSAID's niet effectief zal zijn bij het verlichten van pijn en als u een risico loopt op het ontwikkelen van een maagzweer of in het eerste deel (twaalfvingerige darm) van de dunne darm wanneer u NSAID's gebruikt.
Contra-indicaties Wanneer Vimovo niet mag worden gebruikt
Neem VIMOVO niet in als:
- Hij is allergisch (overgevoelig) voor naproxen.
- U bent allergisch voor esomeprazol of andere protonpompremmers.
- U bent allergisch voor één van de andere bestanddelen van VIMOVO (vermeld in rubriek 6: Aanvullende informatie).
- U gebruikt een geneesmiddel genaamd "atazanavir" of "nelfinavir" (gebruikt voor de behandeling van hiv).
- Acetylsalicylzuur (bijv. aspirine), naproxen of andere NSAID's zoals ibuprofen, diclofenac of COX-2-remmers (bijv. celecoxib, etoricoxib) hebben bij u astma (ademhalingsmoeilijkheden) of een allergische reactie zoals jeuk of huiduitslag (netelroos) veroorzaakt.
- Het is in de laatste 3 maanden van de zwangerschap.
- U heeft ernstige lever-, nier- of hartproblemen.
- U heeft een "zweertje in de maag of darmen".
- U heeft een ernstige, plotselinge bloedingsstoornis of bloeding.
Gebruik VIMOVO niet als u een van de bovengenoemde aandoeningen heeft. Raadpleeg bij twijfel uw arts of apotheker voordat u VIMOVO inneemt.
Voorzorgen bij gebruik Wat u moet weten voordat u Vimovo inneemt
Neem VIMOVO niet in en raadpleeg onmiddellijk uw arts als een van de onderstaande voorvallen optreedt vóór of tijdens het gebruik van VIMOVO, omdat dit geneesmiddel de symptomen van andere ziekten kan verbergen:
- Je verliest veel gewicht zonder reden en hebt moeite met slikken.
- Begin voedsel of bloed te braken.
- Aanwezigheid van zwarte ontlasting (aanwezigheid van verteerd bloed in de ontlasting).
Als een van de bovengenoemde voorvallen optreedt (of als u niet zeker bent), raadpleeg dan uw arts of apotheker voordat u dit geneesmiddel inneemt. Raadpleeg uw arts of apotheker voordat u dit geneesmiddel inneemt als:
- U heeft een darmontsteking (ziekte van Crohn of colitis ulcerosa).
- U heeft andere lever- of nierproblemen of u bent op leeftijd.
- U gebruikt geneesmiddelen zoals orale corticosteroïden, warfarine, selectieve serotonineheropnameremmers (SSRI's), acetylsalicylzuur (aspirine) of NSAID's waaronder COX-2-remmers (zie rubriek Gebruik met andere geneesmiddelen).
Als een van de bovengenoemde voorvallen optreedt (of als u niet zeker bent), raadpleeg dan uw arts of apotheker voordat u dit geneesmiddel inneemt.
Als u ooit een maagzweer of maagbloeding heeft gehad, vertel dit dan aan uw arts. U wordt gevraagd om ongebruikelijke maagklachten (bijv. pijn) aan uw arts te melden
Geneesmiddelen zoals VIMOVO kunnen in verband worden gebracht met een minimaal verhoogd risico op een hartaanval (myocardinfarct) of beroerte. Het risico is groter bij hoge doses en langdurige behandeling. De aanbevolen dosis of duur van de behandeling niet overschrijden.
Het gebruik van VIMOVO bij kinderen wordt niet aanbevolen.
Raadpleeg ook uw arts voordat u dit geneesmiddel inneemt als u hartproblemen heeft, een beroerte heeft gehad of als u denkt dat u risico loopt op een van deze problemen. U loopt mogelijk risico op een van deze problemen als:
- U heeft een hoge bloeddruk.
- U heeft problemen met de bloedsomloop of bloedstolling.
- Hij heeft suikerziekte.
- Hij heeft een hoog cholesterolgehalte.
- Hij is een roker.
Interacties Welke medicijnen of voedingsmiddelen kunnen het effect van Vimovo . veranderen
Vertel het uw arts of apotheker als u andere geneesmiddelen gebruikt of kort geleden heeft gebruikt, zoals geneesmiddelen die u zonder voorschrift kunt krijgen, inclusief kruidenproducten. Dit komt omdat VIMOVO invloed kan hebben op de manier waarop andere geneesmiddelen werken. Ook kunnen andere geneesmiddelen de werking van VIMOVO beïnvloeden.
Gebruik dit geneesmiddel niet en vertel uw arts of apotheker als u:
- een geneesmiddel genaamd "atazanavir" of "nelfinavir" (gebruikt bij de behandeling van hiv) Vertel uw arts of apotheker als u een van de volgende geneesmiddelen gebruikt:
- Acetylsalicylzuur (aspirine). Als u een lage dosis aspirine gebruikt, kunt u VIMOVO blijven gebruiken.
- Andere NSAID-geneesmiddelen (inclusief COX-2-remmers).
- Sommige geneesmiddelen zoals ketoconazol, itraconazol, posaconazol of voriconazol (gebruikt om infecties veroorzaakt door schimmels te behandelen).
- Erlotinib (of andere kankergeneesmiddelen van dezelfde klasse).
- Colestyramine (gebruikt om cholesterol te verlagen).
- Claritromycine (gebruikt om infecties te behandelen).
- Chinolon-antibiotica (voor infecties) zoals ciprofloxacine of moxifloxacine.
- Diazepam (gebruikt bij de behandeling van angst, om spieren te ontspannen of bij de behandeling van epilepsie).
- Idantoïnen en fenytoïne (gebruikt bij de behandeling van epilepsie).
- Lithium (gebruikt bij de behandeling van sommige vormen van depressie).
- Methotrexaat (gebruikt bij de behandeling van reumatoïde artritis, psoriasis en kankers).
- Probenecide (voor jicht).
- "Selectieve serotonineheropnameremmers" (SSRI's) (gebruikt bij de behandeling van ernstige depressie en angststoornissen).
- Ciclosporine of tacrolimus (geneesmiddelen die worden gebruikt om de immuunreacties van het lichaam te verminderen).
- Digoxine (gebruikt bij de behandeling van hartaandoeningen).
- Sulfonylureumderivaten zoals glimepiride (orale geneesmiddelen die bij diabetespatiënten worden gebruikt om de bloedsuikerspiegel onder controle te houden).
- Geneesmiddelen die worden gebruikt bij de behandeling van hoge bloeddruk, diuretica genaamd (zoals furosemide of hydrochloorthiazide), ACE-remmers (zoals enalapril) en bètablokkers (zoals propranolol).
- Corticosteroïdgeneesmiddelen zoals hydrocortison of prednisolon (gebruikt als ontstekingsremmende geneesmiddelen).
- Geneesmiddelen die worden gebruikt om de bloedstolling te blokkeren, zoals warfarine, dicumarol, heparine of clopidogrel.
- Rifampicine (gebruikt voor de behandeling van tuberculose).
- Sint-janskruid (Hypericum geperforeerd) (gebruikt voor de behandeling van lichte depressie).
- Cilostazol (gebruikt bij pijn in de benen als gevolg van een slechte doorbloeding).
Als een van de bovengenoemde voorvallen optreedt (of als u niet zeker bent), raadpleeg dan uw arts of apotheker voordat u VIMOVO inneemt.
Waarop moet u letten met eten en drinken?
Neem VIMOVO niet in met voedsel. Dit kan het effect van VIMOVO verminderen Neem de tabletten ten minste 30 minuten voor de maaltijd in.
Waarschuwingen Het is belangrijk om te weten dat:
Zwangerschap en borstvoeding
- Gebruik VIMOVO niet als u in de laatste 3 maanden van de zwangerschap bent.
- Raadpleeg uw arts voordat u dit geneesmiddel inneemt als u in het eerste of tweede trimester van de zwangerschap bent. Uw arts zal beslissen of u VIMOVO mag gebruiken.
- Geef geen borstvoeding als u VIMOVO gebruikt. Dit komt omdat kleine hoeveelheden van het geneesmiddel in de moedermelk terecht kunnen komen. Als u van plan bent borstvoeding te geven, mag u VIMOVO niet gebruiken.
Vraag uw arts of apotheker om advies voordat u een geneesmiddel inneemt als u zwanger bent, zwanger zou kunnen worden of borstvoeding geeft. VIMOVO kan de conceptie bemoeilijken. Vertel het uw arts als u van plan bent zwanger te worden of problemen heeft om zwanger te worden.
Rijvaardigheid en het gebruik van machines
U kunt zich duizelig of wazig voelen tijdens het gebruik van VIMOVO. Als dit gebeurt, rijd dan niet en gebruik geen gereedschap of machines.
Belangrijke informatie over enkele bestanddelen van VIMOVO
VIMOVO bevat methylparahydroxybenzoaat (E218) en propylparahydroxybenzoaat (E216), die allergische reacties kunnen veroorzaken. Deze reacties treden mogelijk niet onmiddellijk op
Dosis, wijze en tijdstip van toediening Hoe Vimovo te gebruiken: Dosering
Gebruik VIMOVO altijd precies zoals uw arts u dat heeft verteld. Raadpleeg bij twijfel uw arts of apotheker.
Inname van dit geneesmiddel
- Slik de tabletten heel door met een slok water U mag de tabletten niet kauwen, verdelen of fijnmaken Het is belangrijk om de tabletten in hun geheel in te nemen om het geneesmiddel goed te laten werken.
- Neem de tabletten ten minste 30 minuten voor de maaltijd in.
- Als u dit geneesmiddel gedurende lange tijd gebruikt, zal uw arts u willen controleren (vooral als u het langer dan een jaar gebruikt).
Hoeveelheid te nemen
- Neem tweemaal daags één tablet gedurende de tijd die uw arts u heeft verteld.
- VIMOVO is alleen verkrijgbaar in de sterkte 500 mg / 20 mg. Als uw arts denkt dat deze dosis niet geschikt voor u is, kan hij een andere therapie voorschrijven.
Overdosering Wat moet u doen als u te veel Vimovo heeft ingenomen?
Wat u moet doen als u meer van VIMOVO heeft ingenomen dan u zou mogen
Als u meer van VIMOVO heeft ingenomen dan u zou mogen, vertel dit dan onmiddellijk aan uw arts of apotheker. Symptomen van overdosering kunnen zijn: duizeligheid, slaperigheid, pijn in de bovenbuik en/of malaise, brandend maagzuur, misselijkheid, verwardheid, braken, maag- of darmbloeding, bewustzijnsverlies, ernstige zwelling van het gezicht, allergische reacties en onwillekeurige lichaamsbewegingen.
Wat u moet doen wanneer u bent vergeten VIMOVO . in te nemen
- Als u vergeten bent een dosis in te nemen, neem deze dan in zodra u eraan denkt dit te doen. Als het echter bijna tijd is voor de volgende dosis, sla dan de gemiste dosis over.
- Neem geen dubbele dosis (twee doses tegelijk) om een vergeten dosis in te halen.
Bijwerkingen Wat zijn de bijwerkingen van Vimovo
Zoals alle geneesmiddelen kan VIMOVO bijwerkingen hebben, al krijgt niet iedereen daarmee te maken. De volgende bijwerkingen kunnen optreden bij dit geneesmiddel.
Stop met het innemen van VIMOVO en ga onmiddellijk naar een arts als u een van de ernstige bijwerkingen opmerkt, aangezien u mogelijk dringende medische hulp nodig heeft:
- Plotseling piepende ademhaling, zwelling van de lippen, tong en keel of lichaam, huiduitslag, flauwvallen of moeite met slikken (ernstige allergische reactie).
- Roodheid van de huid met blaarvorming of peeling. Er kunnen ook ernstige blaarvorming en bloeding optreden in de lippen, ogen, mond, neus en geslachtsorganen.
- Geel worden van de huid of het wit van de ogen, donkere urine en vermoeidheid, wat symptomen van leverproblemen kunnen zijn.
- Geneesmiddelen zoals VIMOVO kunnen in verband worden gebracht met een minimaal verhoogd risico op een hartaanval (myocardinfarct) of beroerte. Tekenen zijn onder meer pijn op de borst die zich uitbreidt naar de nek en schouders en zich uitbreidt naar de linkerarm, een gevoel van verwarring of spierzwakte, of gevoelloosheid die zich slechts aan één kant van het lichaam kan voordoen.
- Aanwezigheid van zwarte plakkerige ontlasting of bloederige diarree.
- Braakt bloed of donkere deeltjes die op koffiedik lijken.
Vertel het uw arts zo snel mogelijk als u een van de volgende symptomen ervaart:
VIMOVO kan in zeldzame gevallen interfereren met het aantal of de functie van witte bloedcellen, wat resulteert in een immuundeficiëntie.
Als u een infectie heeft met symptomen zoals koorts met ernstige verslechtering van uw algemene toestand of koorts met symptomen van lokale infectie zoals pijn in de nek, keel of mond, of moeite met urineren, moet u zo snel mogelijk naar uw arts gaan zodat dat u met een bloedtest een tekort aan witte bloedcellen (agranulocytose) kunt uitsluiten. Het is belangrijk dat u op dit moment informatie over uw geneesmiddel verstrekt.
Andere mogelijke bijwerkingen zijn:
Vaak (komt voor bij 1 tot 10 gebruikers op 100)
- Hoofdpijn.
- Vermoeidheid.
- Dorst.
- Depressie.
- Piepende ademhaling.
- Verhoogd zweten.
- Jeukende huid en uitslag.
- Duizeligheid (duizeligheid).
- Rode of paarse vlekken, blauwe plekken of vlekken op de huid.
- Misselijkheid of braken.
- Snelle en lichte hartslagen (hartkloppingen).
- Verstoorde slaap of slaapproblemen (slapeloosheid).
- Gehoorproblemen zoals oorsuizen.
- Duizeligheid, slaperigheid of licht gevoel in het hoofd.
- Zwelling in de handen, voeten en enkels (oedeem).
- Ontsteking in de mond, pijn in de mond of mondzweren.
- Problemen met het gezichtsvermogen, zoals wazig zien, conjunctivitis of oogpijn.
- Diarree, maagpijn, brandend maagzuur, indigestie, constipatie, boeren of een opgeblazen gevoel (flatulentie
Soms, zelden of zeer zelden (komt voor bij 1 tot 10 op de 1.000 gebruikers of minder)
- Koorts.
- Flauwvallen.
- Droge mond
- Agressie.
- Gehoorverlies.
- Astma-aanval.
- Convulsies of toevallen.
- Problemen met de menstruatiecyclus.
- Gewichtsveranderingen.
- Haaruitval (alopecia).
- Verhoogde huiduitslag (netelroos).
- Gewrichtspijn (artralgie).
- Borstvergroting bij mannen.
- Pijnlijke of gezwollen tong.
- Onwillekeurige bewegingen of spiertrillingen.
- Problemen met eetlust of smaakveranderingen.
- Spierzwakte of pijn (myalgie).
- Bloedstolling kan langer duren dan normaal.
- Problemen met conceptie bij vrouwen.
- Koorts, roodheid of andere tekenen van infectie.
- Onregelmatige, langzame of zeer snelle hartslag.
- tintelingen.
- Moeite met geheugen of concentratie.
- Agitatie, verwarring, angst of rusteloosheid.
- Algemeen gevoel van malaise, zwakte en gebrek aan energie.
- Gezwollen of pijnlijke lichaamsdelen door verhoogde waterretentie.
- Hoge of lage bloeddruk. U kunt het gevoel hebben flauw te vallen of zich duizelig te voelen.
- Huiduitslag of blaren, of de huid wordt gevoeliger voor blootstelling aan de zon.
- Dingen zien, voelen of horen die er niet zijn (hallucinaties).
- Veranderingen in de resultaten van bloedonderzoeken, zoals die om de leverfunctie te controleren. Uw arts zal ze in detail kunnen uitleggen.
- Een infectie die "candidiasis" wordt genoemd en die het spijsverteringsstelsel kan aantasten en wordt veroorzaakt door een schimmel.
- Bloed in uw urine of andere nierproblemen U kunt rugpijn krijgen.
- Moeite met ademhalen, die langzaam erger kan worden. Dit kan een symptoom zijn van longontsteking of aanhoudende zwelling van de longen.
- Laag zoutgehalte (natrium) in het bloed. Dit kan zwakte, braken en krampen veroorzaken.
- symptomen van meningitis zoals koorts, misselijkheid of braken, stijve nek, hoofdpijn, gevoeligheid voor fel licht en verwardheid.
- Problemen met de alvleesklier. Symptomen zijn onder meer ernstige maagpijn die zich uitstrekt tot aan de rug.
- Lichtgekleurde ontlasting die een symptoom is van ernstige leverproblemen (hepatitis). Ernstige leverproblemen kunnen leiden tot leverfalen en hersenontsteking.
- Verergering van darmontsteking zoals de ziekte van Crohn of colitis ulcerosa. Symptomen zijn onder meer pijn, diarree, braken en gewichtsverlies.
- Bloedproblemen, zoals een lager aantal rode bloedcellen (bloedarmoede), witte bloedcellen of bloedplaatjes. Dit kan zwakte, blauwe plekken, koorts, ernstige tremoren, keelpijn veroorzaken of u kwetsbaarder maken voor infecties.
- Problemen met de manier waarop het hart bloed door het lichaam pompt of schade aan bloedvaten Symptomen kunnen zijn vermoeidheid, piepende ademhaling, flauwvallen, pijn op de borst of pijn in het algemeen.
- Laag magnesiumgehalte in het bloed (hypomagnesiëmie). U heeft mogelijk geen symptomen, tenzij uw niveaus erg laag zijn. In dit geval kunnen verwardheid, spierzwakte of krampen, onregelmatige hartslag of toevallen optreden.
Maak je geen zorgen over deze lijst met mogelijke bijwerkingen. Het is mogelijk dat er geen verschijnt.
Als een van de bijwerkingen ernstig wordt of als er bij u een bijwerking optreedt die niet in deze bijsluiter is vermeld, raadpleeg dan uw arts of apotheker.
Vervaldatum en retentie
Houd VIMOVO buiten het bereik en zicht van kinderen.
Gebruik VIMOVO niet meer na de vervaldatum die staat vermeld op de doos, fles of blister na EXP. De vervaldatum verwijst naar de laatste dag van de maand.
Niet bewaren boven 30°C.
Fles: Bewaren in de oorspronkelijke verpakking en de fles goed gesloten houden ter bescherming tegen vocht.
Blaren: Bewaren in de oorspronkelijke verpakking ter bescherming tegen vocht.
Geneesmiddelen dienen niet weggegooid te worden via het afvalwater of met huishoudelijk afval. Vraag uw apotheker wat u met geneesmiddelen moet doen die u niet meer gebruikt. Dit helpt het milieu te beschermen.
Wat bevat VIMOVO
- De actieve ingrediënten zijn naproxen 500 mg en esomeprazol 20 mg.
- De andere stoffen in de tabletkern zijn croscarmellosenatrium, magnesiumstearaat, povidon, colloïdaal siliciumdioxide en in de omhullende film zijn carnaubawas, glycerolmonostearaat 40-55, hypromellose, ijzeroxide (E172, geel, zwart), macrogol 8000, methacrylzuur-ethylacrylaatcopolymeer, methylparahydroxybenzoaat (E218), polydextrose, polysorbaat 80, propyleenglycol, propylparahydroxybenzoaat (E216), natriumlaurylsulfaat, titaandioxide (E171), triëthylcitraat
Beschrijving van het uiterlijk van VIMOVO en inhoud van de verpakking
Het zijn ovale, gele tabletten met de aanduiding 500/20 in zwarte inkt.
Fles:
Verpakkingsgrootten - 6, 20, 30, 60, 100, 180 of 500 tabletten met gereguleerde afgifte. De flesjes bevatten silicagel droogmiddelen (om de tabletten droog te houden).
Verpakking in aluminium blister:
Verpakkingsgrootten - 10, 20, 30, 60 of 100 tabletten met gereguleerde afgifte.
Mogelijk worden niet alle verpakkingsgrootten in de handel gebracht.
Bron Bijsluiter: AIFA (Italiaans Geneesmiddelenbureau). Inhoud gepubliceerd in januari 2016. De aanwezige informatie is mogelijk niet up-to-date.
Om toegang te hebben tot de meest actuele versie, is het raadzaam om de website van AIFA (Italian Medicines Agency) te bezoeken. Disclaimer en nuttige informatie.
01.0 NAAM VAN HET GENEESMIDDEL
VIMOVO 500 MG / 20 MG TABLETTEN MET GEWIJZIGDE AFGIFTE
02.0 KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
Elke tablet met gereguleerde afgifte bevat 500 mg naproxen en 20 mg esomeprazol (als magnesiumtrihydraat).
Hulpstoffen met bekende effecten:
VIMOVO bevat zeer lage, niet-beschermende hoeveelheden van 0,02 mg methylparahydroxybenzoaat en 0,01 mg propylparahydroxybenzoaat (zie rubrieken 4.4 en 6.1).
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1.
03.0 FARMACEUTISCHE VORM
Tablet met gereguleerde afgifte die maagsapresistente (maagsapresistente) naproxen en filmomhulde esomeprazol bevat.
Ovale, biconvexe, gele tablet met de aanduiding "500/20" in zwarte inkt.
04.0 KLINISCHE INFORMATIE
04.1 Therapeutische indicaties
VIMOVO is geïndiceerd bij volwassenen voor de symptomatische behandeling van osteoartritis, reumatoïde artritis en spondylitis ankylopoetica, bij patiënten met een risico op het ontwikkelen van maag- en/of duodenumzweren geassocieerd met behandeling met niet-steroïde anti-inflammatoire geneesmiddelen (NSAID's) en in gevallen waarin behandeling met lager dan naproxen of andere NSAID's wordt niet voldoende geacht.
04.2 Dosering en wijze van toediening
Dosering
De aanbevolen dosering is tweemaal daags 1 tablet (500 mg / 20 mg).
Bijwerkingen van naproxen kunnen tot een minimum worden beperkt door de laagst mogelijke effectieve dosis gedurende de kortst mogelijke periode te gebruiken (zie rubriek 4.4). Bij patiënten die niet eerder met NSAID's zijn behandeld, moet een lagere dagelijkse dosis naproxen of een andere NSAID worden overwogen. Hiervoor zijn niet-vaste associatieproducten beschikbaar. Wanneer de totale dagelijkse dosis van 1.000 mg naproxen niet adequaat wordt geacht (500 mg tweemaal daags), dienen alternatieve behandelingen met lagere doses naproxen of andere niet-vaste combinatie-NSAID's te worden gebruikt.
De behandeling moet worden voortgezet totdat de individuele behandeldoelen zijn bereikt, moet met regelmatige tussenpozen worden herzien en moet worden stopgezet als er geen voordeel of verslechtering is.
Vanwege de vertraagde afgifte van naproxen uit de enterisch gecoate formulering (3-5 uur), is VIMOVO niet bedoeld voor de snelle verlichting van acute pijnaandoeningen (zoals tandpijn). Opflakkeringen van artrose, reumatoïde artritis en spondylitis ankylopoetica kunnen echter worden behandeld met VIMOVO.
Speciale populaties
Patiënten met nierinsufficiëntie
Bij patiënten met lichte tot matige nierinsufficiëntie dient VIMOVO met voorzichtigheid te worden gebruikt en dient de nierfunctie nauwlettend te worden gecontroleerd. Een verlaging van de totale dagelijkse dosis naproxen moet worden overwogen (zie rubrieken 4.4 en 4.5). Wanneer de totale dagelijkse dosis van 1.000 mg naproxen niet adequaat wordt geacht (500 mg tweemaal daags), moeten alternatieve behandelingen met lagere doses naproxen of andere niet-vaste combinatie-NSAID's worden gebruikt en moet de noodzaak ook opnieuw worden beoordeeld. behandeling.
VIMOVO is gecontra-indiceerd bij patiënten met ernstige nierinsufficiëntie (creatinineklaring
Patiënten met leverinsufficiëntie
Bij patiënten met een lichte tot matige leverfunctiestoornis moet VIMOVO met voorzichtigheid worden gebruikt en moet de leverfunctie nauwlettend worden gecontroleerd. Een verlaging van de totale dagelijkse dosis naproxen moet worden overwogen (zie rubrieken 4.4 en 5.2). Wanneer de totale dagelijkse dosis van 1.000 mg naproxen niet adequaat wordt geacht (500 mg tweemaal daags), moeten alternatieve behandelingen met lagere doses naproxen of andere niet-vaste combinatie-NSAID's worden gebruikt en moet de maagbeschermende behandeling worden voortgezet.
VIMOVO is gecontra-indiceerd bij patiënten met een ernstige leverfunctiestoornis (zie rubrieken 4.3 en 5.2).
Ouderen (> 65 jaar)
Ouderen lopen een verhoogd risico op ernstige gevolgen van bijwerkingen (zie rubrieken 4.4 en 5.2). Wanneer de totale dagelijkse dosis van 1.000 mg naproxen (500 mg tweemaal daags) niet voldoende wordt geacht (bijv. bij ouderen met een verminderde nierfunctie of een laag lichaamsgewicht), moeten alternatieve behandelingen met lagere doses naproxen worden gebruikt. vaste combinatie NSAID's, en de noodzaak van voortzetting van de maagbeschermende behandeling moet ook opnieuw worden geëvalueerd.
Pediatrische patiënten (≤ 18 jaar)
De veiligheid en werkzaamheid van VIMOVO bij kinderen van 0-18 jaar zijn niet vastgesteld Er zijn geen gegevens beschikbaar.
Wijze van toediening
De VIMOVO-tablet moet heel worden doorgeslikt met een beetje water en mag niet worden gedeeld, gekauwd of fijngemaakt.
Het wordt aanbevolen om VIMOVO ten minste 30 minuten voor de maaltijd in te nemen (zie rubriek 5.2).
04.3 Contra-indicaties
• Overgevoeligheid voor de werkzame stoffen of voor één van de in rubriek 6.1 vermelde hulpstoffen of voor vervangende benzimidazolen
• Voorgeschiedenis van astma, urticaria of allergische reacties veroorzaakt door toediening van acetylsalicylzuur of andere NSAID's (zie rubriek 4.4)
• Derde trimester van de zwangerschap (zie rubriek 4.6)
• Ernstige leverinsufficiëntie (bijv. Child-Pugh C)
• Ernstig hartfalen
• Ernstige nierinsufficiëntie
• Actieve maagzweer (zie rubriek 4.4, Gastro-intestinale effecten, Naproxen)
• Gastro-intestinale bloeding, cerebrovasculaire bloeding of andere bloedingsstoornissen (zie rubriek 4.4, hematologische effecten)
• VIMOVO mag niet gelijktijdig worden gebruikt met atazanavir en nelfinavir (zie rubrieken 4.4 en 4.5).
04.4 Bijzondere waarschuwingen en passende voorzorgen bij gebruik
Algemeen
De combinatie van VIMOVO met andere NSAID's, waaronder selectieve cyclo-oxygenase-2-remmers, moet worden vermeden vanwege de cumulatieve risico's van het veroorzaken van ernstige NSAID-gerelateerde bijwerkingen. VIMOVO kan worden gebruikt bij patiënten die worden behandeld met een lage dosis acetylsalicylzuur (zie ook rubriek 4.5).
Bijwerkingen kunnen tot een minimum worden beperkt door de laagst mogelijke effectieve dosis te gebruiken voor de kortst mogelijke duur om de symptomen onder controle te houden (zie rubriek 4.2 en gastro-intestinale en cardiovasculaire effecten hieronder).
Om overbehandeling te voorkomen, moet de voorschrijvende arts met klinisch relevante tussenpozen, op basis van individuele risico's en op basis van de kenmerken en ernst van de onderliggende ziekte die wordt behandeld, beoordelen of voldoende pijnbeheersing met lagere doses NSAID's mogelijk is in niet-vaste verbanden.
Wanneer de totale dagelijkse dosis van 1.000 mg naproxen (500 mg tweemaal daags) niet voldoende wordt geacht, moeten alternatieve behandelingen met lagere doses naproxen of andere niet-vaste combinatie-NSAID's worden gebruikt en moet de noodzaak opnieuw worden beoordeeld om de maagbeschermende behandeling voort te zetten.
Risicofactoren voor de ontwikkeling van gastro-intestinale complicaties die verband houden met behandeling met NSAID's zijn onder meer hoge leeftijd, gelijktijdig gebruik van anticoagulantia, corticosteroïden, andere NSAID's, waaronder een lage dosis acetylsalicylzuur, slopende hart- en vaatziekten, infectie metHelicobacter pylori, evenals een voorgeschiedenis van maag- en / of darmzweren en bloedingen in het bovenste deel van het maagdarmkanaal.
Bij patiënten die aan de volgende aandoeningen lijden, mag naproxen alleen worden gebruikt na een grondige risico-batenanalyse:
• Geïnduceerde porfyrieën
• Systemische lupus erythematodes en ongedifferentieerde bindweefselziekte, aangezien bij deze patiënten zeldzame gevallen van aseptische meningitis zijn beschreven.
Patiënten die langdurig worden behandeld (met name degenen die langer dan een jaar worden behandeld) moeten periodiek worden gecontroleerd.
VIMOVO bevat zeer lage niveaus van methyl- en propylparahydroxybenzoaat, wat allergische reacties kan veroorzaken (soms vertraagd) (zie rubrieken 2 en 6.1).
Ouderen
Naproxen: Bij ouderen is er een verhoogde frequentie van bijwerkingen, met name gastro-intestinale bloedingen en perforaties, die fataal kunnen zijn (zie rubrieken 4.2 en 5.2). De esomeprazolcomponent van VIMOVO verminderde de incidentie van zweren bij ouderen.
Gastro-intestinale effecten
Naproxen: Gastro-intestinale bloedingen, ulceraties of perforaties, die fataal kunnen zijn, zijn gemeld bij alle NSAID's op elk moment tijdens de behandeling, met of zonder waarschuwingssymptomen of een "geschiedenis van ernstige gastro-intestinale voorvallen".
Het risico op gastro-intestinale bloeding, ulceratie of perforatie met NSAID's is hoger bij hogere doses NSAID's, bij patiënten met een "voorgeschiedenis van ulcer", vooral indien gecompliceerd met bloeding of perforatie (zie rubriek 4.3), en bij ouderen. start de behandeling met de laagst beschikbare doses. Voor deze patiënten en voor patiënten die gelijktijdig gebruik van een lage dosis acetylsalicylzuur of andere geneesmiddelen die het gastro-intestinale risico kunnen verhogen, moet een combinatietherapie worden overwogen met beschermende middelen (bijv. misoprostol of protonpompremmers) ( zie hieronder en 4.5). De esomeprazolcomponent van VIMOVO is een protonpompremmer.
Patiënten met een voorgeschiedenis van gastro-intestinale toxiciteit, met name ouderen, moeten ongebruikelijke abdominale symptomen (vooral gastro-intestinale bloedingen) melden, vooral in de vroege stadia van de behandeling.
Voorzichtigheid is geboden bij patiënten die NSAID's gelijktijdig gebruiken met geneesmiddelen die het risico op ulceratie of bloeding kunnen verhogen, zoals orale corticosteroïden, anticoagulantia zoals warfarine, selectieve serotonineheropnameremmers of plaatjesaggregatieremmers zoals acetylsalicylzuur (voor informatie over het gebruik van VIMOVO met een lage dosis acetylsalicylzuur, zie rubriek 4.5).
Met zweren samenhangende complicaties zoals bloeding, perforatie en obstructie zijn niet onderzocht in klinische onderzoeken met VIMOVO.
Als gastro-intestinale bloedingen of ulceraties optreden bij patiënten die VIMOVO gebruiken, moet de behandeling worden stopgezet (zie rubriek 4.3).
NSAID's dienen met voorzichtigheid te worden toegediend aan patiënten met een voorgeschiedenis van gastro-intestinale aandoeningen (colitis ulcerosa, ziekte van Crohn), aangezien deze aandoeningen kunnen verergeren (zie rubriek 4.8 - Bijwerkingen).
Esomeprazol: In het geval van alarmsymptomen (bijv. aanzienlijk onvrijwillig gewichtsverlies, herhaaldelijk braken, dysfagie, hematemesis of melaena) en in het geval van een vermoedelijke of aanwezige maagzweer, moet neoplasma worden uitgesloten, aangezien behandeling met magnesium esomeprazol de symptomen kan verlichten en diagnose uitstellen.
Dyspepsie kan nog steeds optreden ondanks de toevoeging van esomeprazol aan de tablet (zie rubriek 5.1).
Behandeling met protonpompremmers kan leiden tot een licht verhoogd risico op gastro-intestinale infecties, zoals die van:Salmonella En Campylobacter (zie rubriek 5.1).
Esomeprazol kan, net als alle zuurremmende geneesmiddelen, de absorptie van vitamine B12 (cyanocobalamine) verminderen na hypo- of achloorhydrie.Hiermee moet rekening worden gehouden bij patiënten met lage reserves of risicofactoren voor verminderde vitamine B12-absorptie. -termijn therapieën.
Cardiovasculaire en cerebrovasculaire effecten
Naproxen: Adequate monitoring en aanbevelingen zijn vereist voor patiënten met een voorgeschiedenis van arteriële hypertensie en/of licht tot matig congestief hartfalen, aangezien vochtretentie en oedeem zijn gemeld in verband met behandeling met NSAID's.
Klinisch onderzoek en epidemiologische gegevens suggereren dat het gebruik van coxibs en sommige NSAID's (vooral bij hoge doses en bij langdurige behandelingen) gepaard kan gaan met een licht verhoogd risico op arteriële trombotische voorvallen (bijv. myocardinfarct of beroerte). Hoewel de gegevens suggereren dat het gebruik van naproxen (1.000 mg per dag) kan gepaard gaan met een lager risico, een bepaald risico kan niet worden uitgesloten.
Patiënten met ongecontroleerde arteriële hypertensie, congestief hartfalen, vastgestelde ischemische hartziekte, perifere arteriële ziekte en/of cerebrovasculaire ziekte mogen alleen na zorgvuldige overweging met naproxen worden behandeld. Een soortgelijke overweging moet worden gemaakt voordat een langdurige behandeling wordt gestart bij patiënten met risicofactoren voor cardiovasculaire gebeurtenissen (bijv. arteriële hypertensie, hyperlipidemie, diabetes mellitus, roken).
Niereffecten
Naproxen: Langdurige toediening van NSAID's resulteerde in renale papillaire necrose en andere nierlaesies. Niertoxiciteit is ook waargenomen bij patiënten bij wie prostaglandinen een compenserende rol spelen bij het in stand houden van de nierperfusie.Bij deze patiënten kan toediening van NSAID's een dosisafhankelijke vermindering van de vorming van prostaglandine veroorzaken en, secundair, van de nierbloedstroom, wat duidelijk nierfalen kan veroorzaken. Patiënten met het grootste risico op deze reactie zijn patiënten met een verminderde nierfunctie, hypovolemie, hartfalen, leverdisfunctie, elektrolytenstoornissen, patiënten die diuretica, angiotensineconverterende enzymremmers (ACE-remmers) of antagonisten van angiotensinereceptor II en ouderen gebruiken. therapie wordt gewoonlijk gevolgd door terugkeer naar de toestand van voor de behandeling (zie ook hieronder en rubrieken 4.2 en 4.5).
Gebruik bij patiënten met een verminderde nierfunctie
Aangezien naproxen en zijn metabolieten voor het grootste deel (95%) worden geëlimineerd door excretie via de urine via glomerulaire filtratie, moet het met grote voorzichtigheid worden gebruikt bij patiënten met een verminderde nierfunctie en monitoring van serumcreatinine en/of serumcreatinine wordt aanbevolen bij deze patiënten. creatinineklaring. Het gebruik van VIMOVO is gecontra-indiceerd bij patiënten met een baseline creatinineklaring lager dan 30 ml/min (zie rubriek 4.3).
Hemodialyse verlaagt de plasmaconcentratie van naproxen niet vanwege de hoge mate van binding aan plasma-eiwitten.
Bepaalde patiënten, met name degenen bij wie de nierdoorbloeding is aangetast als gevolg van extracellulaire volumedepletie, levercirrose, natriumbeperking, congestief hartfalen en reeds bestaande nierziekte, dienen vóór en tijdens de behandeling met VIMOVO de nierfunctie te evalueren. Sommige ouderen bij wie de nierfunctie naar verwachting verminderd zal zijn, evenals patiënten die diuretica, ACE-remmers of angiotensinereceptor II-antagonisten gebruiken, vallen in deze categorie. Een verlaging van de dagelijkse dosering moet worden overwogen om de mogelijkheid van overmatige accumulatie van metabolieten van naproxen bij deze patiënten.
Levereffecten
Bij patiënten die NSAID's gebruiken, kunnen borderline-verhogingen van een of meer leverfunctietesten optreden. Leverafwijkingen kunnen eerder het gevolg zijn van overgevoeligheid dan van directe toxiciteit. Er zijn zeldzame meldingen geweest van ernstige leverreacties, waaronder geelzucht, fulminante hepatitis met een fataal verloop, levernecrose en leverfalen, sommige met fatale afloop.
Hepatorenaal syndroom
Het gebruik van NSAID's kan in verband worden gebracht met acuut nierfalen bij patiënten met ernstige levercirrose.Deze patiënten lijden ook vaak aan coagulopathie die verband houdt met onvoldoende synthese van stollingsfactoren. De plaatjesaggregatieremmende effecten gerelateerd aan naproxen kunnen het risico op ernstige bloedingen bij deze patiënten verder verhogen.
Hematologische effecten
Naproxen: Patiënten met bloedingsstoornissen of die medicamenteuze therapie krijgen die de hemostase verstoort, moeten nauwlettend worden gecontroleerd bij het toedienen van producten die naproxen bevatten.
Patiënten met een hoog bloedingsrisico en patiënten die een volledige anticoagulantiatherapie ondergaan (bijv. dicumarolderivaten) kunnen een verhoogd risico op bloedingen hebben bij gelijktijdig gebruik van producten die naproxen bevatten (zie rubriek 4.5).
Naproxen vermindert de bloedplaatjesaggregatie en verlengt de bloedingstijd.Met dit effect moet rekening worden gehouden bij het bepalen van de bloedingstijd.
Wanneer actieve en klinisch significante bloedingen optreden bij patiënten die VIMOVO gebruiken, ongeacht de oorzaak, moet de behandeling worden stopgezet.
Oftalmische effecten
Naproxen: Vanwege nadelige oftalmische effecten in dierstudies met NSAID's, wordt aanbevolen een oogheelkundig onderzoek uit te voeren in het geval dat er een visuele beperking of stoornis optreedt.
Dermatologische effecten
Naproxen: Ernstige huidreacties, waarvan sommige fataal, waaronder exfoliatieve dermatitis, Stevens-Johnson-syndroom en toxische epidermale necrolyse, zijn zeer zelden gemeld in verband met het gebruik van NSAID's (zie rubriek 4.8).Patiënten lijken maximaal blootgesteld te zijn. de start van de behandeling, aangezien de reacties in de meeste gevallen binnen de eerste maand van de behandeling optreden. VIMOVO moet worden gestaakt bij het eerste optreden van huiduitslag, slijmvliesletsels of enig ander teken van overgevoeligheid.
Anafylactische (anafylactoïde) reacties
Naproxen: Overgevoeligheidsreacties kunnen optreden bij gevoelige personen. Anafylactische (anafylactoïde) reacties kunnen optreden bij patiënten met en zonder een voorgeschiedenis van overgevoeligheid of blootstelling aan acetylsalicylzuur, andere NSAID's of producten die naproxen bevatten. Ze kunnen ook voorkomen bij personen met een "geschiedenis van angio-oedeem, bronchospastische reactiviteit (bijv. astma), rhinitis en neuspoliepen."
Reeds bestaande astma
Naproxen: Het gebruik van acetylsalicylzuur bij patiënten met acetylsalicylzuurgevoelig astma is in verband gebracht met ernstige bronchospasmen, die fataal kunnen zijn.Aangezien kruisreactiviteit, waaronder bronchospasmen, tussen acetylsalicylzuur en andere NSAID's is gemeld bij patiënten die gevoelig zijn voor acetylsalicylzuur, VIMOVO mag niet worden toegediend aan patiënten met deze vorm van gevoeligheid voor acetylsalicylzuur (zie rubriek 4.3) en moet met voorzichtigheid worden gebruikt bij patiënten met reeds bestaand astma.
Ontsteking
Naproxen: De antipyretische en ontstekingsremmende werking van naproxen kan koorts en andere tekenen van ontsteking verminderen, waardoor hun bruikbaarheid als diagnostische symptomen afneemt.
Vrouwelijke vruchtbaarheid
Het gebruik van VIMOVO kan, net als elk ander geneesmiddel waarvan bekend is dat het de cyclo-oxygenase/prostaglandinesynthese remt, de vrouwelijke vruchtbaarheid aantasten en wordt niet aanbevolen bij vrouwen die proberen zwanger te worden. Bij vrouwen die moeilijk zwanger kunnen worden of die onvruchtbaarheidstesten ondergaan, moet worden overwogen om de behandeling met VIMOVO stop te zetten (zie rubriek 4.6).
Combinatie met andere geneesmiddelen:
Gelijktijdige toediening van atazanavir en protonpompremmers wordt niet aanbevolen (zie rubriek 4.5). Als de combinatie van atazanavir en een protonpompremmer onvermijdelijk wordt geacht, wordt zorgvuldige klinische controle (bijv. viral load) aanbevolen in combinatie met een verhoging van de dosis atazanavir tot 400 mg met 100 mg ritonavir; de dosis esomeprazol mag niet hoger zijn dan 20 mg. mg en daarom mag VIMOVO niet gelijktijdig met atazanavir worden gebruikt (zie rubriek 4.3).
Esomeprazol is een CYP2C19-remmer. Mogelijke interactie met geneesmiddelen die door CYP2C19 worden gemetaboliseerd, moet worden overwogen bij het starten of beëindigen van de behandeling met esomeprazol.Er is een interactie waargenomen tussen clopidogrel en esomeprazol (zie rubriek 4.5). De klinische relevantie van deze interactie is onzeker. Uit voorzorg dient gelijktijdig gebruik van clopidogrel en esomeprazol te worden ontmoedigd.
Hypomagnesiëmie
Van protonpompremmers (PPI's) zoals esomeprazol is aangetoond dat ze ernstige hypomagnesiëmie veroorzaken bij patiënten die gedurende ten minste drie maanden en in veel gevallen gedurende één jaar worden behandeld. Ernstige symptomen van hypomagnesiëmie zijn vermoeidheid, tetanie, delirium, convulsies, duizeligheid en ventriculaire aritmie. Ze kunnen zich aanvankelijk verraderlijk manifesteren en worden verwaarloosd. Hypomagnesiëmie verbetert bij de meeste patiënten na inname van magnesium en het staken van de protonpompremmer Beroepsbeoefenaren in de gezondheidszorg dienen te overwegen de magnesiumspiegels te meten voordat de behandeling met PPI wordt gestart en periodiek tijdens de behandeling behandeling bij patiënten die langdurig worden behandeld of digoxine krijgen of geneesmiddelen die hypomagnesiëmie kunnen veroorzaken (bijv. diuretica).
Botbreuken
Protonpompremmers, vooral bij gebruik in hoge doses en gedurende langere perioden (> 1 jaar), kunnen een licht verhoogd risico op heup-, pols- en wervelkolomfracturen veroorzaken, vooral bij oudere mensen of in aanwezigheid van andere bekende risicofactoren. suggereren dat protonpompremmers het algehele risico op fracturen met 10% tot 40% kunnen verhogen. Deze toename kan gedeeltelijk te wijten zijn aan andere risicofactoren. Patiënten met een risico op osteoporose moeten worden behandeld volgens de huidige klinische praktijkrichtlijnen en moeten een "adequate hoeveelheid vitamine D en calcium.
04.5 Interacties met andere geneesmiddelen en andere vormen van interactie
Contra-indicaties voor gelijktijdig gebruik (zie rubriek 4.3)
Antiretrovirale middelen
Er zijn interacties gemeld tussen omeprazol, het racemische D+S-omeprazol (esomeprazol) en sommige antiretrovirale geneesmiddelen. De klinische relevantie en mechanismen van deze interacties zijn niet altijd bekend. De verhoging van de maag-pH tijdens de behandeling met omeprazol kan de absorptie van het antiretrovirale geneesmiddel veranderen. Andere mogelijke interactiemechanismen treden op via CYP2C19 Voor sommige antiretrovirale geneesmiddelen, zoals atazanavir en nelfinavir, zijn verlaagde serumspiegels gemeld bij toediening met omeprazol Gelijktijdige toediening van omeprazol (40 mg eenmaal daags) met atazanavir 300 mg/100 mg ritonavir bij gezonde vrijwilligers resulteert in een substantiële verlaging van de blootstelling aan atazanavir (ongeveer 75% verlaging van de AUC, Cmax en Cmin). Een verhoging van de dosis atazanavir tot 400 mg compenseert niet de invloed van omeprazol op de blootstelling aan atazanavir. Gelijktijdige toediening van omeprazol (40 mg/dag) verminderde de gemiddelde AUC, Cmax en Cmin van nelfinavir met 36-39% en de gemiddelde AUC, Cmax en Cmin van de farmacologisch actieve metaboliet M8 met 75-92,%.
Voor andere antiretrovirale geneesmiddelen, zoals saquinavir, zijn verhoogde serumspiegels gemeld. Er zijn ook enkele antiretrovirale geneesmiddelen waarvoor onveranderde serumspiegels zijn gemeld bij gelijktijdige toediening met omeprazol.
Er zijn geen interactiestudies van VIMOVO met atazanavir uitgevoerd, maar vanwege de vergelijkbare farmacodynamische en farmacokinetische eigenschappen van omeprazol en esomeprazol wordt gelijktijdig gebruik van atazanavir en nelfinavir met esomeprazol niet aanbevolen en is gelijktijdige toediening met VIMOVO gecontra-indiceerd (zie rubriek 4.3). ).
Gelijktijdig gebruik met voorzorg
Andere analgetica, waaronder selectieve cyclo-oxygenase-2-remmers:
Het gelijktijdig gebruik van twee of meer NSAID's moet worden vermeden, aangezien dit het risico op bijwerkingen kan verhogen, met name gastro-intestinale ulcera en bloedingen.Het gelijktijdige gebruik van VIMOVO met andere NSAID's, behalve een lage dosis acetylsalicylzuur (≤325 mg/dag), is niet aanbevolen (zie rubriek 4.4).
Acetylsalicylzuur
VIMOVO kan worden toegediend tijdens een behandeling met een lage dosis acetylsalicylzuur (≤ 325 mg/dag). In klinische onderzoeken was er geen toename van het aantal maagzweren bij patiënten die VIMOVO in combinatie met een lage dosis acetylsalicylzuur gebruikten in vergelijking met patiënten die VIMOVO alleen gebruikten (zie rubriek 5.1). Gelijktijdig gebruik van acetylsalicylzuur en VIMOVO kan echter het risico op ernstige bijwerkingen verhogen (zie rubrieken 4.4 en 4.8).
Tacrolimus
Zoals bij alle NSAID's is er een mogelijk risico op nefrotoxiciteit wanneer naproxen gelijktijdig wordt toegediend met tacrolimus.Er is gemeld dat gelijktijdige toediening van esomeprazol de serumspiegels van tacrolimus verhoogt. Tijdens de behandeling met VIMOVO moeten de serumtacrolimusconcentratie en de nierfunctie (creatinineklaring) nauwkeuriger worden gecontroleerd en moet de tacrolimusdosering zo nodig worden aangepast.
Cyclosporine
Zoals bij alle NSAID's is voorzichtigheid geboden bij gelijktijdige toediening van ciclosporine vanwege het verhoogde risico op nefrotoxiciteit.
diuretica
Klinische studies hebben, naast postmarketingobservaties, aangetoond dat NSAID's het natriuretische effect van furosemide en thiaziden bij sommige patiënten kunnen verminderen.Deze reactie is toegeschreven aan remming van de renale prostaglandinesynthese. Tijdens gelijktijdige behandeling met NSAID's moet de patiënt nauwlettend worden geobserveerd op tekenen van nierinsufficiëntie en op diuretische werkzaamheid (zie rubriek 4.4).
Selectieve serotonineheropnameremmers (SSRI's)
Gelijktijdig gebruik van NSAID's, inclusief selectieve COX-2-remmers, en SSRI's verhoogt het risico op gastro-intestinale bloedingen (zie rubriek 4.4).
Corticosteroïden
Er is een verhoogd risico op gastro-intestinale bloedingen wanneer corticosteroïden worden gecombineerd met NSAID's, inclusief selectieve COX-2-remmers.Voorzichtigheid is geboden wanneer NSAID's gelijktijdig worden toegediend met corticosteroïden (zie rubriek 4.4).
ACE-remmers / Angiotensine II-receptorantagonisten
Volgens sommige rapporten kunnen NSAID's het antihypertensieve effect van ACE-remmers en angiotensinereceptor II-antagonisten verminderen. NSAID's kunnen ook het risico op nierinsufficiëntie in verband met het gebruik van ACE-remmers of angiotensinereceptor II-antagonisten verhogen. De combinatie van NSAID's, ACE-remmers of angiotensinereceptor II-antagonisten dient met voorzichtigheid te worden toegediend aan oudere patiënten, patiënten met volumedepletie of nierinsufficiëntie (zie rubriek 4.4).
Digoxine
NSAID's kunnen de plasmaspiegels van hartglycosiden verhogen wanneer ze gelijktijdig worden toegediend met hartglycosiden zoals digoxine.
Lithium
NSAID's veroorzaakten een toename van de lithiumspiegels in het plasma en een afname van de renale klaring van lithium. Deze effecten zijn toegeschreven aan remming van de renale prostaglandinesynthese door NSAID's.Als NSAID's en lithium gelijktijdig worden toegediend, moeten proefpersonen daarom nauwlettend worden gecontroleerd op tekenen van lithiumtoxiciteit.
Methotrexaat
Bij toediening met protonpompremmers hebben sommige patiënten de neiging om de methotrexaatspiegels te verhogen. NSAID's hebben de neiging om de tubulaire secretie van methotrexaat in een diermodel te verminderen.Dit kan erop wijzen dat zowel esomeprazol als naproxen de toxiciteit van methotrexaat kunnen versterken. De klinische relevantie is waarschijnlijk groter bij patiënten die hoge doses methotrexaat krijgen en bij patiënten met nierdisfunctie. Voorzichtigheid is geboden wanneer VIMOVO gelijktijdig met methotrexaat wordt toegediend. Tijdelijke schorsing van VIMOVO wordt aanbevolen wanneer hoge doses methotrexaat worden toegediend.
Sulfonylurea, Idantoins
Naproxen is sterk gebonden aan plasma-albumine; daarom heeft het een theoretisch potentieel voor interactie met andere geneesmiddelen die aan albumine binden, zoals sulfonylureumderivaten en hydantoïnen. Patiënten die gelijktijdig met naproxen en een hydantoïne, sulfonamide of sulfonylureumderivaat worden toegediend, dienen te worden geobserveerd om de dosering indien nodig aan te passen.
Clopidogrel
De resultaten van onderzoeken bij gezonde proefpersonen lieten een "farmacokinetische (PK) / farmacodynamische (PD) interactie zien tussen clopidogrel (oplaaddosis 300 mg / 75 mg dagelijkse onderhoudsdosis) en esomeprazol (40 mg oraal dagelijks) met als gevolg een afname van de "blootstelling aan de actieve metaboliet van clopidogrel, gemiddeld met 40% en de daaruit voortvloeiende afname van maximale remming (ADP-geïnduceerd) van de bloedplaatjesaggregatie, gemiddeld met 14%."
In een onderzoek bij gezonde proefpersonen was er een afname in blootstelling van bijna 40% van de actieve metaboliet van clopidogrel wanneer een gecombineerde vaste dosis esomeprazol 20 mg en acetylsalicylzuur 81 mg werd toegediend met clopidogrel, vergeleken met clopidogrel alleen. De maximale remmingsniveaus (ADP-geïnduceerd) van de bloedplaatjesaggregatie bij deze proefpersonen waren echter hetzelfde in beide groepen.
Er zijn geen klinische onderzoeken uitgevoerd naar de interactie tussen clopidogrel en de gecombineerde vaste dosis naproxen + esomeprazol (VIMOVO).
In klinische en observationele onderzoeken zijn tegenstrijdige gegevens gerapporteerd over de klinische implicaties van de PK/PD-interactie van esomeprazol in termen van ernstige cardiovasculaire voorvallen.Als voorzorgsmaatregel dient gelijktijdig gebruik van VIMOVO en clopidogrel te worden ontmoedigd (zie rubriek 4.4).
Anticoagulantia en remmers van de bloedplaatjesaggregatie
NSAID's kunnen de effecten van orale anticoagulantia (bijv. warfarine, dicumarol), heparines en remmers van de bloedplaatjesaggregatie versterken (zie rubriek 4.4).
Gelijktijdige toediening van 40 mg esomeprazol aan met warfarine behandelde patiënten toonde aan dat, ondanks een lichte verhoging van de dalplasmaconcentratie van het minder krachtige R-isomeer van warfarine, de stollingstijden binnen het aanvaarde bereik lagen. Na gebruik na het in de handel brengen zijn er echter gevallen van hoge INR met klinische relevantie gemeld tijdens gelijktijdige behandeling met warfarine.Nauwkeurige controle wordt aanbevolen aan het begin en einde van de behandeling met warfarine of andere coumarinederivaten.
Bètablokkers
Naproxen en andere NSAID's kunnen het antihypertensieve effect van propranolol en andere bètablokkers verminderen.
probenecide
Probenecide gelijktijdig toegediend met naproxen verhoogt de plasmaspiegels van het naproxen-anion en verlengt de plasmahalfwaardetijd aanzienlijk.
Geneesmiddelen met pH-afhankelijke maagabsorptie
Onderdrukking van de maagzuursecretie tijdens behandeling met esomeprazol en andere PPI's kan de absorptie van geneesmiddelen waarvan de absorptie afhankelijk is van de pH van de maag, verlagen of verhogen.
Zoals met andere geneesmiddelen die de zuurgraad van de maag verminderen, kan de absorptie van geneesmiddelen zoals ketoconazol, itraconazol, posaconazol en erlotinib afnemen tijdens de behandeling met esomeprazol, terwijl de absorptie van geneesmiddelen zoals digoxine kan toenemen.
Gelijktijdige behandeling met posaconazol en erlotinib moet worden vermeden. Gelijktijdige behandeling met omeprazol (20 mg per dag) en digoxine bij gezonde proefpersonen verhoogde de biologische beschikbaarheid van digoxine tot 10% (tot 30% bij twee op de tien proefpersonen).
Meer informatie over geneesmiddelinteracties
Evaluatieonderzoeken naar de gelijktijdige toediening van esomeprazol en naproxen (niet-selectieve NSAID) of rofecoxib (COX-2-selectieve NSAID) identificeerden geen klinisch relevante interacties.
Net als bij andere NSAID's kan gelijktijdige toediening van colestyramine de absorptie van naproxen vertragen.
Bij gezonde vrijwilligers resulteerde gelijktijdige toediening van 40 mg esomeprazol in een toename van 32% van de oppervlakte onder de plasmaconcentratie-tijdcurve (AUC) en een verlenging van de eliminatiehalfwaardetijd (t½) van 31%, maar er was geen significante verhoging van de piekplasmaspiegels van cisapride. Het licht verlengde QTc-interval, dat werd waargenomen na toediening van cisapride als monotherapie, werd niet verder verlengd wanneer cisapride werd toegediend in combinatie met esomeprazol (zie ook rubriek 4.4).
Van esomeprazol is aangetoond dat het geen klinisch relevant effect heeft op de farmacokinetiek van amoxicilline en kinidine.
Esomeprazol remt CYP2C19, het belangrijkste metaboliserende enzym van esomeprazol. Esomeprazol wordt ook gemetaboliseerd door CYP3A4. Met betrekking tot deze enzymen werd het volgende waargenomen:
• Gelijktijdige toediening van 30 mg esomeprazol resulteerde in een vermindering van 45% in de klaring van het CYP2C19-substraat diazepam. Het is onwaarschijnlijk dat de interactie klinisch relevant is.
• Gelijktijdige toediening van 40 mg esomeprazol resulteerde in een stijging van 13% van de dalplasmaspiegels van fenytoïne bij epileptische patiënten.
• Gelijktijdige toediening van esomeprazol en een gecombineerde CYP2C19- en CYP3A4-remmer, zoals voriconazol, kan resulteren in een meer dan verdubbelde blootstelling aan esomeprazol.
• Gelijktijdige toediening van esomeprazol en een CYP3A4-remmer, claritromycine (500 mg tweemaal daags), resulteerde in een verdubbelde blootstelling (AUC) aan esomeprazol.
In geen van deze gevallen is aanpassing van de dosering van esomeprazol nodig.
Geneesmiddelen waarvan bekend is dat ze CYP2C19 of CYP3A4 of beide induceren (zoals rifampicine en sint-janskruid) kunnen leiden tot verlaagde serumspiegels van esomeprazol door een verhoogd metabolisme van esomeprazol.
Omeprazol werkt, net als esomeprazol, als een remmer van CYP2C19. Omeprazol, gegeven in doses van 40 mg aan gezonde proefpersonen in een cross-over onderzoek, verhoogde de Cmax en AUC van cilostazol met respectievelijk 18% en 26%, en een van zijn actieve metabolieten met maximaal 29% en 69, respectievelijk %.
Diergegevens wijzen erop dat NSAID's het risico op aanvallen geassocieerd met chinolon-antibiotica kunnen verhogen. Er kan een verhoogd risico zijn op het ontwikkelen van aanvallen bij patiënten die chinolonen gebruiken.
Geneesmiddel / laboratoriumtest interactie
Naproxen kan de bloedplaatjesaggregatie verminderen en de bloedingstijd verlengen. Met dit effect moet rekening worden gehouden bij het bepalen van de bloedingstijd.
Toediening van naproxen kan leiden tot hogere urinewaarden van 17-ketogene steroïden vanwege een "interactie tussen het geneesmiddel en / of zijn metabolieten met m-di-nitrobenzeen, dat voor deze test wordt gebruikt. Hoewel blijkbaar de waarden van 17 -hydroxy-corticosteroïden (Porter-Silber-test) niet worden gewijzigd, is het raadzaam om de behandeling met naproxen 72 uur voor het uitvoeren van de bijnierfunctietests tijdelijk te onderbreken, indien de Porter-Silber-test wordt gebruikt.
Naproxen kan interfereren met sommige urinaire doseringen van 5-hydroxy-indolazijnzuur (5HIAA).
04.6 Zwangerschap en borstvoeding
Zwangerschap
Naproxen:
Remming van de prostaglandinesynthese kan een nadelige invloed hebben op de zwangerschap en/of de ontwikkeling van het embryo/de foetus Gegevens uit epidemiologische onderzoeken wijzen op een verhoogd risico op spontane abortus en hartafwijkingen en gastroschisis na gebruik van een syntheseremmer van prostaglandines in het begin van de zwangerschap. Het absolute risico op hartafwijkingen nam toe van minder dan 1% tot ongeveer 1,5%. Aangenomen wordt dat het risico toeneemt met de dosis en de duur van de therapie. Bij dieren is aangetoond dat toediening van een prostaglandinesyntheseremmer leidt tot meer pre- en postimplantatieverlies en embryo-foetale letaliteit. Bovendien is een verhoogde incidentie van verschillende misvormingen, waaronder cardiovasculaire, gemeld bij dieren die tijdens de organogenetische periode een prostaglandinesyntheseremmer kregen toegediend (zie rubriek 5.3).
Bij vrouwen die proberen zwanger te worden of tijdens het eerste en tweede trimester van de zwangerschap, mag VIMOVO niet worden gegeven, tenzij het mogelijke voordeel voor de patiënt opweegt tegen het mogelijke risico voor de foetus. Als VIMOVO wordt gebruikt door een vrouw die van plan is zwanger te worden of tijdens het eerste en tweede trimester van de zwangerschap, moet de behandelingsduur zo kort mogelijk zijn.
Tijdens het derde trimester van de zwangerschap kunnen alle prostaglandinesyntheseremmers de foetus blootstellen aan:
• cardiopulmonale toxiciteit (met voortijdige sluiting van het arteriële kanaal en pulmonale hypertensie);
• nierfunctiestoornis, die zich kan ontwikkelen tot nierfalen met oligo-hydroamniose;
de moeder en de pasgeborene, aan het einde van de zwangerschap, om:
• mogelijke verlenging van de bloedingstijd, een antibloedplaatjeseffect dat zelfs bij zeer lage doses kan optreden.
• remming van de samentrekkingen van de baarmoeder, wat een vertraagde of langdurige bevalling veroorzaakt.
Daarom is VIMOVO gecontra-indiceerd tijdens het derde trimester van de zwangerschap (zie rubriek 4.3).
Esomeprazol:
Er is een beperkte hoeveelheid gegevens over het gebruik van esomeprazol bij zwangere vrouwen. Met het racemisch mengsel van omeprazol wijzen gegevens van epidemiologische onderzoeken bij een groter aantal aan behandeling blootgestelde zwangerschappen niet op de aanwezigheid van misvormende of foetotoxische effecten. Dierstudies met esomeprazol duiden niet op directe of indirecte schadelijke effecten op de ontwikkeling van het embryo/de foetus. Dierstudies met het racemische mengsel wijzen niet op directe of indirecte schadelijke effecten met betrekking tot zwangerschap, bevalling of postnatale ontwikkeling.
Voedertijd
Naproxen wordt in kleine hoeveelheden uitgescheiden in de moedermelk. Het is niet bekend of esomeprazol wordt uitgescheiden in de moedermelk. Een gepubliceerd casusrapport over een racemisch mengsel van omeprazol wees op de uitscheiding van kleine hoeveelheden in de moedermelk (voor gewicht aangepaste dosis
Vruchtbaarheid
Het gebruik van NSAID's zoals naproxen kan de vrouwelijke vruchtbaarheid verminderen.Het gebruik van VIMOVO wordt niet aanbevolen bij vrouwen die proberen zwanger te worden (zie rubriek 4.4).
04.7 Beïnvloeding van de rijvaardigheid en het vermogen om machines te bedienen
VIMOVO heeft geringe effecten op de rijvaardigheid of op het vermogen om machines te bedienen; op basis hiervan moet er rekening mee worden gehouden dat sommige van de gemelde bijwerkingen (bijv. duizeligheid) na het gebruik van VIMOVO het reactievermogen kunnen verminderen.
04.8 Bijwerkingen
Samenvatting van het veiligheidsprofiel
Esomeprazol met onmiddellijke afgifte is opgenomen in de tabletformulering om de incidentie van gastro-intestinale bijwerkingen veroorzaakt door naproxen te verminderen. Het is aangetoond dat VIMOVO maagzweren en bovenste gastro-intestinale bijwerkingen geassocieerd met NSAID's significant vermindert in vergelijking met naproxen alleen (zie rubriek 5.1). .
Er waren geen nieuwe gegevens over het veiligheidsprofiel tijdens de behandeling met VIMOVO in de totale populatie die werd geëvalueerd in klinische onderzoeken (n=1157) in vergelijking met de vastgestelde veiligheidsprofielen van de afzonderlijke werkzame stoffen naproxen en esomeprazol.
Getabelleerde samenvatting van bijwerkingen
Bijwerkingen zijn ingedeeld naar frequentie en systeem/orgaanklasse. Frequentiecategorieën worden gedefinieerd volgens de volgende conventie: Zeer vaak (≥1/10), Vaak (≥1/100 tot
VIMOVO
De volgende bijwerkingen zijn gemeld bij patiënten die VIMOVO gebruikten tijdens klinische onderzoeken.
* zoals opgemerkt door geplande routine-endoscopie
Naproxen
De volgende bijwerkingen zijn gemeld bij patiënten die naproxen gebruikten tijdens klinische onderzoeken en via postmarketingrapporten.
Esomeprazol :
De volgende bijwerkingen zijn vastgesteld of vermoed tijdens het klinische proefprogramma voor maagsapresistente esomeprazol en/of bij gebruik na het in de handel brengen.Geen daarvan is vastgesteld als dosisgerelateerd.
Beschrijving van bepaalde bijwerkingen
Naproxen
Klinische studies en epidemiologische gegevens suggereren dat het gebruik van coxibs en sommige NSAID's (vooral bij hoge doses en bij langdurige behandelingen) gepaard kan gaan met een licht verhoogd risico op arteriële trombotische voorvallen (bijv. myocardinfarct of beroerte). gebruik van naproxen (1.000 mg per dag) kan gepaard gaan met een lager risico, een bepaald risico kan niet worden uitgesloten (zie rubriek 4.4).
Oedeem, arteriële hypertensie en hartfalen zijn gemeld in verband met behandeling met NSAID's.
De meest waargenomen bijwerkingen zijn gastro-intestinaal van aard. Maagzweren, gastro-intestinale perforatie of bloeding, soms fataal, kunnen optreden, vooral bij ouderen (zie rubriek 4.4). Misselijkheid, braken, diarree, flatulentie, constipatie, dyspepsie, buikpijn, melaena, hematemesis, ulceratieve stomatitis, verergering van colitis en de ziekte van Crohn (zie rubriek 4.4 - Bijzondere waarschuwingen en voorzorgen bij gebruik) zijn gemeld na toediening van het geneesmiddel Gastritis werd minder vaak waargenomen.
VIMOVO is ontwikkeld met esomeprazol om de incidentie van gastro-intestinale bijwerkingen van naproxen te verminderen en er is aangetoond dat het het optreden van maag- en/of duodenumzweren en bovenste gastro-intestinale bijwerkingen geassocieerd met NSAID's significant vermindert in vergelijking met naproxen bij monotherapie.
Melding van vermoedelijke bijwerkingen
Het melden van vermoedelijke bijwerkingen die optreden na toelating van het geneesmiddel is belangrijk omdat het een continue monitoring van de baten/risicoverhouding van het geneesmiddel mogelijk maakt. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via het nationale meldsysteem. "adres https: //www.aifa.gov.it/content/segnalazioni-reazioni-avverse.
04.9 Overdosering
Er zijn geen klinische gegevens over overdosering met VIMOVO.
Eventuele effecten van een overdosis VIMOVO zullen naar verwachting in de eerste plaats de effecten van een overdosis naproxen weerspiegelen.
Symptomen
Geassocieerd met een overdosis naproxen
Een significante overdosis naproxen kan worden gekenmerkt door lethargie, duizeligheid, slaperigheid, epigastrische pijn, buikpijn, brandend maagzuur, indigestie, misselijkheid, voorbijgaande veranderingen in de leverfunctie, hypoprotrombinemie, nierdisfunctie, metabole acidose, apneu, desoriëntatie of braken.
Gastro-intestinale bloedingen kunnen optreden. Hoge bloeddruk, acuut nierfalen, ademhalingsdepressie en coma kunnen voorkomen, hoewel zelden. Er zijn anafylactoïde reacties gemeld bij behandeling met NSAID's, die kunnen optreden na een overdosis. Sommige patiënten kregen epileptische aanvallen, maar het is onduidelijk of ze verband hielden met het medicijn. Het is niet bekend welke dosis van het medicijn levensbedreigend kan zijn.
Geassocieerd met een overdosis esomeprazol
De symptomen beschreven in verband met de vrijwillige overdosering van esomeprazol (beperkte ervaring met doses hoger dan 240 mg/dag) zijn van voorbijgaande aard. Enkelvoudige doses van 80 mg esomeprazol hadden geen gevolgen.
Beheer
Geassocieerd met naproxen
Patiënten moeten worden behandeld met symptomatische en ondersteunende therapie na een overdosis NSAID's, met name met betrekking tot gastro-intestinale effecten en nierinsufficiëntie. Er zijn geen specifieke antidota.
Hemodialyse verlaagt de plasmaconcentratie van naproxen niet vanwege de hoge mate van eiwitbinding. Emesis en/of actieve kool (60 tot 100 g bij volwassenen, 1 tot 2 g/kg bij kinderen) en/of een osmotische catharsis kunnen geïndiceerd zijn bij patiënten die symptomen ervaren binnen 4 uur na inname of na een significante overdosis. Geforceerde diurese, urine-alkalisatie of hemoperfusie zijn mogelijk niet nuttig vanwege de hoge eiwitbinding.
Geassocieerd met esomeprazol
Er zijn geen specifieke antidota bekend. Esomeprazol heeft een sterke plasma-eiwitbinding en is daarom niet gemakkelijk dialyseerbaar. Zoals in elk geval van overdosering, dient de behandeling symptomatisch te zijn en dienen algemene ondersteunende maatregelen te worden genomen.
05.0 FARMACOLOGISCHE EIGENSCHAPPEN
05.1 Farmacodynamische eigenschappen
Farmacotherapeutische categorie: naproxen en esomeprazol ATC-code: M01AE52
Werkingsmechanisme
VIMOVO is ontwikkeld als tabletten met sequentiële afgifte, een combinatie van een esomeprazolmagnesiumlaag met onmiddellijke afgifte en een maagsapresistente naproxenkern met vertraagde afgifte. Esomeprazol wordt vervolgens in de maag afgegeven voordat naproxen in de dunne darm oplost.De enterische coating voorkomt de afgifte van naproxen bij pH-waarden onder 5, waardoor bescherming wordt geboden tegen de mogelijke lokale maagtoxiciteit van naproxen.
Vanwege de vertraagde afgifte van naproxen is VIMOVO niet bedoeld of onderzocht voor de behandeling van acute pijn.
Naproxen is een NSAID met pijnstillende en koortswerende eigenschappen. Het werkingsmechanisme van het naproxen-anion is, net als dat van andere NSAID's, niet volledig bekend, maar kan in verband worden gebracht met de remming van prostaglandinesynthetase.
Esomeprazol is de "S.-enantiomeer van omeprazol en vermindert maagzuursecretie door een specifiek en gericht werkingsmechanisme Esomeprazol is een zwakke base en wordt geconcentreerd en omgezet in de actieve vorm in de sterk zure omgeving van de secretoire canaliculi van de pariëtale maagcel, waar het remt het " enzym H + K + -ATPase - zuur pompt en remt zowel de basale als de geïnduceerde zuursecretie.
Farmacodynamische effecten
Effect op maagzuursecretie
Een optimaal effect (behoud van een hoge maag-pH) werd verkregen met de VIMOVO-formulering met 20 mg esomeprazol. Na 9 dagen behandeling met VIMOVO tweemaal daags toegediend, werd bij gezonde vrijwilligers een intragastrische pH van meer dan 4 gehandhaafd gedurende een gemiddelde periode van 17,1 uur (SD 3,1). De corresponderende waarde voor NEXIUM 20 mg was 13,6 uur (SD 2,4).
Andere effecten geassocieerd met zuurremming
Tijdens behandeling met antisecretoire geneesmiddelen neemt serumgastrine toe als reactie op verminderde zuursecretie. Chromogranine A (CgA) neemt ook toe door de afname van maagzuur.De toename van de concentratie van CgA kan elk onderzoek naar endocriene tumoren verstoren. Uit literatuurgegevens blijkt dat een protonpompremmer minimaal 5 dagen voor de CgA-meting moet worden gestaakt. Als de CgA- en gastrinespiegels na 5 dagen niet normaliseren, moet de meting 14 dagen na het einde van de behandeling met esomeprazol worden herhaald.
Bij sommige patiënten is tijdens langdurige behandeling met esomeprazol een toename van het aantal enterochromaffine-achtige (ECL) cellen waargenomen, mogelijk geassocieerd met verhoogde serumgastrinespiegels.De resultaten worden als niet klinisch relevant beschouwd.
Tijdens langdurige behandeling met antisecretoire geneesmiddelen werd een toename in de frequentie van optreden van maagkliercysten waargenomen. Deze veranderingen zijn een fysiologisch gevolg van de uitgesproken remming van de zuursecretie, zijn goedaardig en lijken omkeerbaar.
Verminderde maagzuurgraad op welke manier dan ook, inclusief protonpompremmers, verhoogt de maagtellingen van bacteriën die normaal in het maagdarmkanaal aanwezig zijn. Behandeling met protonpompremmers kan leiden tot een licht verhoogd risico op gastro-intestinale infecties Salmonella En Campylobacter en mogelijk ook van Clostridium difficile bij gehospitaliseerde patiënten.
Klinische werkzaamheid en veiligheid
In klinische onderzoeken werd VIMOVO toegediend aan in totaal 491 patiënten gedurende 6 maanden en 135 patiënten gedurende 12 maanden.
In twee gerandomiseerde, dubbelblinde, actief-gecontroleerde onderzoeken was de incidentie van maag- en darmzweren significant lager na behandeling met VIMOVO vergeleken met maagsapresistente naproxen 500 mg tweemaal daags (zonder toediening van esomeprazol of een andere PPI) tijdens een behandeling De deelnemers liepen a priori risico op het ontwikkelen van NSAID-geassocieerde ulcera, vanwege een hoge leeftijd of een voorgeschiedenis van maag- of duodenumulcera. Patiënten die positief testten op: H. pylorize waren uitgesloten van klinische onderzoeken.
De incidentie van maagzweren voor VIMOVO was 5,6% en voor enterisch gecoate naproxen 23,7% (6 maanden gegevens van 2 endoscopische onderzoeken). VIMOVO verminderde ook significant het optreden van relatieve duodenumzweren. enterisch gecoate naproxen (0,7 vs. 5,4 %) (6 maanden gegevens van 2 endoscopische onderzoeken).
Tijdens deze klinische onderzoeken verminderde VIMOVO ook significant het optreden van bepaalde vooraf bepaalde NSAID-geassocieerde bijwerkingen van het bovenste deel van het maagdarmkanaal in vergelijking met enterisch gecoate naproxen (53,3% versus 70,4% (totale gegevens).
In klinische onderzoeken met VIMOVO werden alleen patiënten opgenomen met een risico op het ontwikkelen van NSAID-geassocieerde gastroduodenale ulcera, zoals patiënten ouder dan 50 jaar of met ongecompliceerde eerdere ulcera; Patiënten die gelijktijdig een lage dosis acetylsalicylzuur (ABD) gebruikten, werden ook toegelaten tot het onderzoek. Subgroepanalyses van patiënten bevestigden een trend die vergelijkbaar is met die waargenomen voor de gehele onderzochte populatie met betrekking tot de werkzaamheid bij de preventie van gastro-intestinale ulcera door VIMOVO. Bij ABD-gebruikers was de incidentie van gastroduodenale ulcera 4,0% (95% BI 1,1-10,0). %) in de VIMOVO-groep (n = 99) versus 32,4% (95% BI 23,4-42,3%) in de groep met alleen naproxen EC (n = 102). Bij ouderen ≥ 60 jaar was de incidentie van gastroduodenale ulcera 3,3% (95% BI 1,3-6,7%) in de VIMOVO-groep (n = 212) vergeleken met 30,1% (95% BI 24,0-36,9%) in de naproxen-only groep EC (n = 209).
In twee klinische onderzoeken die 6 maanden duurden, rapporteerde VIMOVO minder gevallen van ongemak in de bovenbuik dan maagsapresistente naproxen, beoordeeld als symptomen van dyspepsie. Een significant kleiner deel van de patiënten die VIMOVO gebruikten stopte voortijdig met onderzoeken vanwege bijwerkingen vergeleken met patiënten die maagsapresistente naproxen gebruikten (respectievelijk 7,9% versus 12,5%), respectievelijk 4,0% en 12,0% van de stopzettingen bijwerkingen die verband houden met het bovenste spijsverteringskanaal, waaronder zweren van de twaalfvingerige darm).
In twee onderzoeken van 12 weken bij patiënten met artrose van de knie, veroorzaakte VIMOVO (500 mg / 20 mg tweemaal daags) een vergelijkbare verbetering van pijn en functie, tijd tot aanvang van de analgetische werkzaamheid en als gevolg van studieonderbrekingen. vergeleken met die waargenomen voor de celecoxib 200 mg eenmaal daags groep.
Pediatrische populatie
Het Europees Geneesmiddelenbureau heeft besloten af te zien van de verplichting om de resultaten van onderzoek met VIMOVO in te dienen.
05.2 "Farmacokinetische eigenschappen
Absorptie
Naproxen
Na toediening van een enkele dosis wordt de tijd tot piekplasmaconcentratie bereikt na 3-5 uur, maar voedselinname leidt tot een verdere vertraging, tot 8 uur of meer.
Bij steady state werden na tweemaal daagse toediening van VIMOVO de piekplasmaconcentraties van naproxen bereikt binnen een mediaan van 3 uur na zowel ochtend- als avonddosering.
Bio-equivalentie tussen VIMOVO en enterisch gecoate naproxen is aangetoond, zowel op basis van de oppervlakte onder de plasmaconcentratie-tijdcurve (AUC) als de maximale plasmaconcentratie (Cmax) van naproxen.
Naproxen wordt snel en volledig geabsorbeerd in het maagdarmkanaal met een biologische beschikbaarheid in vivo 95%.
De steady-state van naproxen wordt binnen 4-5 dagen bereikt.
Esomeprazol
Na tweemaal daagse toediening van VIMOVO wordt esomeprazol snel geabsorbeerd met een piekplasmaconcentratie die wordt bereikt binnen de gemiddelde tijd van 0,5-0,75 uur na de ochtend- en avonddosis, zowel op de eerste dag van toediening als in steady state. Na herhaalde toediening van VIMOVO tweemaal daags was de Cmax 2-3 keer hoger en de AUC 4-5 keer hoger dan op de eerste dag van de behandeling. Dit is waarschijnlijk gedeeltelijk te wijten aan verhoogde absorptie vanwege het "farmacodynamische effect van esomeprazol". met een hogere intragastrische pH, wat leidt tot minder zuurafbraak van esomeprazol in de maag. Verlaagd first-pass metabolisme en systemische klaring van esomeprazol bij herhaalde dosering draagt ook bij tot hogere steady-state plasmaconcentraties (zie Lineariteit/niet-lineariteit).
Hoewel het steady-state AUC-interval vergelijkbaar was voor NEXIUM 20 mg eenmaal daags en VIMOVO tweemaal daags: respectievelijk 292,0 - 2279,0 ng/ml en 189,0 - 2931,0 ng/ml, was de gemiddelde blootstelling groter dan 60% (BI: 1,28 - 1,93 ) voor VIMOVO. Dit is te verwachten vanwege de verschillende totale dosis esomeprazol die wordt toegediend als VIMOVO of als NEXIUM (40 versus 20 mg). Cmax was hoger dan 60% (BI: 1,27 - 2,02) voor VIMOVO, een verwacht resultaat voor een IR-formulering.
Gelijktijdige toediening met voedsel
Toediening van VIMOVO samen met voedsel heeft geen invloed op de hoeveelheid naproxenabsorptie, maar vertraagt de absorptie aanzienlijk met ongeveer 8 uur en verlaagt de piekplasmaconcentratie met ongeveer 12%.
Toediening van VIMOVO samen met voedsel vertraagt de absorptie van esomeprazol niet, maar vermindert de hoeveelheid absorptie aanzienlijk, wat resulteert in verlagingen van respectievelijk 52% en 75% in het gebied onder de plasmaconcentratie-versus-tijdcurve en in de plasmaconcentratie. .
Toediening van VIMOVO 30 minuten voorafgaand aan voedsel heeft slechts minimale of geen effecten op de hoeveelheid en tijd van absorptie van naproxen en heeft geen significant effect op de snelheid of hoeveelheid absorptie van esomeprazol in vergelijking met toediening in nuchtere toestand (zie paragraaf 4.2).
Verdeling
Naproxen
Naproxen heeft een distributievolume van 0,16 l/kg. Op therapeutische niveaus wordt naproxen voor meer dan 99% aan albumine gebonden.Het naproxen-anion is aangetroffen in de melk van vrouwen die borstvoeding geven in concentraties gelijk aan ongeveer 1% van de maximale plasma-naproxenconcentratie (zie rubriek 4.6).
Esomeprazol
Het schijnbare steady-state distributievolume bij gezonde proefpersonen is ongeveer 0,22 l/kg lichaamsgewicht. Esomeprazol heeft een plasma-eiwitbinding van 97%.
Biotransformatie
Naproxen
30% van naproxen wordt in de lever gemetaboliseerd door het cytochroom P450 (CYP)-systeem, voornamelijk door CYP2C9, tot 6-0-desmethylnaproxen. Noch het oorspronkelijke geneesmiddel, noch zijn metabolieten induceren metaboliserende enzymen. Zowel naproxen als 6-0-desmethylnaproxen worden verder gemetaboliseerd tot hun respectievelijke geconjugeerde acylglucuronidemetabolieten.
Esomeprazol
Esomeprazol wordt volledig gemetaboliseerd door het CYP-systeem. Het grootste deel van het metabolisme van esomeprazol hangt af van de CYP2C19-polymorf, die verantwoordelijk is voor de vorming van de hydroxy- en desmethylmetabolieten van esomeprazol. De rest hangt af van een andere specifieke isovorm, CYP3A4, die verantwoordelijk is voor de vorming van esomeprazolsulfon, de belangrijkste plasmametaboliet.De belangrijkste metabolieten van esomeprazol hebben geen effect op de maagzuursecretie.
Eliminatie
Naproxen
Na tweemaal daagse toediening van VIMOVO is de gemiddelde eliminatiehalfwaardetijd van naproxen ongeveer 9 uur en 15 uur na respectievelijk de ochtend- en avonddosis, zonder verandering na herhaalde toediening.
De klaring van naproxen is 0,13 ml/min/kg. Ongeacht de dosis wordt ongeveer 95% van elke dosis naproxen uitgescheiden in de urine, voornamelijk als naproxen (feces. Bij patiënten met nierinsufficiëntie kunnen metabolieten zich ophopen (zie rubriek 4.4).
Esomeprazol
Na tweemaal daagse toediening van VIMOVO is de gemiddelde eliminatiehalfwaardetijd van esomeprazol ongeveer 1 uur na de ochtend- en avonddosis op de eerste dag met een iets langere eliminatiehalfwaardetijd bij steady state (1,2-1,5 uur).
De totale plasmaklaring van esomeprazol is ongeveer 17 l/u na een enkele dosis en ongeveer 9 l/u na herhaalde toediening.
Bijna 80% van een orale dosis esomeprazol wordt uitgescheiden als metabolieten in de urine, de rest in de feces. Minder dan 1% van het oorspronkelijke medicijn wordt teruggevonden in de urine.
Lineariteit / niet-lineariteit
Naproxen
Bij doses naproxen van meer dan 500 mg/dag is er een minder dan proportionele toename van de plasmaspiegels als gevolg van een toename van de klaring veroorzaakt door verzadiging van plasma-eiwitbinding bij hogere doses (minimum gemiddelde Css 36,5, 49,2 en 56,4 mg/l bij dagelijkse doses van naproxen van respectievelijk 500, 1.000 en 1.500 mg).
Esomeprazol
De oppervlakte onder de plasmaconcentratie-tijdcurve van esomeprazol neemt toe bij herhaalde toediening van VIMOVO. Deze toename is dosisafhankelijk en resulteert in een niet-lineaire dosis-AUC-relatie na herhaalde toediening. Deze tijd- en dosisafhankelijkheid is gedeeltelijk te wijten aan een vermindering van het first-pass metabolisme en de systemische klaring, mogelijk als gevolg van een "remming van het CYP2C19-enzym door esomeprazol en/of zijn sulfonmetaboliet. Een verhoogde absorptie van esomeprazol bij herhaalde toediening van VIMOVO heeft waarschijnlijk ook bijgedragen aan tijd- en dosisafhankelijkheid (zie Absorptie) .
Speciale populaties
Nierfalen
De farmacokinetiek van VIMOVO is niet vastgesteld bij patiënten met nierinsufficiëntie.
Naproxen: De farmacokinetiek van naproxen is niet vastgesteld bij personen met nierinsufficiëntie.
Aangezien naproxen, zijn metabolieten en conjugaten voornamelijk door de nieren worden uitgescheiden, bestaat de kans dat naproxenmetabolieten zich ophopen in aanwezigheid van nierinsufficiëntie. De eliminatie van naproxen is verminderd bij patiënten met ernstige nierinsufficiëntie Het gebruik van VIMOVO is gecontra-indiceerd bij patiënten met ernstige nierinsufficiëntie (creatinineklaring
Esomeprazol: Er zijn geen onderzoeken uitgevoerd met esomeprazol bij patiënten met een verminderde nierfunctie. Aangezien de nieren verantwoordelijk zijn voor de uitscheiding van de metabolieten van esomeprazol, maar niet voor de eliminatie van de moederverbinding, wordt geen verandering van het metabolisme van esomeprazol verwacht bij patiënten met een verminderde nierfunctie.
Leverinsufficiëntie
De farmacokinetiek van VIMOVO is niet vastgesteld bij patiënten met een verminderde leverfunctie.
Naproxen: De farmacokinetiek van naproxen is niet vastgesteld bij personen met leverinsufficiëntie.
Chronische alcoholische leverziekte en mogelijk andere vormen van cirrose verlagen ook de totale plasmaconcentratie van naproxen, maar de plasmaconcentratie van vrij naproxen is verhoogd. De implicatie hiervan voor de dosering van de naproxencomponent van VIMOVO is niet bekend, maar het is verstandig om de laagste effectieve dosis te gebruiken.
Esomeprazol: Het metabolisme van esomeprazol bij patiënten met een lichte tot matige leverfunctiestoornis kan verstoord zijn. De snelheid waarmee het geneesmiddel wordt gemetaboliseerd is verminderd bij patiënten met een ernstige leverfunctiestoornis, wat resulteert in een verdubbeling van de oppervlakte onder de plasmaconcentratie-tijdcurve voor esomeprazol.
Patiënten met een ernstige leverfunctiestoornis mogen VIMOVO niet gebruiken (zie rubriek 4.3).
Ouderen
Er zijn geen specifieke gegevens over de farmacokinetiek van VIMOVO bij patiënten ouder dan 65 jaar.
Naproxen: Sommige onderzoeken geven aan dat hoewel de totale plasmaconcentratie van naproxen ongewijzigd is, de vrije plasmafractie van naproxen verhoogd is bij ouderen, maar de vrije fractie is
Esomeprazol: Het metabolisme van esomeprazol is niet significant veranderd bij oudere proefpersonen (in de leeftijd van 71 tot 80 jaar).
Slechte metaboliseerders CYP2C19
Esomeprazol: Ongeveer 3% van de bevolking heeft een gebrek aan functie van het CYP2C19-enzym; deze personen worden trage metaboliseerders genoemd. Bij deze personen wordt het metabolisme van esomeprazol waarschijnlijk voornamelijk gekatalyseerd door CYP3A4. Na herhaalde toediening van 40 mg dagelijkse doses esomeprazol (eenmaal daags) was de gemiddelde oppervlakte onder de plasmaconcentratie-tijdcurve ongeveer 100% hoger bij trage metaboliseerders dan bij personen met CYP2C19-enzymfunctionaliteit (extensieve metaboliseerders).De gemiddelde piekplasmaconcentraties waren ongeveer 60% hoger.
Deze resultaten hebben geen implicaties voor de VIMOVO-dosering.
Seks
Esomeprazol: Na een enkelvoudige dosis van 40 mg esomeprazol is de gemiddelde oppervlakte onder de plasmaconcentratie-tijdcurve ongeveer 30% hoger bij vrouwen dan bij mannen. Er werden geen geslachtsverschillen waargenomen na herhaalde enkelvoudige doses. Deze resultaten hebben geen gevolgen voor de dosering van VIMOVO .
05.3 Gegevens uit het preklinisch veiligheidsonderzoek
Er zijn geen niet-klinische gegevens beschikbaar over de combinatie van werkzame stoffen. Er zijn geen interacties bekend tussen naproxen en esomeprazol die zouden kunnen wijzen op nieuwe of nadelige farmacologische, geneesmiddel/toxicokinetische, toxicologische, chemische/fysische interacties of verdraagbaarheidsproblemen als gevolg van hun combinatie.
Naproxen
Niet-klinische gegevens duiden niet op een speciaal risico voor mensen, gebaseerd op conventionele onderzoeken naar genotoxiciteit, carcinogeen potentieel, embryofoetale toxiciteit en vruchtbaarheid. De belangrijkste bevindingen bij hoge doses in toxiciteitsonderzoeken met herhaalde orale doses bij dieren waren gastro-intestinale irritatie en nierbeschadiging. toe te schrijven aan de remming van de prostaglandinesynthese. Orale toediening van naproxen aan vrouwelijke ratten in het derde trimester van de zwangerschap in peri- en postnatale onderzoeken resulteerde in moeilijke bevallingen. Dit is een bekend effect voor deze categorie medicijnen.
Esomeprazol
Preklinische studies ". Overbrugging". bracht geen speciaal gevaar voor mensen aan het licht op basis van conventionele onderzoeken naar toxiciteit bij herhaalde dosering, genotoxiciteit en reproductietoxiciteit. Carcinogeniteitsonderzoeken bij ratten met het racemische mengsel toonden maag-ECL-celhyperplasie en carcinoïden aan. Deze maageffecten bij ratten zijn het resultaat van hoge en langdurige secundaire hypergastrinemie tot verminderde maagzuurproductie en zijn waargenomen na langdurige behandeling bij ratten met maagzuursecretieremmers.
06.0 FARMACEUTISCHE INFORMATIE
06.1 Hulpstoffen
Kern van de tablet
Croscarmellosenatrium
Magnesium stearaat
Povidon K90
Silica, colloïdaal watervrij
Coating
Carnaubawas
Glycerolmonostearaat 40-55
Hypromellose
IJzeroxide E172 (geel)
Macrogol 8000
Methacrylzuur-ethylacrylaatcopolymeer (1: 1)
Methylparahydroxybenzoaat E218 *
Polydextrose
Polysorbaat 80
Propylparahydroxybenzoaat E216 *
Natriumlaurylsulfaat
Titaandioxide E171
Triethylcitraat
Drukinkt
Hypromellose
IJzeroxide E172 (zwart)
Propyleenglycol
* Deze conserveermiddelen zijn aanwezig in het filmcoatingmengsel en zijn aanwezig in het eindproduct in zeer lage, niet-functionele niveaus.
06.2 Incompatibiliteit
Niet relevant.
06.3 Geldigheidsduur
2 jaar
06.4 Speciale voorzorgsmaatregelen bij bewaren
Niet bewaren boven 30°C.
Fles: Bewaren in de oorspronkelijke verpakking en de fles goed gesloten houden ter bescherming tegen vocht.
Blaren: Bewaren in de oorspronkelijke verpakking ter bescherming tegen vocht.
06.5 Aard van de primaire verpakking en inhoud van de verpakking
HDPE-flessen met silicagel-droogmiddelen met kindveilige of niet-kindveilige polypropyleen sluiting (distributieverpakking) met inductieafdichting. De zak met het droogmiddel mag niet worden ingeslikt.
Verpakkingsgrootten: 6, 20, 30, 60, 100, 180 of 500 tabletten met gereguleerde afgifte.
Aluminium / aluminium blister.
Verpakkingsgrootten: 10, 20, 30, 60 of 100 tabletten met gereguleerde afgifte.
Mogelijk worden niet alle verpakkingsgrootten in de handel gebracht.
06.6 Instructies voor gebruik en verwerking
Geen speciale instructies
07.0 HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
AstraZeneca S.p.A.
Voltapaleis
Via F. Sforza
20080 Basiglio (MI)
08.0 NUMMER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Vimovo "500 mg / 20 mg tabletten met gereguleerde afgifte"
6 tabletten in HDPE-fles - AIC: 040611016
20 tabletten in HDPE-fles - AIC 040611028
30 tabletten in HDPE-fles - AIC: 040611030
60 tabletten in HDPE-fles - AIC: 040611042
100 tabletten in HDPE-fles - AIC: 040611055
180 tabletten in HDPE-fles - AIC: 040611067
500 tabletten in HDPE-fles - AIC: 040611079
10 tabletten in Al / Al Blister - AIC: 040611081
20 tabletten in Al / Al Blister - AIC: 040611093
30 tabletten in Al / Al Blister - AIC: 040611105
60 tabletten in Al / Al Blister - AIC: 040611117
100 tabletten in Al / Al Blister - AIC: 040611129
09.0 DATUM VAN EERSTE VERGUNNING OF VERLENGING VAN DE VERGUNNING
augustus 2011
10.0 DATUM VAN HERZIENING VAN DE TEKST
juni 2014