Wat is Temozolomide Hospira?
Temozolomide Hospira is een geneesmiddel dat de werkzame stof temozolomide bevat. Het is verkrijgbaar in de vorm van capsules (wit en groen: 5 mg; wit en geel: 20 mg; wit en roze: 100 mg; wit en blauw: 140 mg; wit en bruin: 180 mg; wit: 250 mg).
Temozolomide Hospira is een 'generiek geneesmiddel', wat betekent dat Temozolomide Hospira vergelijkbaar is met een 'referentiegeneesmiddel' dat al in de Europese Unie (EU) is toegelaten onder de naam Temodal.
Waarvoor wordt Temozolomide Hospira gebruikt?
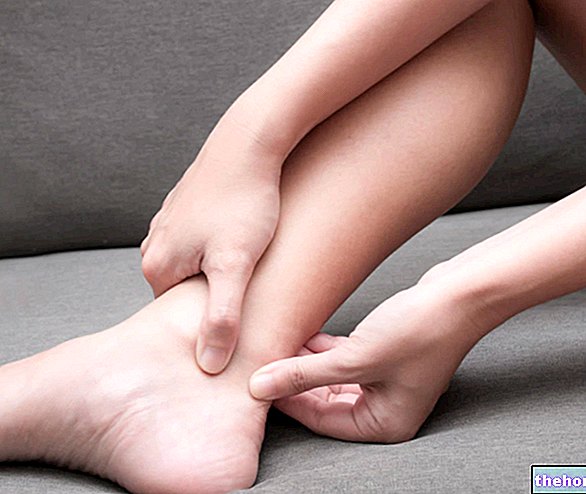
Temozolomide Hospira is een geneesmiddel tegen kanker. Het is geïndiceerd voor de behandeling van kwaadaardige gliomen (hersentumoren) bij de volgende patiëntengroepen:
volwassenen die onlangs gediagnosticeerd zijn met glioblastoma multiforme (een bijzonder agressief type hersentumor). Temozolomide Hospira wordt eerst gebruikt met bestralingstherapie, daarna alleen;
volwassenen en kinderen vanaf drie jaar met een kwaadaardig glioom zoals glioblastoom multiforme of anaplastisch astrocytoom, wanneer de tumor is teruggekomen of erger is geworden na standaardbehandeling. Bij deze patiënten wordt alleen Temozolomide Hospira gebruikt.
Het geneesmiddel is alleen op recept verkrijgbaar.
Hoe wordt Temozolomide Hospira gebruikt?
Behandeling met Temozolomide Hospira moet worden voorgeschreven door een arts die ervaring heeft met de behandeling van hersentumoren.
De dosering van Temozolomide Hospira, eenmaal per dag toegediend, hangt af van het lichaamsoppervlak (berekend aan de hand van de lengte en het gewicht van de patiënt) en varieert van 75 tot 200 mg per vierkante meter eenmaal per dag, afhankelijk van het type kanker dat wordt behandeld, of de patiënt eerder is behandeld, of Temozolomide Hospira alleen of in combinatie met andere therapieën wordt gebruikt, en de reactie van de patiënt op de behandeling. Temozolomide Hospira moet tussen de maaltijden worden toegediend.
Alvorens Temozolomide Hospira te krijgen, kunnen patiënten ook een geneesmiddel nodig hebben dat braken voorkomt. Temozolomide Hospira moet met voorzichtigheid worden gebruikt bij patiënten met ernstige lever- of nierproblemen.
Zie voor volledige informatie de samenvatting van de productkenmerken (ook opgenomen in het EPAR).
Hoe werkt Temozolomide Hospira?
De werkzame stof in Temozolomide Hospira, temozolomide, behoort tot een groep geneesmiddelen tegen kanker die alkylerende middelen worden genoemd. In het lichaam wordt temozolomide omgezet in een andere verbinding genaamd MTIC.MTIC bindt aan het DNA van cellen tijdens de reproductieve fase, waardoor de celdeling wordt geblokkeerd. Als gevolg hiervan kunnen kankercellen zich niet voortplanten en wordt de tumorgroei vertraagd.
Hoe is Temozolomide Hospira onderzocht?
Aangezien Temozolomide Hospira een generiek geneesmiddel is, zijn de onderzoeken beperkt tot bewijs om aan te tonen dat het geneesmiddel biologisch gelijkwaardig is aan het referentiegeneesmiddel, Temodal. Twee geneesmiddelen zijn bio-equivalent als ze dezelfde hoeveelheid van de werkzame stof in het lichaam produceren.
Wat zijn de voordelen en risico's van Temozolomide Hospira?
Omdat Temozolomide Hospira een generiek geneesmiddel is en biologisch gelijkwaardig aan het referentiegeneesmiddel, wordt aangenomen dat de voordelen en risico's van het geneesmiddel hetzelfde zijn als die van het referentiegeneesmiddel.
Waarom is Temozolomide Hospira goedgekeurd?
Het Comité voor geneesmiddelen voor menselijk gebruik (CHMP) heeft geconcludeerd dat op basis van de vereisten van de EU-wetgeving is aangetoond dat Temozolomide Hospira van vergelijkbare kwaliteit is als en biologisch gelijkwaardig aan Temodal. Daarom is het CHMP van mening dat, net als in het geval van Temodal, de voordelen opwegen tegen de vastgestelde risico's. Het Comité heeft daarom aanbevolen een vergunning voor het in de handel brengen van Temozolomide Hospira te verlenen.
Overige informatie over Temozolomide Hospira
Op 15 maart 2010 heeft de Europese Commissie aan Hospira UK Ltd een "Marketing Authorization" voor Temozolomide Hospira verleend, geldig in de hele Europese Unie.
De handelsvergunning is vijf jaar geldig en kan na deze periode worden verlengd.
Voor de volledige versie van de Temozolomide Hospira EPAR, klik hier.
Lees de bijsluiter (meegeleverd in het EPAR) voor meer informatie over de behandeling met Temozolomide Hospira.
De volledige EPAR-versie van het referentiegeneesmiddel is ook te vinden op de website van het Geneesmiddelenbureau.
Laatste update van dit overzicht: 03/2010.
De informatie over Temozolomide Hospira die op deze pagina wordt gepubliceerd, kan verouderd of onvolledig zijn. Zie voor een correct gebruik van deze informatie de pagina Disclaimer en nuttige informatie.























.jpg)