Glycogeen is een macromolecuul (molecuulmassa van ongeveer 400 miljoen dalton) van -glucose waarin voornamelijk α-1,4-glycosidebindingen en vertakkingen in een verhouding van 1:10 voorkomen, vanwege α-1,6-glycosidebindingen.
Glycogeen vormt reservemateriaal en wordt continu afgebroken en gereconstitueerd; in de totale lichaamscelmassa zit ongeveer 100 g glycogeen: het meeste bevindt zich in de lever waar het mobiel is en kan daarom worden gebruikt als reserve voor andere organen (glycogeen in spieren is niet mobiel).
De enzymen die de afbraak en synthese van glycogeen katalyseren, bevinden zich allemaal in het cytoplasma, daarom is er een regulatiesysteem nodig dat het ene pad inactief maakt wanneer het andere actief is: als er glucose beschikbaar is, wordt dit laatste omgezet in glycogeen (anabolisme) dat een reserve, omgekeerd, als c " nodig is voor glucose, wordt het glycogeen afgebroken (katabolisme).

Het enzym dat voornamelijk betrokken is bij de afbraak van glycogeen is de glycogeenfosforylase; dit enzym is in staat om een glycosidische α-1,4-binding te splitsen met behulp van een anorganisch orthofosfaat als lytisch middel: de splitsing vindt plaats op fosforolytische wijze en glucose-1-fosfaat wordt verkregen.
Op vijf of zes eenheden van een vertakkingspunt kan het glycogeenfosforylase-enzym niet langer werken, daarom maakt het zich los van het glycogeen en wordt het vervangen door een deramificerend enzym dat een transferase: op de katalytische plaats van dit enzym c "is een" histidine dat de overdracht van drie saccharide-eenheden naar de dichtstbijzijnde glycosidische keten mogelijk maakt (histidine valt de eerste koolstof van een glucosemolecuul aan). Het zojuist genoemde enzym is de glycosyltransferase; aan het einde van de werking van dit enzym blijft er slechts één glucose-eenheid over op de zijketen, waarbij de eerste koolstof is gebonden aan de zesde koolstof van een glucose in de hoofdketen. De laatste glucose-eenheid in de zijketen wordt vrijgegeven door de werking van "enzym α-1,6 glycosidase (dit enzym vormt het tweede deel van het deramificerende enzym); aangezien de vertakkingen in glycogeen zich in een verhouding van 1:10 bevinden, verkrijgen we uit de volledige afbraak van het macromolecuul ongeveer 90% glucose 1-fosfaat en ongeveer 10% van glucose.
De werking van de bovengenoemde enzymen maakt de eliminatie van een zijketen van het glycogeenmolecuul mogelijk; de activiteit van deze enzymen kan worden herhaald totdat de volledige afbraak van de keten optreedt.
Laten we een hepatocyt beschouwen; glucose (opgenomen via de voeding), wanneer het de cel binnenkomt, wordt het omgezet in glucose-6-fosfaat en wordt het dus geactiveerd. Glucose 6-fosfaat, door de werking van fosfoglucomutase, wordt omgezet in glucose 1-fosfaat: dit laatste is een niet-directe voorloper van biosynthese; bij biosynthese wordt een geactiveerde vorm van suikers gebruikt die wordt voorgesteld door suiker gekoppeld aan een difosfaat: meestal uridyldifosfaat (UDP). vervolgens omgezet in UDP-glucose, deze metaboliet onder invloed van glycogeen synthase die in staat is UDP-glucose te binden aan een niet-reducerend uiteinde van het groeiende glycogeen: er wordt een langwerpig glycogeen van een glucosidische eenheid en UDP verkregen UDP wordt door het nucleosidedifosfokinase-enzym omgezet in UTP dat terugkeert naar de circulatie.
De afbraak van glycogeen vindt plaats door de werking van glycogeenfosforylase die een glucosemolecuul afgeeft en omzet in glucose 1-fosfaat. Vervolgens zet fosfoglucomutase glucose 1-fosfaat om in glucose 6-fosfaat.
Glycogeen wordt vooral in de lever en spieren gesynthetiseerd: in het organisme is 1-1,2 hectogram glycogeen verdeeld over de spiermassa.
Het glycogeen van een myocyt vertegenwoordigt alleen een energiereserve voor deze cel, terwijl het glycogeen in de lever ook een reserve is voor andere weefsels, dat wil zeggen dat het als glucose naar andere cellen kan worden gestuurd.
Het glucose-6-fosfaat dat in de spieren wordt verkregen door de afbraak van glycogeen wordt vervolgens, bij energiebehoefte, naar de glycolyse gestuurd; in de lever wordt glucose-6-fosfaat omgezet in glucose door de werking van glucose-6-fosfaatfosfatase (karakteristiek enzym van hepatocyten) en wordt in de bloedbaan getransporteerd.
Glycogeensynthase en glycogeenfosforylase werken beide op de niet-reducerende eenheden van glycogeen, dus er moet een hormonaal signaal zijn dat de activering van de ene route en de blokkering van de andere regelt (of vice versa).
In het laboratorium was het mogelijk om de glycogeenketen te verlengen door gebruik te maken van glycogeenfosforylase en glucose 1-fosfaat in een zeer hoge concentratie te gebruiken.
In cellen katalyseert glycogeenfosforylase alleen de afbraakreactie omdat de concentraties van de metabolieten zodanig zijn dat het evenwicht van de volgende reactie naar rechts verschuift (dwz naar de afbraak van glycogeen):

Laten we eens kijken naar het werkingsmechanisme van het glycogeenfosforylase: de acetaalzuurstof (die fungeert als een brug tussen de glucose-eenheden) bindt zich aan de waterstof van de fosforyl: een reactietussenproduct wordt gevormd door een carbokation (op de glucose die alles is " extremiteiten) waaraan fosforyl (Pi) zeer snel bindt.
Glycogeenfosforylase vereist een cofactor die pyridoxaalfosfaat is (dit molecuul is ook een cofactor voor transaminasen): het heeft een gedeeltelijk geprotoneerde fosforyl (pyridoxaalfosfaat is omgeven door een hydrofobe omgeving die de aanwezigheid van protonen die eraan gebonden zijn rechtvaardigt). De fosforyl (Pi) is in staat een proton over te dragen aan het glycogeen omdat deze fosforyl dan het proton terugkrijgt uit het gedeeltelijk geprotoneerde fosforyl van het pyridoxaalfosfaat. De kans dat de fosforyl bij fysiologische pH zijn proton verliest en volledig gedeprotoneerd blijft, is zeer laag.
Laten we nu kijken hoe fosfoglucomutase werkt. Dit enzym presenteert op de katalytische plaats een residu van gefosforyleerd serine; serine levert fosforyl op tot glucose 1-fosfaat (op positie zes): glucose 1,6-bisfosfaat wordt gedurende een korte tijd gevormd, vervolgens wordt serine opnieuw gefosforyleerd waarbij de fosforyl op positie één komt. Fosfogluco-mutase kan in beide richtingen werken, namelijk glucose 1-fosfaat omzetten in glucose 6-fosfaat of omgekeerd; als glucose-6-fosfaat wordt geproduceerd, kan het direct naar de glycolyse worden gestuurd, in de spieren, of worden omgezet in glucose in de lever.
het enzym uridylfosfoglucotransferase (of UDP-glucosepyrofosforylase) katalyseert de glucose 1-fosfaatoverdrachtsreactie naar UTP door hechting aan fosforyl a.
Het zojuist beschreven enzym is een pyrofosforylase: deze naam is te danken aan het feit dat de tegengestelde reactie van de zojuist beschreven reactie een pyrofosforylering is.
UDP-glucose, verkregen zoals beschreven, kan de glycogeenketen verlengen met een monosacharide-eenheid.
Het is mogelijk om de reactie te laten evolueren naar de vorming van UDP-glucose door een product dat pyrofosfaat is te elimineren; het enzym pyrofosfatase zet pyrofosfaat om in twee moleculen orthofosfaat (hydrolyse van een anhydride) en houdt daarbij de concentratie pyrofosfaat zo laag dat het proces van vorming van UDP-glucose thermodynamisch wordt bevorderd.
Zoals vermeld, kan UDP-glucose, dankzij de werking van glycogeensynthase, de glycogeenketen verlengen.
De vertakkingen (in een verhouding van 1:10) zijn te wijten aan het feit dat, wanneer een glycogeenketen uit 20-25 eenheden bestaat, een vertakkend enzym (met een "histidine op zijn katalytische plaats) ingrijpt, in staat om een reeks van 7 -8 glycosidische eenheden verder stroomafwaarts van 5-6 eenheden: zo ontstaat een nieuwe vertakking.
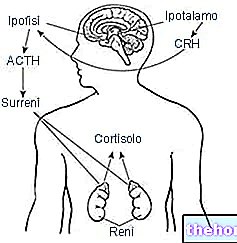
Om redenen van nerveuze oorsprong of als er energie nodig is door lichamelijke inspanning, wordt adrenaline door de bijnieren uitgescheiden.
De doelcellen van adrenaline (en noradrenaline) zijn die van de lever, spieren en vetweefsel (in het laatste is er de afbraak van triglyceriden en de circulatie van vetzuren: bijgevolg wordt glucose geproduceerd in de mitochondria 6-fosfaat, naar de glycolyse gestuurd, terwijl in adipocyten glucose-6-fosfaat wordt omgezet in glucose door de werking van het enzym glucose-6-fosfaatfosfatase en naar de weefsels wordt geëxporteerd).
Laten we eens kijken, nu de modaliteiten van actie van adrenaline. Adrenaline bindt zich aan een receptor op het celmembraan (van myocyten en hepatocyten) en deze bepaalt de translatie van het signaal van buiten naar binnen in de cel. Het proteïne kinase wordt geactiveerd dat gelijktijdig inwerkt op de systemen die de synthese en afbraak van glycogeen reguleren:
Glycogeensynthase bestaat in twee vormen: een gedefosforyleerde (actieve) vorm en een gefosforyleerde (inactieve) vorm; eiwitkinase fosforyleert glycogeensynthase en blokkeert de werking ervan.
Glycogeenfosforylase kan in twee vormen voorkomen: een actieve vorm waarin een gefosforyleerde serine aanwezig is en een inactieve vorm waarin serine is gedefosforyleerd. Glycogeenfosforylase kan worden geactiveerd door het enzym glycogeen fosforylase kinase. Glycogeenfosforylasekinase is actief als het gefosforyleerd is en inactief als het gedefosforyleerd is; het eiwitkinase heeft als substraat het glycogeenfosforylasekinase, d.w.z. het is in staat dit laatste te fosforyleren (en dus te activeren), wat op zijn beurt het glycogeenfosforylase activeert.
Zodra het adrenalinesignaal voorbij is, moet ook het effect dat het op de cel heeft ophouden: fosfatase-enzymen grijpen dan in op de eiwitsoort.