INLEIDING: Gewrichtskraakbeen is een zeer gespecialiseerd bindweefsel dat bestaat uit cellen die chondrocyten worden genoemd en het omliggende ondersteunende weefsel, de matrix. Het heeft een parelwitte kleur en bedekt de uiteinden van de gewrichtsbotten en beschermt ze tegen wrijving.Zijn functie is vergelijkbaar met die van een schokdemper, die in staat is om normale gewrichtsrelaties te beschermen en beweging mogelijk te maken.
Door de volledige afwezigheid van vascularisatie en innervatie vertoont het kraakbeen een slecht regeneratief vermogen bij letsel, vooral als het ernstig is. Zelfs wanneer dit regenereert, geeft het nog steeds aanleiding tot weefsel van het type fibrokraakbeen, minder resistent en elastisch dan het origineel; het kan daarom de functionaliteit van het gewricht aantasten en het ontstaan van degeneratieve verschijnselen in de loop van de tijd (artrose of osteoartritis) bevorderen.
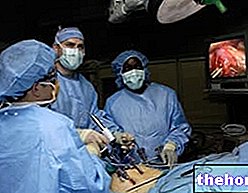
Kraakbeenletsels zijn een veel voorkomend probleem, gemakkelijk te vinden bij ouderen (degeneratieve artrose), maar soms ook bij jongeren, waar vaker schade van traumatische oorsprong optreedt met een hoog risico op evolutie naar artritische vormen. mogelijkheden behandelingen waren beperkt en de patiënt was veroordeeld tot invaliditeit of, waar mogelijk, het gewricht te vervangen door een gewrichtsprothese. Tegenwoordig bieden moderne chirurgische technieken die verband houden met tissue engineering wat meer hoop.
Het is mogelijk om het beenmerg te stimuleren om herstellend fibrokraakbeenweefsel te vormen, waarbij meerdere kleine gaatjes worden gemaakt (perforatie), microfracturen veroorzaken of het oppervlak van het subchondrale bot (benig gedeelte onder het kraakbeen) wordt gevijld; zoals enkele regels geleden vermeld, is het gevormde herstelweefsel van het fibrokraakbeenachtige type (van serie B) en heeft als zodanig een veel lagere functionaliteit dan het kraakbeen dat door moeder natuur wordt geleverd. Om deze reden zijn deze technieken momenteel geïndiceerd bij de behandeling van ondiepe en bescheiden chondrale laesies.
Bij uitgebreidere laesies is het mogelijk om te kiezen voor een kraakbeentransplantatie.
De kraakbeentransplantatie
Het is goed om allereerst te verduidelijken dat deze term niet verwijst naar één, maar naar drie verschillende chirurgische technieken.
→ Perichondrium- of periosteumimplantaten (dunne membranen die respectievelijk het kraakbeen bedekken, behalve de gewrichtsdelen, en de botten, behalve de gewrichtsvlakken en de inbrengpunten van de pezen). De chirurg neemt flappen van deze weefsels en brengt ze in het geblesseerde gebied in, waar ze de groei van een weefsel veroorzaken dat lijkt op kraakbeen of fibrokraakbeen.
INDICATIES: De langetermijnresultaten zijn tegenstrijdig; om deze reden is het geen wijdverbreide techniek.
→ Mozaïekplastiek of osteochondraal transplantaat: omvat het gebruik van cilinders van osteochondraal weefsel (dwz botdelen met het bovenliggende kraakbeen) die uit het gewonde gewricht van dezelfde patiënt worden genomen en onder druk worden getransplanteerd in het kraakbeendefect.
INDICATIES: deze kraakbeentransplantatie kan arthroscopisch worden uitgevoerd, is daarom minimaal invasief en veroorzaakt geen afstotings- en infectieproblemen. Het wordt uitgevoerd op hetzelfde chirurgische tijdstip en is alleen geïndiceerd voor kleine laesies, terwijl de diepte geen beperkende factor is; om voor de hand liggende redenen is het osteochondrale materiaal dat nodig is voor het transplantaat in feite beperkt en hogere monsters zouden aanzienlijke schade aan de donorplaats veroorzaken. De kraakbeentransplantatie is daarom het resultaat van een compromis: een "kritisch gebied voor de functionaliteit van het gewricht" is " gerepareerd" het kraakbeen uit een minder belangrijk gebied halen, maar daarvoor niet nutteloos of overbodig.
Kraakbeentransplantatie kan niet worden uitgevoerd voor inoperabele gewrichten, zoals die in de vingers, voet of wervelkolom; het is in plaats daarvan geïndiceerd voor de knie, enkel, schouder en heup.
→ Autologe chondrocytentransplantatie: kraakbeencellen worden bij de patiënt geoogst door een klein plakje kraakbeen te verwijderen in een niet-ladende ruimte. Door middel van biotechnologische technieken worden de verzamelde chondrocyten geïsoleerd en gedurende 2-4 weken in het laboratorium gekweekt, waarbij ze differentiëren door hun aantal te vermenigvuldigen. Op dit punt ondergaat de patiënt een nieuwe operatie, waarbij de laesie wordt schoongemaakt en bedekt met het periost, waardoor een klein gaatje overblijft waardoor de gekweekte cellen vervolgens worden geïnjecteerd. De periostale flap, genomen van het antero-mediale oppervlak van de ipsilaterale tibia, is verantwoordelijk voor eventuele complicaties die zich binnen korte tijd kunnen voordoen; bovendien vereist het een vrij complexe chirurgische techniek, die niet artroscopisch kan worden uitgevoerd. Om deze problemen te overwinnen, kunnen autologe chondrocytimplantaten worden gebruikt op hyaluronzuurondersteuning van biotechnologische oorsprong, die ook het voordeel hebben dat ze een minder invasieve chirurgische techniek vereisen. Het onderzoek is momenteel gericht op de identificatie van nieuwe biotechnologische dragers die de enting en proliferatie van getransplanteerde chondrocytenculturen kunnen bevorderen, volgens de kenmerken van het "natuurlijke" gewrichtskraakbeen.
Ook in dit geval, aangezien de patiënt tegelijkertijd donor en ontvanger is, zijn er geen problemen met afstoting of infectie. In tegenstelling tot de vorige techniek is de beperkende factor niet zozeer de omvang van de laesie, maar de diepte ervan: als de schade zich uitbreidt tot het onderliggende bot (ernstige verwondingen, osteochondritis, vergevorderde artrose) wortelt het implantaat moeilijk omdat het geen Daarom wordt gezocht naar biotechnologische materialen die als een geschikte drager fungeren, om de verspreiding van de chondrocyten in de omgeving te vermijden en hun groei te bevorderen, zelfs in aanwezigheid van momenteel onbehandelbare pathologieën.
OPMERKINGEN: zowel behandelingen op basis van perforaties, schaafwonden en microfracturen als behandelingen met kraakbeentransplantatie zijn geïndiceerd voor patiënten onder de 40-50 jaar, aangezien veroudering de proliferatieve capaciteit van het kraakbeen vermindert tot nul. Geen van de technieken vermeld in dit artikel is geldig voor gevorderde artrose.