Actieve ingrediënten: Silodosine
Urorec 8 mg harde capsules
Urorec 4 mg harde capsules
Indicaties Waarom wordt Urorec gebruikt? Waar is het voor?
Wat is Urorec
Urorec behoort tot een groep geneesmiddelen die alfa1A-adrenoceptorremmers worden genoemd Urorec is selectief voor receptoren in de prostaat, blaas en urethra Door deze receptoren te blokkeren, ontspant het geneesmiddel de gladde spieren in deze weefsels, vergemakkelijkt het urineren en verlicht de symptomen .
Waar is Urorec voor?
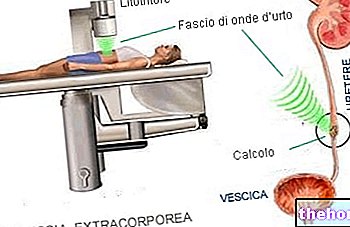
Urorec wordt gebruikt bij volwassen mannen voor de behandeling van urinewegsymptomen die gepaard gaan met een goedaardige vergroting van de prostaat (prostaathyperplasie), zoals:
- moeite met plassen,
- het gevoel hebben dat u uw blaas niet volledig hebt geleegd,
- frequente behoefte om te plassen, zelfs 's nachts.
Contra-indicaties Wanneer Urorec niet mag worden gebruikt
Neem Urorec niet in
als u allergisch bent voor silodosine of voor één van de andere bestanddelen van dit geneesmiddel (vermeld in rubriek 6).
Voorzorgen bij gebruik Wat u moet weten voordat u Urorec inneemt
Neem contact op met uw arts of apotheker voordat u Urorec® inneemt
- Als u een oogoperatie ondergaat vanwege vertroebeling van de kristallijne (staaroperatie), is het belangrijk dat u uw oogarts onmiddellijk informeert dat u Urorec gebruikt of in het verleden heeft gebruikt. Dit komt omdat sommige patiënten die met dit type geneesmiddel werden behandeld, tijdens deze procedure een verlies van spierspanning in de iris (het gekleurde ronde deel van het oog) hebben ervaren. De oogarts zal passende voorzorgsmaatregelen nemen met betrekking tot de medicijnen en chirurgische technieken die zullen worden gebruikt.Vraag uw arts of het nodig is om de behandeling met Urorec uit te stellen of tijdelijk te stoppen in geval van een cataractoperatie.
- Als u in het verleden bent flauwgevallen of u zich duizelig voelde toen u plotseling opstond, vertel dit dan aan uw arts voordat u Urorec inneemt.Als u Urorec inneemt, kunt u duizelig worden bij het opstaan en af en toe flauwvallen, vooral aan het begin van de behandeling of als u Urorec inneemt. die de bloeddruk verlagen Ga in dit geval onmiddellijk zitten of liggen totdat uw symptomen verdwijnen en vertel het uw arts zo snel mogelijk (zie ook rubriek "Rijvaardigheid en het gebruik van machines").
- Als u ernstige leverproblemen heeft, mag u Urorec niet gebruiken, aangezien het geneesmiddel niet is onderzocht bij patiënten met deze aandoeningen.
- Als u nierproblemen heeft, vraag dan uw arts om advies. Als u matige nierproblemen heeft, zal uw arts voorzichtig beginnen met de behandeling met Urorec en mogelijk met een lagere dosis (zie rubriek 3 "Dosis"). Als u een ernstige nierziekte heeft, moet u mag Urorec niet gebruiken.
- Aangezien een goedaardige vergroting van de prostaat en prostaatkanker dezelfde symptomen kunnen hebben, zal uw arts controleren of u geen prostaatkanker heeft voordat de behandeling met Urorec wordt gestart. Urorec is geen behandeling voor prostaatkanker.
- Behandeling met Urorec kan leiden tot abnormale ejaculatie (vermindering van de hoeveelheid sperma die vrijkomt tijdens geslachtsgemeenschap), wat de mannelijke vruchtbaarheid tijdelijk kan verminderen. Dit effect verdwijnt na stopzetting van de behandeling met Urorec. Vertel het uw arts als u kinderen wilt.
Kinderen en adolescenten
Geef dit geneesmiddel niet aan kinderen en jongeren tot 18 jaar, aangezien er geen indicatie is voor deze leeftijdsgroep.
Interacties Welke medicijnen of voedingsmiddelen kunnen het effect van Urorec . veranderen
Vertel het uw arts of apotheker als u andere geneesmiddelen gebruikt, kort geleden heeft gebruikt of in de nabije toekomst gaat gebruiken.
Vertel het uw arts in het bijzonder als u:
- geneesmiddelen die de bloeddruk verlagen (vooral geneesmiddelen die alfa1-blokkers worden genoemd, zoals prazosine of doxazosine), omdat er een mogelijk risico bestaat dat het effect van deze geneesmiddelen wordt versterkt tijdens de behandeling met Urorec.
- antischimmelmiddelen (zoals ketoconazol of itraconazol), geneesmiddelen die worden gebruikt om de hiv/aids-infectie onder controle te houden (zoals ritonavir) of geneesmiddelen die na transplantatie worden gebruikt om orgaanafstoting te voorkomen (zoals ciclosporine), omdat deze geneesmiddelen de concentratie van Urorec in het bloed kunnen verhogen .
- geneesmiddelen die worden gebruikt als u problemen heeft met het krijgen of behouden van een erectie (zoals sildenafil of tadalafil), omdat gelijktijdig gebruik met Urorec uw bloeddruk enigszins kan verlagen.
- geneesmiddelen tegen epilepsie of rifampicine (een geneesmiddel dat wordt gebruikt om tuberculose te behandelen), omdat het effect van Urorec kan worden verminderd.
Waarschuwingen Het is belangrijk om te weten dat:
Rijvaardigheid en het gebruik van machines
Rijd niet en bedien geen machines als u zich zwak, duizelig of slaperig voelt of wazig ziet.
Dosis, wijze en tijdstip van toediening Hoe Urorec te gebruiken: Dosering
Gebruik dit geneesmiddel altijd precies zoals uw arts of apotheker u dat heeft verteld. Raadpleeg bij twijfel uw arts of apotheker.
De aanbevolen dosering is één Urorec 8 mg capsule per dag oraal.
Neem de capsule altijd bij een maaltijd in, bij voorkeur elke dag op hetzelfde tijdstip. De capsule niet fijnmaken of kauwen, maar in zijn geheel doorslikken, bij voorkeur met een glas water.
Patiënten met nierproblemen
Als u matige nierproblemen heeft, kan uw arts u een andere dosis voorschrijven. Voor deze gevallen zijn Urorec 4 mg harde capsules beschikbaar.
Overdosering Wat moet u doen als u te veel Urorec heeft ingenomen?
Wat u moet doen als u meer van Urorec heeft ingenomen dan u zou mogen
Vertel het uw arts zo snel mogelijk als u meer dan één capsule heeft ingenomen. Als u zich duizelig of flauw voelt, vertel dit dan onmiddellijk aan uw arts.
Wat u moet doen wanneer u bent vergeten Urorec in te nemen
Als u eerder bent vergeten een capsule in te nemen, kunt u deze later op dezelfde dag innemen. Als het bijna tijd is voor uw volgende dosis, sla dan de vergeten dosis over en neem geen dubbele dosis om een vergeten capsule in te halen.
Als u stopt met het innemen van Urorec
Als u stopt met de behandeling, kunnen uw symptomen terugkeren.
Als u nog vragen heeft over het gebruik van dit geneesmiddel, neem dan contact op met uw arts of apotheker.
Bijwerkingen Wat zijn de bijwerkingen van Urorec
Zoals elk geneesmiddel kan ook dit geneesmiddel bijwerkingen hebben, al krijgt niet iedereen daarmee te maken.
Neem onmiddellijk contact op met uw arts als u een van de volgende allergische reacties bemerkt: zwelling van het gezicht of de keel, ademhalingsmoeilijkheden, flauwvallen, jeukende huid of netelroos, aangezien de gevolgen ernstig kunnen worden.
De meest voorkomende bijwerking is een vermindering van de hoeveelheid sperma die vrijkomt tijdens geslachtsgemeenschap. Dit effect verdwijnt na het stoppen van de behandeling met Urorec Vertel het uw arts als u kinderen wilt.
Duizeligheid kan optreden, ook bij het opstaan en soms flauwvallen. Als u zich flauw of duizelig voelt, ga dan onmiddellijk zitten of liggen totdat de symptomen verdwijnen. Als u zich duizelig voelt bij het opstaan of als u flauwvalt, vertel dit dan zo snel mogelijk aan uw arts.
Urorec kan complicaties veroorzaken tijdens cataractchirurgie (operatie aan het oog die wordt uitgevoerd om de vertroebeling van de lens te verhelpen, zie rubriek "Waarschuwingen en voorzorgen") Het is belangrijk dat u uw oogarts onmiddellijk op de hoogte brengt als u Urorec gebruikt of eerder heeft gebruikt .
Mogelijke bijwerkingen worden hieronder vermeld:
Zeer vaak voorkomende bijwerkingen (kunnen voorkomen bij meer dan 1 op de 10 mensen)
- Abnormale ejaculatie (vermindering of afwezigheid van sperma-emissie tijdens geslachtsgemeenschap, zie rubriek "Waarschuwingen en voorzorgen")
Vaak voorkomende bijwerkingen (kunnen voorkomen bij maximaal 1 op de 10 mensen)
- Duizeligheid, ook bij opstaan (zie ook eerder in deze paragraaf)
- Loopneus of verstopte neus
- Diarree
Soms voorkomende bijwerkingen (kunnen voorkomen bij maximaal 1 op de 100 mensen)
- Verminderd seksueel verlangen
- Misselijkheid
- Droge mond
- Moeite met het krijgen of behouden van een erectie
- Versnelde hartslag
- Symptomen van een allergische huidreactie, zoals uitslag, jeuk, netelroos en door geneesmiddelen veroorzaakte uitslag
- Abnormale leverfunctietesten
- Lage bloeddruk
Zelden voorkomende bijwerkingen (kunnen voorkomen bij maximaal 1 op de 1.000 mensen)
- Snelle of onregelmatige hartslag (hartkloppingen genoemd)
- Flauwvallen / bewustzijnsverlies
Zeer zelden voorkomende bijwerkingen (kunnen voorkomen bij maximaal 1 op de 10.000 mensen)
- Andere allergische reacties met zwelling van het gezicht of de keel
Niet bekend (frequentie kan met de beschikbare gegevens niet worden bepaald)
- Markeer pupil tijdens staaroperatie (zie ook eerder in deze paragraaf)
Als u denkt dat er enig effect is op uw seksleven, vertel dit dan aan uw arts.
Melding van bijwerkingen
Krijgt u last van bijwerkingen, neem dan contact op met uw arts of apotheker.Dit geldt ook voor mogelijke bijwerkingen die niet in deze bijsluiter staan. U kunt bijwerkingen ook rechtstreeks melden via het nationale meldsysteem zoals vermeld in aanhangsel V. Door bijwerkingen te melden, kunt u ons helpen meer informatie te verkrijgen over de veiligheid van dit geneesmiddel.
Vervaldatum en retentie
Buiten het zicht en bereik van kinderen houden.
Gebruik dit geneesmiddel niet meer na de uiterste houdbaarheidsdatum. Die is te vinden op de doos en blister na EXP/EXP. De vervaldatum verwijst naar de laatste dag van die maand.
Niet bewaren boven 30°C.
Bewaren in de oorspronkelijke verpakking ter bescherming tegen licht en vocht.
Gebruik dit geneesmiddel niet als u merkt dat de verpakking beschadigd is of als er tekenen van knoeien zijn.
Gooi geneesmiddelen niet weg via het afvalwater of met het huisvuil.Vraag uw apotheker wat u met geneesmiddelen moet doen die u niet meer gebruikt.Dit helpt het milieu te beschermen.
Samenstelling en farmaceutische vorm
Wat bevat Urorec
Urorec 8 mg
Het actieve ingrediënt is silodosine. Elke capsule bevat 8 mg silodosine.
De andere stoffen in dit middel zijn gepregelatineerd maïszetmeel, mannitol (E421), magnesiumstearaat, natriumlaurylsulfaat, gelatine, titaandioxide (E171).
Urorec 4 mg
Het actieve ingrediënt is silodosine. Elke capsule bevat 4 mg silodosine.
De andere stoffen in dit middel zijn gepregelatineerd maïszetmeel, mannitol (E421), magnesiumstearaat, natriumlaurylsulfaat, gelatine, titaniumdioxide (E171), geel ijzeroxide (E172).
Hoe ziet Urorec eruit en hoeveel zit er in een verpakking?
Urorec 8 mg zijn witte, ondoorzichtige, harde gelatinecapsules.
Urorec 4 mg zijn gele ondoorzichtige harde gelatinecapsules.
Urorec is verkrijgbaar in verpakkingen van 5, 10, 20, 30, 50, 90, 100 capsules. Mogelijk worden niet alle verpakkingsgrootten in de handel gebracht.
Bron Bijsluiter: AIFA (Italiaans Geneesmiddelenbureau). Inhoud gepubliceerd in januari 2016. De aanwezige informatie is mogelijk niet up-to-date.
Om toegang te hebben tot de meest actuele versie, is het raadzaam om de website van AIFA (Italian Medicines Agency) te bezoeken. Disclaimer en nuttige informatie.
01.0 NAAM VAN HET GENEESMIDDEL
UROREC 4 MG HARDE CAPSULES
02.0 KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
Elke harde capsule bevat 4 mg silodosine.
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1.
03.0 FARMACEUTISCHE VORM
Harde capsule.
Harde gelatinecapsule, geel, ondoorzichtig, maat 3.
04.0 KLINISCHE INFORMATIE
04.1 Therapeutische indicaties
Behandeling van de tekenen en symptomen van goedaardige prostaathyperplasie (BPH) bij volwassen mannen.
04.2 Dosering en wijze van toediening
Dosering
De aanbevolen dosering is één Urorec 8 mg capsule per dag. Voor speciale patiëntenpopulaties wordt één Urorec 4 mg capsule per dag aanbevolen (zie hieronder).
Bejaarden
Bij ouderen is geen dosisaanpassing nodig (zie rubriek 5.2).
Nierfunctiestoornis
Bij patiënten met een lichte nierfunctiestoornis (CLCR ≥50 tot ≤80 ml/min) is geen dosisaanpassing vereist.
Bij patiënten met een matige nierfunctiestoornis (CLCR ≥30 tot
leverfunctiestoornis
Bij patiënten met een lichte tot matige leverfunctiestoornis is geen dosisaanpassing nodig.
Gebruik bij patiënten met een ernstige leverfunctiestoornis wordt niet aanbevolen omdat er geen gegevens beschikbaar zijn (zie rubrieken 4.4 en 5.2).
Pediatrische populatie
Er is geen indicatie voor een specifiek gebruik van Urorec bij pediatrische patiënten voor de goedgekeurde indicatie.
Wijze van toediening
Oraal gebruik.
De capsule moet elke dag met voedsel worden ingenomen, bij voorkeur op hetzelfde tijdstip. De capsule mag niet worden fijngemaakt of gekauwd, maar moet in zijn geheel worden doorgeslikt, bij voorkeur met een glas water.
04.3 Contra-indicaties
Overgevoeligheid voor de werkzame stof of voor één van de in rubriek 6.1 vermelde hulpstoffen.
04.4 Bijzondere waarschuwingen en passende voorzorgen bij gebruik
Intraoperatief Floppy Iris Syndroom (Intraoperatief Floppy Iris-syndroom, IFIS)
IFIS (een variant van het kleine-pupilsyndroom) is waargenomen tijdens cataractchirurgie bij sommige patiënten die werden behandeld met 1-blokkers of eerder waren behandeld met α1-blokkers.Deze omstandigheid kan de procedurele complicaties tijdens de operatie vergroten.
Het starten van een behandeling met silodosine bij patiënten die wachten op een cataractoperatie wordt niet aanbevolen. Stopzetting van de behandeling met α1-blokkers 1-2 weken voorafgaand aan cataractchirurgie is aanbevolen, maar de voordelen en duur van het staken van de behandeling voorafgaand aan cataractchirurgie zijn nog niet vastgesteld.
Tijdens de preoperatieve evaluatie moeten oogchirurgen en het hele team overwegen of patiënten die op een cataractoperatie wachten, worden behandeld of zijn behandeld met silodosine, om ervoor te zorgen dat er passende maatregelen beschikbaar zijn om IFIS tijdens "interventie" aan te pakken.
Orthostatische effecten
De incidentie van orthostatische effecten met silodosine is erg laag. Bij individuele patiënten kan echter een verlaging van de bloeddruk optreden, wat zelden syncope kan veroorzaken. Bij de eerste symptomen van orthostatische hypotensie (zoals houdingsduizeligheid) moet de patiënt gaan zitten of liggen tot de symptomen verdwijnen Bij patiënten met orthostatische hypotensie wordt behandeling met silodosine niet aanbevolen.
Nierfunctiestoornis
Het gebruik van silodosine bij patiënten met een ernstige nierfunctiestoornis (CLCR
leverfunctiestoornis
Aangezien er geen gegevens beschikbaar zijn, wordt het gebruik van silodosine niet aanbevolen bij patiënten met een ernstige leverfunctiestoornis (zie rubrieken 4.2 en 5.2).
Prostaatkanker
Aangezien BPH en prostaatkanker dezelfde symptomen kunnen hebben en naast elkaar kunnen bestaan, moeten patiënten waarvan wordt aangenomen dat ze BPH hebben, worden geëvalueerd voordat de behandeling met silodosine wordt gestart om de aanwezigheid van prostaatkanker uit te sluiten, vervolgens met regelmatige tussenpozen digitaal rectaal onderzoek en, indien nodig, prostaatkanker specifieke antigeen (PSA) meting moet worden uitgevoerd.
Behandeling met silodosine resulteert in verminderde of geen ejaculatie tijdens het orgasme, wat de mannelijke vruchtbaarheid tijdelijk kan verminderen. Het effect verdwijnt na stopzetting van de behandeling met silodosine (zie rubriek 4.8).
04.5 Interacties met andere geneesmiddelen en andere vormen van interactie
Silodosine wordt uitgebreid gemetaboliseerd, voornamelijk via CYP3A4, alcoholdehydrogenase en UGT2B7. Silodosine is ook een substraat van P-glycoproteïne Stoffen die deze enzymen en transporters remmen (zoals ketoconazol, itraconazol, ritonavir of ciclosporine) of induceren (zoals rifampicine, barbituraten, carbamazepine, fenytoïne) kunnen de plasmaconcentraties van silodosine en zijn metaboliet actief.
Alfablokkers
Er is onvoldoende informatie over de veiligheid van het gebruik van silodosine in combinatie met andere -adrenoceptorantagonisten, daarom wordt gelijktijdig gebruik van andere α-adrenoceptorantagonisten niet aanbevolen.
CYP3A4-remmers
In een interactieonderzoek werd een 3,7-voudige toename van de maximale plasmaconcentratie van silodosine en een 3,1-voudige toename van de blootstelling aan silodosine (dwz AUC) waargenomen bij gelijktijdige toediening van een krachtige remmer van silodosine, CYP3A4 (ketoconazol 400 mg). Gelijktijdig gebruik van krachtige CYP3A4-remmers (zoals ketoconazol, itraconazol, ritonavir of ciclosporine) wordt niet aanbevolen.
Wanneer silodosine gelijktijdig werd toegediend met een matig krachtige CYP3A4-remmer zoals diltiazem, werd een toename van de silodosine-AUC van ongeveer 30% waargenomen, terwijl de Cmax en de halfwaardetijd niet werden beïnvloed. Deze wijziging is niet klinisch relevant en er is geen dosisaanpassing nodig.
PDE-5-remmers
Er zijn minimale farmacodynamische interacties waargenomen tussen silodosine en maximale doses sildenafil of tadalafil. In een placebogecontroleerd onderzoek bij 24 proefpersonen in de leeftijd van 45 tot 78 jaar die werden behandeld met silodosine, veroorzaakte gelijktijdige toediening van sildenafil 100 mg of tadalafil 20 mg geen klinisch significante gemiddelde verlagingen van de systolische of diastolische bloeddruk, zoals aangetoond uit de orthostatische test ( staand versus rugligging). Bij personen ouder dan 65 jaar varieerde de gemiddelde afname op verschillende tijdstippen van 5 tot 15 mmHg (systolische bloeddruk) en van 0 tot 10 mmHg (diastolische bloeddruk). Positieve orthostatische testen kwamen slechts iets vaker voor bij gezamenlijke toediening; er waren echter geen episodes van symptomatische orthostatische hypotensie of duizeligheid. Patiënten die worden behandeld met PDE-5-remmers in combinatie met silodosine moeten worden gecontroleerd op mogelijke bijwerkingen.
Antihypertensiva
Als onderdeel van het klinische studieprogramma zijn veel patiënten gelijktijdig behandeld met antihypertensiva (voornamelijk met renine-angiotensine-werkende middelen, bètablokkers, calciumkanaalblokkers en diuretica), zonder een verhoogde incidentie van orthostatische hypotensie. Niettemin moet voorzichtigheid worden betracht bij het starten van gelijktijdig gebruik met antihypertensiva en moeten patiënten worden gecontroleerd op mogelijke bijwerkingen.
Digoxine
Steady-state spiegels van digoxine, een substraat van P-glycoproteïne, waren niet significant veranderd bij gelijktijdige toediening met silodosine 8 mg eenmaal daags. Er is geen dosisaanpassing nodig.
04.6 Zwangerschap en borstvoeding
Zwangerschap en borstvoeding
Niet relevant omdat silodosine alleen bedoeld is voor mannelijke patiënten.
Vruchtbaarheid
Gevallen van ejaculatie met verminderde of geen sperma-emissie (zie rubriek 4.8) vanwege de farmacodynamische eigenschappen van silodosine zijn gemeld tijdens behandeling met silodosine. Alvorens met de behandeling te beginnen, moet de patiënt worden geïnformeerd over dit mogelijke effect, dat de mannelijke vruchtbaarheid tijdelijk schaadt.
04.7 Beïnvloeding van de rijvaardigheid en het vermogen om machines te bedienen
Urorec heeft geen of een verwaarloosbare invloed op de rijvaardigheid of op het vermogen om machines te bedienen. Patiënten moeten worden geïnformeerd over het mogelijke optreden van symptomen die verband houden met orthostatische hypotensie (zoals duizeligheid) en moeten worden geadviseerd voorzichtig te zijn bij het autorijden en het bedienen van machines totdat ze zich bewust zijn van de mogelijke effecten van silodosine op hun lichaam.
04.8 Bijwerkingen
Samenvatting van het veiligheidsprofiel
De veiligheid van silodosine werd geëvalueerd in vier dubbelblinde gecontroleerde klinische fase II-III-onderzoeken (met 931 patiënten die eenmaal daags 8 mg silodosine kregen en 733 patiënten die met placebo werden behandeld) en in twee open-labelstudies op lange termijn. In totaal kregen 1.581 patiënten silodosine in een dosis van 8 mg eenmaal daags, waaronder 961 patiënten die gedurende ten minste 6 maanden werden blootgesteld en 384 patiënten die gedurende 1 jaar werden blootgesteld.
De meest voorkomende bijwerkingen die met silodosine werden gemeld in placebogecontroleerde klinische onderzoeken en bij langdurig gebruik waren ejaculatiestoornissen zoals retrograde ejaculatie en anejaculatie (verminderd of afwezig ejaculaatvolume), met een frequentie van 23%. Dit kan de mannelijke vruchtbaarheid tijdelijk verminderen. Dit effect is binnen enkele dagen na het stoppen van de behandeling omkeerbaar (zie rubriek 4.4).
Tabel met bijwerkingen
In de onderstaande tabel zijn bijwerkingen die zijn waargenomen in alle klinische onderzoeken en uit postmarketingervaring wereldwijd waarvoor een redelijk causaal verband is vastgesteld, opgesomd per MedDRA-systeem/orgaanklasse en per frequentie: zeer vaak (≥1/10), vaak ( ≥1 / 100,
1 - Bijwerkingen gemeld via spontane melding op basis van postmarketingervaring wereldwijd (frequenties berekend op basis van voorvallen gemeld in klinische fase I-IV-onderzoeken en niet-interventionele onderzoeken).
Beschrijving van geselecteerde bijwerkingen
Orthostatische hypotensie
De incidentie van orthostatische hypotensie in placebogecontroleerde klinische onderzoeken was 1,2% met silodosine en 1,0% met placebo Orthostatische hypotensie kan soms syncope veroorzaken (zie rubriek 4.4).
Intraoperatief Floppy Iris Syndroom (IFIS)
IFIS is waargenomen tijdens cataractchirurgie (zie rubriek 4.4).
Melding van vermoedelijke bijwerkingen
Het melden van vermoedelijke bijwerkingen die optreden na toelating van het geneesmiddel is belangrijk omdat het een continue controle van de baten/risicoverhouding van het geneesmiddel mogelijk maakt.Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via het nationale meldsysteem.
04.9 Overdosering
Silodosine is geëvalueerd tot maximale doses van 48 mg/dag bij gezonde mannelijke proefpersonen. Orthostatische hypotensie is de dosisbeperkende bijwerking. In geval van recente inname, overweeg braken op te wekken of maagspoeling uit te voeren. Als een overdosis silodosine hypotensie veroorzaakt, moet cardiovasculaire ondersteuning worden geboden. Cardiovasculaire ondersteuning is onwaarschijnlijk. dialyse heeft een significant voordeel, aangezien silodosine sterk eiwitgebonden (96,6%).
05.0 FARMACOLOGISCHE EIGENSCHAPPEN
05.1 Farmacodynamische eigenschappen
Farmacotherapeutische categorie: Urologische middelen, alfa-adrenoceptorantagonisten, ATC-code: G04CA04.
Werkingsmechanisme
Silodosine is zeer selectief voor α1A-adrenoceptoren die zich voornamelijk in de menselijke prostaat, bodem en nek van de urineblaas, prostaatkapsel en prostaaturethra bevinden. De blokkering van deze α1A-adrenoceptoren induceert ontspanning van de gladde spieren van deze weefsels, met als gevolg een vermindering van de weerstand van het uitstroomkanaal van de blaas, zonder de contractiliteit van de gladde spier van de detrusor in gevaar te brengen. Dit resulteert in een verbetering van de symptomen van de lagere urinewegen (symptomen van lagere urinewegen, LUTS) gerelateerd aan het vullen (irriterend) en ledigen (obstructief), die geassocieerd zijn met goedaardige prostaathyperplasie.
Silodosine heeft een duidelijk lagere affiniteit voor α1B-adrenoceptoren die zich voornamelijk in het cardiovasculaire systeem bevinden. in vitro dat de α1A: α1B bindingsverhouding van silodosine (162: 1) extreem hoog is.
Klinische werkzaamheid en veiligheid
In een fase II-dosissetting, dubbelblind, placebogecontroleerd klinisch onderzoek uitgevoerd met silodosine 4 of 8 mg eenmaal daags, werd een meer uitgesproken verbetering van de symptoomscore waargenomen.Amerikaanse Urologische Vereniging (AUA) met 8 mg silodosine (-6,8 ± 5,8, n = 90; p = 0,0018) en 4 mg silodosine (-5,7 ± 5,5, n = 88; p = 0,0355) vergeleken met placebo (-4,0 ± 5,5, n = 83).
Meer dan 800 patiënten met matige tot ernstige BPH-symptomen (Internationale prostaatsymptoomscore, IPSS, baseline ≥13) werden behandeld met silodosine 8 mg eenmaal daags in twee placebogecontroleerde klinische fase III-onderzoeken uitgevoerd in de Verenigde Staten en in één placebo- en actieve comparator-gecontroleerde klinische studie in Europa. In alle onderzoeken werden patiënten die niet reageerden op placebo in een 4 weken durende placebo-aanloopfase gerandomiseerd om onderzoeksbehandeling te krijgen. In alle onderzoeken werd een meer uitgesproken vermindering van zowel vullende (irriterende) als ledigende (obstructieve) symptomen als gevolg van BPH waargenomen bij patiënten die met silodosine werden behandeld in vergelijking met placebo, gemeten na 12 weken behandeling. populaties van elke studie worden hieronder weergegeven:
* pvs-placebo; ° p = 0,002 vs placebo
In de actieve comparator gecontroleerde klinische studie die in Europa werd uitgevoerd, bleek silodosine 8 mg eenmaal daags niet inferieur te zijn in werkzaamheid ten opzichte van tamsulosine 0,4 mg eenmaal daags: het gecorrigeerde gemiddelde verschil (95% BI) in de IPSS-totaalscore tussen behandelingen in de populatie per protocol was 0,4 (-0,4 tot 1,1). Het responspercentage (d.w.z. verbetering van de IPSS-totaalscore met ten minste 25%) was significant hoger in de silodosine- (68%) en tamsulosine- (65%)-groepen vergeleken met de placebo-groep (53%).
In de open-label, langdurige verlengingsfase van deze gecontroleerde onderzoeken, waarin patiënten tot 1 jaar met silodosine werden behandeld, hield de door silodosine geïnduceerde symptoomverbetering in week 12 van de behandeling gedurende 1 jaar aan.
In alle klinische onderzoeken met silodosine werden geen significante verlagingen van de bloeddruk in rugligging waargenomen.
Doses van 8 mg en 24 mg silodosine per dag hadden geen statistisch significant effect op ECG-intervallen of hartrepolarisatie in vergelijking met placebo.
Pediatrische populatie
Het Europees Geneesmiddelenbureau heeft besloten af te zien van de verplichting om de resultaten in te dienen van onderzoek met Urorec in alle subgroepen van pediatrische patiënten met BPH (zie rubriek 4.2 voor informatie over pediatrisch gebruik).
05.2 Farmacokinetische eigenschappen
De farmacokinetiek van silodosine en zijn belangrijkste metabolieten werd onderzocht bij volwassen mannelijke proefpersonen met en zonder BPH na enkelvoudige en meervoudige dosering, met doses variërend van 0,1 mg tot 48 mg per dag. De farmacokinetiek van silodosine is lineair over dit dosisbereik.
De blootstelling aan de belangrijkste metaboliet in plasma, silodosineglucuronide (KMD-3213G), is bij steady-state ongeveer driemaal de blootstelling aan de oorspronkelijke stof. Silodosine en zijn glucuronide bereiken een steady state na respectievelijk 3 dagen en 5 dagen behandeling.
Absorptie
Oraal toegediende silodosine wordt goed geabsorbeerd en de absorptie is dosisproportioneel De absolute biologische beschikbaarheid is ongeveer 32%.
In een studio in vitro uitgevoerd met Caco-2-cellen is aangetoond dat silodosine een substraat is van P-glycoproteïne.
Voedsel verlaagt de Cmax met ongeveer 30%, verhoogt de Tmax met ongeveer 1 uur en heeft beperkte effecten op de AUC.
Bij gezonde mannelijke proefpersonen, representatief voor de leeftijd van de patiënten (n = 16, gemiddelde leeftijd 55 ± 8 jaar), waren er na toediening van 8 mg eenmaal daags gedurende 7 dagen onmiddellijk na het ontbijt de volgende farmacokinetische parameters: Cmax 87 ± 51 ng / ml (SD), Tmax 2,5 uur (bereik 1,0-3,0), AUC 433 ± 286 ng • uur / ml.
Verdeling
Silodosine heeft een distributievolume van 0,81 l/kg en is voor 96,6% gebonden aan plasma-eiwitten. Het verspreidt zich niet in bloedcellen.
De eiwitbinding van silodosineglucuronide is 91%.
Biotransformatie
Silodosine wordt uitgebreid gemetaboliseerd via glucuronidering (UGT2B7), alcoholdehydrogenase, aldehydedehydrogenase en oxidatie, voornamelijk door CYP3A4. De belangrijkste metaboliet in plasma, het glucuronzuurconjugaat van silodosine (KMD-3213G), waarvan is aangetoond dat het actief is in vitro, heeft een verlengde halfwaardetijd (ongeveer 24 uur) en bereikt plasmaconcentraties die ongeveer vier keer hoger zijn dan de silodosineconcentraties. in vitro geven aan dat silodosine niet het vermogen heeft om het cytochroom P450-enzymsysteem te remmen of te induceren.
Eliminatie
Na orale toediening van 14C-gelabeld silodosine was de terugwinning van radioactiviteit na 7 dagen ongeveer 33,5% in urine en 54,9% in feces. De totale klaring van silodosine was ongeveer 0,28 l/u/kg. Silodosine wordt voornamelijk uitgescheiden in de vorm van metabolieten, minimale hoeveelheden van de onveranderde stof worden teruggevonden in de urine. De terminale halfwaardetijd van silodosine en zijn glucuronide is respectievelijk ongeveer 11 uur en 18 uur.
Speciale patiëntenpopulaties
Bejaarden
Blootstelling aan silodosine en zijn belangrijkste metabolieten varieert niet significant met de leeftijd, zelfs niet bij patiënten ouder dan 75 jaar.
Pediatrische populatie
Silodosine is niet onderzocht bij patiënten jonger dan 18 jaar.
leverfunctiestoornis
In een onderzoek met een enkelvoudige dosis was de farmacokinetiek van silodosine niet veranderd bij negen patiënten met een matige leverfunctiestoornis (Child-Pugh-score tussen 7 en 9) vergeleken met negen gezonde vrijwilligers. De resultaten van deze studie moeten met voorzichtigheid worden geïnterpreteerd, aangezien de opgenomen patiënten normale biochemische waarden hadden, wat wijst op een normale metabole functie, en werden geclassificeerd als matig leverinsufficiëntie, op basis van de aanwezigheid van ascites en hepatische encefalopathie.
De farmacokinetiek van silodosine is niet onderzocht bij patiënten met een ernstige leverfunctiestoornis.
Nierfunctiestoornis
In een onderzoek met een enkelvoudige dosis werd bij patiënten met een lichte (n = 8) en matige (n = 8) nierfunctiestoornis gemiddeld een verhoging van de Cmax (1,6-voudig) en de AUC (1,7-voudig) waargenomen bij blootstelling aan silodosine (ongebonden). ) vergeleken met patiënten met een normale nierfunctie (n = 8) Bij proefpersonen met een ernstige nierfunctiestoornis (n = 5) was de toename in blootstelling 2,2-voudig voor Cmax en 3,7 keer voor de AUC. Blootstelling aan de belangrijkste metabolieten, silodosineglucuronide en KMD-3293, was ook verhoogd.
Monitoring van plasmaspiegels in een klinische fase III-studie toonde aan dat de totale silodosinespiegels na 4 weken behandeling niet veranderden bij patiënten met een lichte stoornis (n = 70) in vergelijking met patiënten met een normale nierfunctie (n = 155), terwijl ze verdubbelden op gemiddeld bij patiënten met een matige beperking (n = 7).
Een beoordeling van de veiligheidsgegevens die zijn verkregen bij patiënten die deelnamen aan alle klinische onderzoeken, wijst er niet op dat een lichte nierfunctiestoornis (n = 487) een extra veiligheidsrisico met zich meebrengt tijdens de behandeling met silodosine (zoals verhoogde duizeligheid of orthostatische hypotensie) in vergelijking met patiënten met een normale nierfunctiestoornis. nierfunctiestoornis (n = 955) Bijgevolg is er geen dosisaanpassing nodig bij patiënten met een lichte nierfunctiestoornis Aangezien er slechts beperkte ervaring is bij patiënten met een matige nierfunctiestoornis (n = 35), kan een verlaagde startdosis van 4 mg patiënten met een ernstige nierfunctiestoornis wordt niet aanbevolen.
05.3 Gegevens uit het preklinisch veiligheidsonderzoek
Niet-klinische gegevens duiden niet op een speciaal risico voor mensen. Deze gegevens zijn afkomstig van conventioneel onderzoek van veiligheidsfarmacologie en kankerverwekkend, mutageen en teratogeen potentieel. Effecten bij dieren (aantasting van de schildklier bij knaagdieren) werden alleen waargenomen bij blootstellingen die als voldoende hoger werden beschouwd dan de maximale menselijke blootstelling, wat erop wijst dat deze weinig relevant zijn voor klinisch gebruik.
Bij mannelijke ratten werd onvruchtbaarheid waargenomen bij blootstellingen die ongeveer het dubbele waren van de blootstelling bij de maximaal aanbevolen dosis voor de mens. Het waargenomen effect was omkeerbaar.
06.0 FARMACEUTISCHE INFORMATIE
06.1 Hulpstoffen
Capsule inhoud
Voorgegelatineerd zetmeel (maïs)
Mannitol (E421)
Magnesium stearaat
Natriumlaurylsulfaat
Capsuleomhulsel
Gelei
Titaandioxide (E171)
Geel ijzeroxide (E172)
06.2 Incompatibiliteit
Niet relevant.
06.3 Geldigheidsduur
3 jaar.
06.4 Speciale voorzorgsmaatregelen bij bewaren
Niet bewaren boven 30°C.
Bewaren in de oorspronkelijke verpakking ter bescherming tegen licht en vocht.
06.5 Aard van de primaire verpakking en inhoud van de verpakking
De capsules worden geleverd in blisterverpakkingen van PVC/PVDC/aluminiumfolie, verpakt in kartonnen dozen.
Verpakkingen van 5, 10, 20, 30, 50, 90, 100 capsules.
Mogelijk worden niet alle verpakkingsgrootten in de handel gebracht.
06.6 Instructies voor gebruik en verwerking
Geen speciale instructies.
07.0 HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Recordati Ierland Ltd.
Raheens Oost
Ringaskiddy Co. Cork
Ierland
08.0 NUMMER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
EU / 1/09/608/001
EU / 1/09/608/002
EU / 1/09/608/003
EU / 1/09/608/004
EU / 1/09/608/005
EU / 1/09/608/006
EU / 1/09/608/007
039789019
039789021
039789033
039789045
039789058
039789060
039789072
09.0 DATUM VAN EERSTE VERGUNNING OF VERLENGING VAN DE VERGUNNING
Datum eerste autorisatie: 29/01/2010
10.0 DATUM VAN HERZIENING VAN DE TEKST
D.CCE september 2014