Actieve ingrediënten: Lidocaïne
Versatis 5% medicinale pleister
Waarom wordt Versatis gebruikt? Waar is het voor?
Versatis bevat lidocaïne, een lokale pijnstiller, die werkt door pijn in de huid te verminderen. Het is aan u voorgeschreven voor de behandeling van pijn veroorzaakt door postherpetische neuralgie. Deze aandoening wordt over het algemeen gekenmerkt door plaatselijke symptomen zoals brandende, stekende of stekende pijn.
Contra-indicaties Wanneer Versatis niet mag worden gebruikt
Gebruik geen Versatis
- als u allergisch bent voor lidocaïne of voor één van de andere bestanddelen van dit geneesmiddel (vermeld in rubriek 6)
- als u een allergische reactie heeft gehad op andere lidocaïne-achtige producten, zoals bupivacaïne, etidocaïne, mepivacaïne of prilocaïne
- op een beschadigde huid of open wonden.
Voorzorgen bij gebruik Wat u moet weten voordat u Versatis inneemt
Neem contact op met uw arts of apotheker voordat u Versatis gebruikt. Als u een ernstige leverziekte heeft of ernstige hart- of nierproblemen heeft, moet u met uw arts overleggen voordat u Versatis gebruikt. Versatis moet op de huid worden aangebracht nadat de laesies van de gordelroos zijn genezen en niet op of nabij de ogen of mond.
Lidocaïne wordt in de lever gemetaboliseerd tot talrijke verbindingen. Eén zo'n verbinding is 2.6 xylidine, waarvan is aangetoond dat het tumoren veroorzaakt bij ratten wanneer het continu in zeer hoge doses wordt gegeven. De waarde van deze gegevens bij mensen is niet bekend.
Kinderen en adolescenten
Versatis is niet onderzocht bij patiënten jonger dan 18 jaar, daarom wordt het gebruik bij deze patiënten niet aanbevolen.
Interacties Welke medicijnen of voedingsmiddelen kunnen het effect van Versatis veranderen
Vertel het uw arts of apotheker als u andere geneesmiddelen gebruikt, kort geleden heeft gebruikt of in de nabije toekomst gaat gebruiken.
Waarschuwingen Het is belangrijk om te weten dat:
Zwangerschap, borstvoeding en vruchtbaarheid
Als u zwanger bent, denkt zwanger te zijn of zwanger wilt worden, of als u borstvoeding geeft, vraag dan uw arts of apotheker om advies voordat u dit geneesmiddel gebruikt.Versatis mag niet tijdens de zwangerschap worden gebruikt, tenzij strikt noodzakelijk. Er zijn geen studies over het gebruik van de pleister tijdens borstvoeding. Bij gebruik van Versatis kan er slechts een kleine hoeveelheid van het werkzame bestanddeel, lidocaïne, in het bloed aanwezig zijn. Een effect op baby's die borstvoeding krijgen is onwaarschijnlijk.
Rijvaardigheid en het gebruik van machines
Een effect van Versatis op de rijvaardigheid of het vermogen om machines te bedienen is onwaarschijnlijk. Daarom is het mogelijk om auto te rijden of aan machines te werken tijdens het gebruik van Versatis.
Versatis bevat propyleenglycol, methylparahydroxybenzoaat en propylparahydroxybenzoaat.
De pleisters bevatten propyleenglycol (E1520), wat huidirritatie kan veroorzaken. Bovendien bevatten ze methylparahydroxybenzoaat (E218) en propylparahydroxybenzoaat (E216) die allergische reacties kunnen veroorzaken. Soms kunnen allergische reacties optreden na het gebruik van de pleisters gedurende een bepaalde tijd.
Dosis, wijze en tijdstip van toediening Hoe gebruikt u Versatis: Dosering
Gebruik dit geneesmiddel altijd precies zoals uw arts u dat heeft verteld. Raadpleeg bij twijfel uw arts of apotheker. Normaal gesproken is de dagelijkse dosering één tot drie pleisters ter grootte van het gebied met een zere huid.Versatis kan in kleinere stukjes worden gesneden om het getroffen gebied te bedekken. U mag niet meer dan 3 pleisters tegelijk gebruiken. De pleisters moeten na 12 uur aanbrengen worden verwijderd; op deze manier heeft u een periode van 12 uur zonder pleister. U kunt kiezen of u Versatis overdag of 's nachts toepast. Over het algemeen zult u vanaf de eerste dag van gebruik enige pijnverlichting voelen, maar het kan tot 2-4 weken duren voordat het pijnstillende effect van Versatis volledig is. Als de pijn na deze tijd nog steeds erg hevig is, vertel dit dan aan uw arts, aangezien het voordeel van de behandeling moet worden afgewogen tegen de mogelijke risico's (zie "Waarschuwingen en voorzorgen").
Uw arts zal regelmatig controleren of Versatis werkt.
Voordat u Versatis op het getroffen gebied aanbrengt
- als het pijnlijke deel van de huid bedekt is met haar of haar, moet het met een schaar worden geknipt en mogen ze niet worden geschoren.
- De huid moet schoon en droog zijn.
- Crèmes of lotions mogen alleen op de behandelde huid worden gebruikt gedurende de periode dat de pleister niet wordt aangebracht.
- Als u net een bad of douche heeft genomen, moet u wachten tot uw huid is afgekoeld voordat u de pleister aanbrengt.
Breng de pleister aan
Stap 1: Open het zakje en verwijder een of meer pleisters
- scheur of knip de envelop langs de stippellijn
- als u een schaar gebruikt, pas dan op dat u de pleisters niet beschadigt
- neem een of meer pleisters, afhankelijk van de grootte van het pijnlijke deel van de huid
Stap 2: Sluit de envelop
- sluit de zak na gebruik goed af
- de pleister bevat water en kan uitdrogen als het zakje niet goed wordt gesloten
Stap 3: Knip de pleister indien nodig af
- knip indien nodig, voordat u de film verwijdert, de pleister op de maat die nodig is om het pijnlijke deel van de huid te bedekken.
Stap 4: Verwijder de film
- verwijder de transparante film van de patch
- probeer het plakkerige deel van de pleister niet aan te raken
Stap 5: Breng de pleister aan en druk stevig op de huid
- breng maximaal drie pleisters aan op het pijnlijke deel van de huid
- druk de pleister op de huid
- houd de pleister minimaal 10 seconden ingedrukt zodat de pleister goed op de huid hecht
- zorg ervoor dat de hele pleister, inclusief de randen, aan de huid hecht.
Laat de pleister slechts 12 uur zitten
Het is belangrijk dat Versatis slechts 12 uur op de huid wordt aangebracht. Als u bijvoorbeeld 's nachts meer pijn voelt, kunt u de pleister om 19.00 uur aanbrengen en om 7.00 uur verwijderen. Als u overdag meer pijn voelt, kunt u Versatis om 7 uur 's ochtends aanbrengen en om 7 uur 's avonds weer verwijderen.
Bad, douche en zwemmen
Aangezien contact van Versatis met water moet worden vermeden, mogen baden, douches of zwemmen worden gedaan zolang de pleister niet wordt aangebracht.Na het baden of douchen moet de huid worden afgekoeld voordat u de pleister aanbrengt.
Als de pleister eraf valt
In zeer zeldzame gevallen kan de pleister loslaten of niet goed hechten. Als dit het geval is, probeer het dan opnieuw op hetzelfde gebied te bevestigen. Als het niet plakt, verwijder het dan volledig en breng een nieuwe pleister aan, altijd op hetzelfde gebied.
Hoe Versatis te verwijderen
Om de pleister te verwisselen, verwijdert u de oude pleister langzaam. Als het niet gemakkelijk loslaat, kunt u het een paar minuten nat maken met heet water voordat u het verwijdert.
Overdosering Wat te doen als u te veel Versatis heeft ingenomen
Wat u moet doen als u de pleister na 12 uur bent vergeten te verwijderen
Verwijder de pleister zodra u eraan denkt. De nieuwe pleister kan na 12 uur worden aangebracht.
Wat u moet doen als u meer pleisters heeft gebruikt dan u zou mogen
Als u meer pleisters gebruikt dan u nodig heeft of deze te lang aanhoudt, kan het risico op bijwerkingen toenemen.
Bent u vergeten Versatis aan te brengen
Als u bent vergeten een nieuwe pleister aan te brengen na een pauze van 12 uur zonder de vorige pleister, breng de nieuwe pleister dan aan zodra u eraan denkt.
Als u nog vragen heeft over het gebruik van dit geneesmiddel, neem dan contact op met uw arts of apotheker.
Bijwerkingen Wat zijn de bijwerkingen van Versatis
Zoals alle geneesmiddelen kan ook dit geneesmiddel bijwerkingen hebben, al krijgt niet iedereen daarmee te maken. Als er irritatie of een branderig gevoel is tijdens het aanbrengen van de pleister, moet de pleister worden verwijderd.Breng geen nieuwe pleister aan op dat gebied totdat de irritatie is genezen.
Zeer vaak voorkomende bijwerkingen die bij meer dan 1 op de 10 mensen kunnen optreden, worden hieronder vermeld.
Deze omvatten veranderingen in de huid op of nabij het aanbrenggebied van de pleister en kunnen roodheid, uitslag, jeuk, branderig gevoel, dermatitis en blaren omvatten.
Soms voorkomende bijwerkingen die bij maximaal 1 op de 100 mensen kunnen optreden, worden hieronder vermeld.
Huidveranderingen en wonden
Zeer zelden voorkomende bijwerkingen, die bij maximaal 1 op de 10.000 mensen kunnen optreden, worden hieronder vermeld.
Open wonden, ernstige allergische reacties en allergie.
Melding van bijwerkingen
Krijgt u last van bijwerkingen, neem dan contact op met uw arts of apotheker.Dit geldt ook voor mogelijke bijwerkingen die niet in deze bijsluiter staan. U kunt bijwerkingen ook rechtstreeks melden via het nationale meldsysteem op http://www.agenziafarmaco.gov.it/it/responsabili Door bijwerkingen te melden, kunt u ons helpen meer informatie te verkrijgen over de veiligheid van dit geneesmiddel.
Vervaldatum en retentie
Buiten het zicht en bereik van kinderen houden. Gebruik dit geneesmiddel niet meer na de vervaldatum die staat vermeld op het zakje en de doos na EXP.De vervaldatum verwijst naar de laatste dag van die maand. Niet in de koelkast of vriezer bewaren. Sluit de zak zorgvuldig na de eerste opening. Na opening van het zakje moeten de pleisters binnen 14 dagen worden gebruikt. Gebruik dit geneesmiddel niet als u merkt dat het zakje beschadigd is. Dan kan de pleister uitgedroogd zijn en daardoor niet goed hechten.
Hoe Versatis te verwijderen
De gebruikte pleisters bevatten nog steeds een actief ingrediënt dat gevaarlijk kan zijn voor anderen. Vouw de oude lapjes dubbel, met de plakzijde naar binnen, en gooi ze weg, zodat ze buiten bereik van kinderen blijven.
Gooi geneesmiddelen niet weg via het afvalwater of met huishoudelijk afval. Vraag uw apotheker wat u met geneesmiddelen moet doen die u niet meer gebruikt. Dit helpt het milieu te beschermen.
Samenstelling en farmaceutische vorm
Wat bevat Versatis
- het actieve ingrediënt is lidocaïne
- elke pleister van 10 cm x 14 cm bevat 700 mg (5% w/w) lidocaïne
- de andere bestanddelen van de pleister (hulpstoffen) zijn: glycerol, vloeibaar kristalliseerbare sorbitol, natriumcarmellose, propyleenglycol (E1520), ureum, zwaar kaolien, wijnsteenzuur, gelatine, polyvinylalcohol, aluminiumglycinaat, dinatriumedetaat, methylparahydroxybenzoaat (E218) , propylparahydroxybenzoaat (E216), polyacrylzuur, natriumpolyacrylaat, gezuiverd water.
De steunlaag en de hechtlaag: polyethyleentereftalaat (PET).
Beschrijving van hoe Versatis eruit ziet en de inhoud van het pakket
De medicinale pleisters zijn 14 cm lang en 10 cm breed. Ze zijn wit, van zacht materiaal en dragen het opschrift "lidocaïne 5%". De pleisters zijn verpakt in hersluitbare zakjes met elk 5 pleisters.
Elke verpakking bevat 5, 10, 20, 25 of 30 pleisters, verpakt in respectievelijk 1, 2, 4, 5 of 6 zakjes.
Niet alle pakketten zijn in de handel verkrijgbaar.
Bron Bijsluiter: AIFA (Italiaans Geneesmiddelenbureau). Inhoud gepubliceerd in januari 2016. De aanwezige informatie is mogelijk niet up-to-date.
Om toegang te hebben tot de meest actuele versie, is het raadzaam om de website van AIFA (Italian Medicines Agency) te bezoeken. Disclaimer en nuttige informatie.
01.0 NAAM VAN HET GENEESMIDDEL
VERSATIS 5% GEDICHTEERDE PATCH
02.0 KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
Elke pleister van 10 cm x 14 cm bevat 700 mg (5% w/w) lidocaïne (50 mg lidocaïne/gram lijmbasis)
Hulpstoffen met bekend effect:
Methylparahydroxybenzoaat 14 mg
Propylparahydroxybenzoaat 7 mg
Propyleenglycol 700 mg
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1.
03.0 FARMACEUTISCHE VORM
Medicinale pleister
Witte hydrogelpleister met kleefstof aangebracht op een non-woven polyethyleentereftalaatdrager met de tekst "Lidocaine 5%" in reliëf en bedekt met een beschermende film van polyethyleentereftalaat.
04.0 KLINISCHE INFORMATIE
04.1 Therapeutische indicaties
Versatis is geïndiceerd voor de symptomatische behandeling van neuropathische pijn geassocieerd met eerdere herpes zoster-infectie (postherpetische neuralgie, NPH) bij volwassenen.
04.2 Dosering en wijze van toediening
Volwassenen en ouderen
Het pijnlijke gebied moet worden bedekt met de pleister, die eenmaal per dag gedurende maximaal 12 uur binnen 24 uur wordt aangebracht. Alleen de pleisters die nodig zijn voor een effectieve behandeling mogen worden aangebracht. Indien nodig kan de pleister met een schaar in kleinere delen worden gesneden voordat de beschermfolie wordt verwijderd. In totaal mogen niet meer dan drie pleisters tegelijk worden aangebracht.
De pleister moet worden aangebracht op een intacte, droge en niet-geïrriteerde huid (na genezing van herpeslaesies).
Elke pleister mag niet langer dan 12 uur worden aangebracht. Het vrije interval vanaf de volgende applicatie moet minimaal 12 uur zijn.De pleister kan overdag of 's nachts worden aangebracht.
De pleister moet onmiddellijk op de huid worden aangebracht nadat deze uit het zakje is gehaald en de beschermende film van het hydrogeloppervlak is verwijderd. Haar en haar in het toepassingsgebied moeten met een schaar worden geknipt (niet geschoren).
De behandeling moet na 2-4 weken opnieuw worden geëvalueerd. Als er na deze periode geen therapeutische respons op Versatis is geweest (tijdens het aanbrengen van de pleister en/of de pleistervrije periode, dient de behandeling te worden gestaakt, aangezien in deze situatie de potentiële risico's de voordelen zouden kunnen overtreffen (zie rubrieken 4.4 en 5.1. Langdurig gebruik van Versatis in klinische onderzoeken heeft aangetoond dat het aantal te gebruiken pleisters in de loop van de tijd afneemt. Daarom moet de behandeling met regelmatige tussenpozen opnieuw worden beoordeeld om te beslissen of het aantal pleisters dat nodig is om het pijnlijke gebied te bedekken kan worden verminderd of dat het vrije interval tussen het aanbrengen van de pleister kan worden verlengd.
Nierfunctiestoornis
Bij patiënten met lichte of matige nierinsufficiëntie zijn geen dosisaanpassingen nodig. Versatis moet met voorzichtigheid worden gebruikt bij patiënten met een ernstige nierfunctiestoornis (zie rubriek 4.4).
leverfunctiestoornis
Bij patiënten met een lichte of matige leverfunctiestoornis zijn geen dosisaanpassingen nodig. Versatis moet met voorzichtigheid worden gebruikt bij patiënten met een ernstige leverfunctiestoornis (zie rubriek 4.4).
Pediatrische populatie
De veiligheid en werkzaamheid van Versatis bij patiënten jonger dan 18 jaar zijn niet vastgesteld. Er zijn geen gegevens beschikbaar.
04.3 Contra-indicaties
Overgevoeligheid voor de werkzame stof of voor één van de in rubriek 6.1 vermelde hulpstoffen. De pleister is ook gecontra-indiceerd bij patiënten met een bekende overgevoeligheid voor andere lokale anesthetica van het amidetype, zoals bupivacaïne, etidocaïne, mepivacaïne en prilocaïne.
De pleister mag niet worden aangebracht op een ontstoken of beschadigde huid, zoals actieve herpes zoster-laesies, atopische dermatitis, wonden.
04.4 Bijzondere waarschuwingen en passende voorzorgen bij gebruik
De pleister mag niet op de slijmvliezen worden aangebracht. Contact van de pleister met de ogen moet worden vermeden.
De pleister bevat propyleenglycol dat huidirritatie kan veroorzaken. Het bevat ook methylparahydroxybenzoaat en propylparahydroxybenzoaat, die allergische reacties kunnen veroorzaken (zelfs vertraagd).
De pleister moet met voorzichtigheid worden gebruikt bij patiënten met ernstige hart-, nier- of leverschade.
Een van de lidocaïnemetabolieten, 2,6 xylidine, bleek een genotoxische en carcinogene werking te hebben bij ratten (zie rubriek 5.3). Secundaire metabolieten bleken mutageen te zijn. De klinische betekenis van deze bevinding is niet bekend. Bijgevolg is een langdurige behandeling met Versatis alleen gerechtvaardigd door een werkelijk therapeutisch voordeel voor de patiënt (zie rubriek 4.2).
04.5 Interacties met andere geneesmiddelen en andere vormen van interactie
Er zijn tot nu toe geen interactiestudies beschikbaar. In klinische onderzoeken met de pleister werden geen klinisch relevante interacties gemeld.
Aangezien de maximale plasmaconcentraties van lidocaïne die werden waargenomen in klinische onderzoeken met de pleister laag waren (zie rubriek 5.2), zijn klinisch relevante farmacokinetische interacties onwaarschijnlijk.
Hoewel de absorptie van lidocaïne door de huid gewoonlijk laag is, moet de pleister met voorzichtigheid worden gebruikt bij patiënten die klasse I-antiaritmica (bijv. tocaïnide, mexiletine) of andere lokale anesthetica krijgen, aangezien het risico van een systemisch additie-effect niet kan worden uitgesloten.
04.6 Zwangerschap en borstvoeding
Zwangerschap
Lidocaïne passeert de placentabarrière. Er zijn echter onvoldoende gegevens over het gebruik van lidocaïne bij zwangere vrouwen.
Dierstudies wijzen niet op een teratogeen potentieel van lidocaïne. (zie punt 5.3).
Het potentiële risico voor mensen is niet bekend.Daarom mag Versatis niet tijdens de zwangerschap worden gebruikt, tenzij duidelijk aangegeven.
Borstvoeding
Lidocaïne wordt uitgescheiden in de moedermelk. Voor de pleister zijn er echter geen klinische onderzoeken bij vrouwen die borstvoeding geven. Aangezien het metabolisme van lidocaïne relatief snel is en bijna volledig in de lever plaatsvindt, wordt aangenomen dat slechts een zeer kleine hoeveelheid lidocaïne in de moedermelk kan worden uitgescheiden.
Vruchtbaarheid
Er zijn geen klinische gegevens over vruchtbaarheid beschikbaar. Dierstudies hebben geen effecten op de vrouwelijke vruchtbaarheid aangetoond.
04.7 Beïnvloeding van de rijvaardigheid en het vermogen om machines te bedienen
Er is geen onderzoek gedaan naar de effecten op de rijvaardigheid of op het vermogen om machines te bedienen. Aangezien de systemische absorptie minimaal is (rubriek 5.2), zijn effecten op de rijvaardigheid of het vermogen om machines te bedienen onwaarschijnlijk.
04.8 Bijwerkingen
De volgende bijwerkingen worden gerapporteerd in afnemende volgorde van ernst binnen elke frequentiegroep.
Ongeveer 16% van de patiënten die worden behandeld, kan bijwerkingen krijgen. Dit zijn lokale reacties vanwege de kenmerken van het medicijn.
De meest gemelde bijwerkingen waren reacties op de toedieningsplaats (zoals een branderig gevoel, dermatitis, erytheem, pruritus, huiduitslag, huidirritatie en blaren).
De onderstaande tabel geeft een overzicht van bijwerkingen die zijn gemeld door patiënten die de pleister gebruikten in onderzoeken naar postherpetische neuralgie. Ze zijn gerangschikt op klasse en frequentie in de verschillende apparaten. Hun frequentie is gedefinieerd als: zeer vaak ≥ 1/10; gemeenschappelijk ≥ 1/100 tot
De volgende reacties zijn waargenomen bij patiënten die de pleister gebruikten in een postmarketingsetting
Alle bijwerkingen waren over het algemeen licht of matig van intensiteit. Minder dan 5% van hen leidde tot stopzetting van de behandeling.
Bij correct gebruik van de pleister zijn systemische bijwerkingen onwaarschijnlijk aangezien de systemische concentratie van lidocaïne erg laag is (zie rubriek 5.2). Systemische bijwerkingen van lidocaïne zijn vergelijkbaar met die waargenomen voor andere amiden die worden gebruikt als lokale anesthetica (zie rubriek 4.9).
Melding van vermoedelijke bijwerkingen
Het melden van vermoedelijke bijwerkingen die optreden na toelating van het geneesmiddel is belangrijk omdat het een continue controle van de baten/risicoverhouding van het geneesmiddel mogelijk maakt. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via het nationale meldsysteem. "Italiaans Geneesmiddelenbureau Website: http://www.agenziafarmaco.gov.it/it/responsabili
04.9 Overdosering
Overdosering met de pleister is onwaarschijnlijk, maar het kan niet worden uitgesloten dat onjuist gebruik van de pleister, zoals het gelijktijdig gebruik van een groot aantal pleisters, voor een langere periode van aanbrengen of gebruik op een beschadigde huid, kan leiden tot een hoger dan normaal plasma niveaus van lidocaïne. Mogelijke tekenen van systemische toxiciteit zijn vergelijkbaar met die waargenomen na toediening van lidocaïne als lokaal anestheticum en kunnen de volgende tekenen en symptomen omvatten: duizeligheid, braken, slaperigheid, toevallen, mydriasis, bradycardie, aritmie en shock.
Bovendien kunnen bekende interacties tussen systemische concentraties van lidocaïne met bètablokkers, CYP3A4-remmers (bijv. imidazoolderivaten, macroliden) en anti-aritmica relevant worden in geval van overdosering.
Als overdosering wordt vermoed, moet de pleister worden verwijderd en moeten ondersteunende maatregelen worden genomen als dit klinisch noodzakelijk is. Er is geen tegengif voor lidocaïne.
05.0 FARMACOLOGISCHE EIGENSCHAPPEN
05.1 Farmacodynamische eigenschappen
Farmacotherapeutische categorie: lokale anesthetica, amiden
ATC-code: N01BB02
Werkingsmechanisme
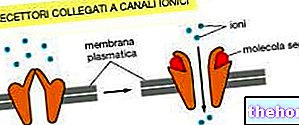
Versatis heeft een dubbel werkingsmechanisme: de farmacologische activiteit van lidocaïne en de mechanische werking van de hydrogelpleister die het overgevoelige gebied beschermt.
Lidocaïne in de Versatis-pleisters verspreidt zich continu in de huid en zorgt voor een lokaal pijnstillend effect. Het werkingsmechanisme is gerelateerd aan de stabilisatie van neuronale membranen, waarvan wordt aangenomen dat het de oorzaak is naar beneden regulering van natriumkanalen en dus pijnvermindering.
Klinische werkzaamheid
Pijnbestrijding bij NPH is moeilijk. Er zijn aanwijzingen voor de werkzaamheid van Versatis bij de symptomatische verlichting van de allodynamische component van NPH in sommige gevallen (zie rubriek 4.2).
De werkzaamheid van Versatis is aangetoond in onderzoeken naar postherpetische neuralgie.
Er zijn twee belangrijke gecontroleerde onderzoeken uitgevoerd om de werkzaamheid van 5% lidocaïne-medicinale pleisters te evalueren.
In de eerste studie werden de patiënten gerekruteerd uit een reeds geloofde populatie "antwoorderDit was een cross-over-onderzoek, waarbij 14 dagen behandeling met 5% lidocaïne-medicinale pleisters werd gevolgd door placebo of omgekeerd.Het primaire doel was de "tijd om af te sluiten", d.w.z. het tijdstip waarop patiënten het onderzoek verlieten omdat de pijnverlichting 2 punten lager was dan hun gebruikelijke respons op een 6-puntsschaal (van verergering tot volledige pijnverlichting). Van de 32 gerekruteerde patiënten voltooiden 30 de studie. De "tijd om af te sluiten" het gemiddelde voor placebo was 4 dagen, terwijl het voor het actieve geneesmiddel 14 dagen was (p
In de tweede studie werden 265 patiënten met postherpetische neuralgie gerekruteerd voor een 8 weken durende open-label behandeling met 5% lidocaïne pleister. In dit ongecontroleerde onderzoek reageerde ongeveer 50% van de patiënten op de behandeling met een verlaging van ten minste vier punten op een 6-puntsschaal (van verslechtering tot volledige verlichting). In totaal werden 71 patiënten gerandomiseerd om placebo of 5% lidocaïne-medicamenteuze pleisters te krijgen die gedurende 2-14 dagen werden toegediend. Het primaire eindpunt werd gedefinieerd als gebrek aan werkzaamheid gedurende 2 opeenvolgende dagen omdat pijnverlichting twee punten lager was dan de normale respons op de zespuntsschaal (variërend van verergering tot totale remissie), wat leidde tot stopzetting van de behandeling. bij 9/36 patiënten die met het geneesmiddel werden behandeld en bij 16/35 patiënten die met placebo werden behandeld.
Post-hocanalyses van de tweede studie toonden aan dat de initiële respons onafhankelijk was van de duur van de reeds bestaande NPH-aandoening.Het feit dat patiënten met een langere duur van NPH (> 12 maanden) het meeste baat hebben bij actieve behandeling, wordt echter ondersteund door de bevinding dat deze groep patiënten vaker stopte met het onderzoek vanwege ineffectiviteit bij het overschakelen op placebobehandeling tijdens de dubbelblinde fasestudie .
In een open-label gecontroleerde studie lijkt Versatis een "vergelijkbare werkzaamheid met pregabaline te hebben bij 98 patiënten met PHN, met een gunstig veiligheidsprofiel.
05.2 "Farmacokinetische eigenschappen
Absorptie
Wanneer de 5% lidocaïne-medicinale pleister wordt gebruikt binnen de aanbevolen maximale dosis (3 pleisters gelijktijdig aangebracht gedurende 12 uur), is ongeveer 3 ± 2% van de totale toegediende lidocaïnedosis systemisch beschikbaar voor zowel enkelvoudige als meervoudige toedieningen.
Populatiekinetische analyse uitgevoerd tijdens klinische werkzaamheidsstudies bij NPH-patiënten toonde een gemiddelde maximale lidocaïneconcentratie van 45 ng/ml aan na gelijktijdige toepassing van 3 pleisters, 12 uur per dag, herhaald gedurende maximaal een jaar. Deze waarde komt overeen met die gevonden in farmacokinetische studies bij patiënten met NPH (52 ng/ml) en bij gezonde vrijwilligers (85 ng/ml en 125 ng/ml).
Er was geen neiging tot accumulatie van lidocaïne en zijn metabolieten MEGX, GX en 2,6 xylidine; stabiele toestand ze worden bereikt in de eerste 4 dagen.
Populatiekinetische analyse gaf aan dat systemische blootstelling een proportioneel kleinere toename laat zien dan het aantal gelijktijdig aangebrachte pleisters, wanneer hun aantal toeneemt van 1 naar 3.
Verdeling
Na intraveneuze toediening van lidocaïne aan gezonde vrijwilligers was het distributievolume 1,3 ± 0,4 l/kg (gemiddelde ± SD, n = 15). Het distributievolume is niet leeftijdsafhankelijk, het is verminderd bij patiënten met congestieve hartziekte en verhoogd bij patiënten met leverziekte. Bij plasmaconcentraties bepaald door het aanbrengen van een pleister, bindt ongeveer 70% van lidocaïne aan plasma-eiwitten Lidocaïne passeert de placenta en de bloed-hersenbarrière, waarschijnlijk door passieve diffusie.
Biotransformatie
Lidocaïne wordt in de lever snel gemetaboliseerd tot een aantal metabolieten. De belangrijkste metabole route van lidocaïne is N-dealkylering tot mono-ethylglycinxylidide (MEGX) en glycinxylidide (GX), die beide minder actief zijn dan lidocaïne en in lage concentraties beschikbaar zijn. Deze metabolieten worden gehydrolyseerd tot 2,6-xylidine dat door conjugatie wordt omgezet in 4-hydroxy-2,6-xylidine.
De farmacologische activiteit van de metaboliet 2,6-xylidine is niet bekend, maar vertoont carcinogeen potentieel bij ratten (zie rubriek 5.3). Een populatiekinetische analyse onthulde een gemiddelde maximale concentratie voor 2,6-xylidine van 9 ng/ml na dagelijkse herhaalde aanvragen tot 1 jaar. Deze bevinding wordt bevestigd door een farmacokinetisch onderzoek in fase I. Gegevens over het lidocaïnemetabolisme in de huid zijn niet beschikbaar.
Eliminatie
Lidocaïne en zijn metabolieten worden uitgescheiden door de nieren. Meer dan 85% van de dosis wordt in de urine teruggevonden in de vorm van metabolieten of werkzame stof. Minder dan 10% van de dosis lidocaïne wordt onveranderd uitgescheiden. De belangrijkste metaboliet in de urine is een conjugaat van 4-hydroxy-2, 6-xylidine, dat ongeveer 70-80% van de dosis vertegenwoordigt die in de urine wordt uitgescheiden Bij mensen wordt 2,6-xylidine in de urine uitgescheiden in concentraties van minder dan 1% van de dosis De gemiddelde eliminatiehalfwaardetijd van lidocaïne na het aanbrengen van de pleister bij gezonde vrijwilligers is 7,6 uur. De uitscheiding van lidocaïne en zijn metabolieten kan vertraagd zijn in het geval van hart-, nier- of leverinsufficiëntie.
05.3 Gegevens uit het preklinisch veiligheidsonderzoek
Effecten in preklinische algemene toxiciteitsonderzoeken werden alleen waargenomen bij doses die als voldoende hoger werden beschouwd dan de maximaal haalbare menselijke blootstelling, wat wijst op een lage klinische relevantie.
Lidocaïnehydrochloride was niet genotoxisch in de onderzoeken in vitro of in vivo. Zijn metaboliet geproduceerd door hydrolyse, 2,6-xylidine, vertoonde genotoxische activiteit in verschillende tests, vooral na metabolische activering.
Er zijn geen carcinogeniteitsonderzoeken met lidocaïne uitgevoerd. Studies uitgevoerd op de metaboliet 2,6-xylidine, gemengd in het dieet van mannelijke en vrouwelijke ratten, hebben behandelingsgerelateerde cytotoxiciteit aangetoond: hyperplasie van het reukepitheel van de neus, carcinomen en adenomen in de neusholtes zijn ook waargenomen. op lever- en subcutaan niveau Aangezien het risico voor de mens onduidelijk is, dient een langdurige behandeling met lidocaïne te worden vermeden.
Lidocaïne had geen effect op de algehele reproductiecapaciteit, vrouwelijke vruchtbaarheid of embryo-foetale ontwikkeling/teratogenese bij ratten die werden onderworpen aan plasmaconcentraties tot 50 keer die waargenomen bij patiënten. Dierstudies met betrekking tot mannelijke vruchtbaarheid, bevalling of postnatale ontwikkeling zijn niet volledig.
06.0 FARMACEUTISCHE INFORMATIE
06.1 Hulpstoffen
Zelfklevende laag
Glycerol, vloeibaar kristalliseerbare sorbitol, natriumcarmellose, propyleenglycol (E1520), ureum, zwaar kaolien, wijnsteenzuur, gelatine, polyvinylalcohol, aluminiumglycinaat, dinatriumedetaat, methylparahydroxybenzoaat (E218), propylparahydroxybenzoaat (E216), polyacrylzuur, natrium polyacrylaat, gezuiverd water.
Steun
Polyethyleentereftalaat (PET)
Film
Polyethyleentereftalaat
06.2 Incompatibiliteit
Niet relevant.
06.3 Geldigheidsduur
3 jaar.
Na opening van het zakje moet de pleister binnen 14 dagen worden gebruikt.
06.4 Speciale voorzorgsmaatregelen bij bewaren
Niet in de koelkast of vriezer bewaren. Houd het zakje gesloten na de eerste opening.
06.5 Aard van de primaire verpakking en inhoud van de verpakking
Hersluitbare zakken van papier / polyethyleen / aluminium / ethyleenzuur meta-acrylcopolymeer, met 5 pleisters.
Elke verpakking bevat 5, 10, 20, 25 of 30 pleisters.
Mogelijk worden niet alle verpakkingsgrootten in de handel gebracht.
06.6 Instructies voor gebruik en verwerking
Na gebruik bevat de pleister nog werkzame stof.Na het verwijderen dient de pleister dubbel te worden gevouwen, met de kleeflaag naar binnen zodat de zelfklevende laag niet bloot komt te liggen en moet worden weggegooid.
De ongebruikte of weggegooide pleister moet worden weggegooid in overeenstemming met de lokale regelgeving.
07.0 HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
AIC-HOUDER: GRÜNENTHAL ITALIA S.r.l. via Carlo Bo 11 20143 Milaan
08.0 NUMMER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
10 medicinale pleisters 5% AIC n. 040335022
30 medicinale pleisters 5% AIC n. 040335059
09.0 DATUM VAN EERSTE VERGUNNING OF VERLENGING VAN DE VERGUNNING
Datum eerste registratie: maart 2012
Datum van laatste verlenging: 5.01.2012
10.0 DATUM VAN HERZIENING VAN DE TEKST
30 mei 2015