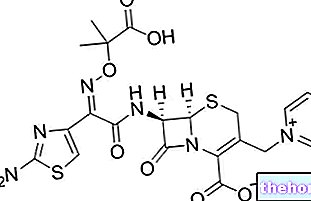
Actieve ingrediënten: Domperidon
RAXAR 10 mg orodispergeerbare tabletten
Waarom wordt Raxar gebruikt? Waar is het voor?
Dit geneesmiddel bevat domperidon, een dopamine-antagonist. Het is een geneesmiddel dat inwerkt op de maagmotiliteit.
Dit geneesmiddel wordt gebruikt bij volwassenen en adolescenten (12 jaar of ouder en met een gewicht van 35 kg of meer) om misselijkheid (misselijkheid) en braken (misselijkheid) te behandelen.
Contra-indicaties Wanneer Raxar niet mag worden gebruikt
Neem geen RAXAR 10 mg orodispergeerbare tablet in de volgende gevallen:
- Bekende allergie voor domperidon of voor één van de andere bestanddelen van dit geneesmiddel (zie samenstelling).
- Prolactinoom (hypofyseziekte)
- Maag- of darmbloeding, darmobstructie of maag-darmperforatie.
- Matige of ernstige leverfunctiestoornis
- Als het ECG (elektrocardiogram) een hartaandoening detecteert die "verlenging van het" gecorrigeerde QT-interval "wordt genoemd
- Als u een aandoening heeft of heeft gehad waarbij uw hart niet in staat is het bloed door uw lichaam te pompen zoals zou moeten (een aandoening die hartfalen wordt genoemd).
- Als u een aandoening heeft waardoor u een laag kalium- of magnesiumgehalte of een hoog kaliumgehalte in uw bloed heeft.
- Als u bepaalde geneesmiddelen gebruikt (zie "Andere geneesmiddelen en RAXAR")
BIJ TWIJFEL, RAADPLEEG UW ARTS OF APOTHEKER.
Voorzorgen bij gebruik Wat u moet weten voordat u Raxar inneemt
Wees extra voorzichtig met RAXAR 10 mg orodispergeerbare tablet:
- Als uw arts u heeft verteld dat u bepaalde suikers niet verdraagt, neem dan contact op met uw arts voordat u dit geneesmiddel inneemt;
- Vertel het uw arts als u leverproblemen heeft (leverfunctiestoornis of leverfalen) (zie "Wanneer mag u RAXAR niet gebruiken").
- Als u oraal ketoconazol (voor de behandeling van infecties veroorzaakt door microscopische schimmels) of orale erytromycine (een antibioticum) gebruikt, neem dit geneesmiddel dan niet in zonder eerst met uw arts te overleggen (zie "Gebruikt u nog andere geneesmiddelen?"
- Als u nierproblemen heeft (nierfunctiestoornis of nierfalen). Vraag uw arts om advies in geval van langdurige behandeling, aangezien u mogelijk een lagere dosis van dit geneesmiddel moet innemen of dit geneesmiddel minder vaak moet gebruiken en uw arts u misschien regelmatig wil bezoeken.
- Domperidon kan in verband worden gebracht met een verhoogd risico op hartritmestoornissen en hartstilstand. Dit risico kan groter zijn bij patiënten ouder dan 60 jaar of die doses van meer dan 30 mg per dag gebruiken. Het risico neemt ook toe wanneer domperidon samen met andere geneesmiddelen wordt gegeven. Vertel het uw arts of apotheker als u geneesmiddelen gebruikt om infecties (schimmelinfecties of bacteriële infecties) te behandelen en/of als u hartproblemen of aids/hiv heeft (zie rubriek Gebruikt u nog andere geneesmiddelen en RAXAR).
Domperidon dient bij volwassenen en kinderen in de laagste effectieve dosis te worden gebruikt.
- Het gebruik van domperidon en andere medicijnen die de QTc-intervallen verlengen, vereist voorzichtigheid bij patiënten met een bestaande verlenging van het hartgeleidingsinterval, met name QTc, patiënten met significante elektrolytafwijkingen of onderliggende hartaandoeningen zoals congestief hartfalen.
- In zeldzame gevallen kan het ernstige overgevoeligheidsreacties en bronchospasmen veroorzaken. Neem tijdens het gebruik van domperidon contact op met uw arts als u hartritmestoornissen opmerkt, zoals hartkloppingen, ademhalingsmoeilijkheden, flauwvallen.In dit geval moet de behandeling met domperidon worden stopgezet.
Interacties Welke medicijnen of voedingsmiddelen kunnen het effect van Raxar . veranderen?
Gebruik RAXAR niet als u geneesmiddelen gebruikt voor de behandeling van:
- schimmelinfecties, bijvoorbeeld azol-antischimmelmiddelen, vooral oraal ketoconazol, fluconazol of voriconazol
- bacteriële infecties, vooral erytromycine, claritromycine, telithromycine, moxifloxacine, pentamidine (deze geneesmiddelen zijn antibiotica)
- hartproblemen of hoge bloeddruk (bijv. amiodaron, dronedarone, kinidine, disopyramide, dofetilide, sotalol, diltiazem, verapamil)
- psychose (bijv. haloperidol, pimozide, sertindol)
- depressie (bijv. citalopram, escitalopram)
- gastro-intestinale stoornissen (bijv. cisapride, dolasetron, prucalopride)
- allergie (bijv. mechitazine, mizolastine)
- malaria (vooral halofantrine)
- AIDS / HIV (proteaseremmers)
- tumoren (bijv. toremifen, vandetanib, vincamine)
Vertel het uw arts of apotheker als u medicijnen gebruikt om infecties, hartaandoeningen of aids/hiv te behandelen.
Het is belangrijk om uw arts of apotheker te vragen of RAXAR veilig voor u is tijdens het gebruik van andere geneesmiddelen, waaronder geneesmiddelen zonder recept.
Waarschuwingen Het is belangrijk om te weten dat:
Zwangerschap
Als voorzorgsmaatregel heeft het de voorkeur om het gebruik van RAXAR 10 mg tijdens het eerste trimester van de zwangerschap te vermijden. Overweeg indien nodig het gebruik van domperidon tijdens het tweede en derde trimester van de zwangerschap. Als het geneesmiddel tijdens de zwangerschap wordt voorgeschreven, zorg er dan voor dat u uw instructies van de arts zorgvuldig door.
Als u tijdens de behandeling zwanger wordt, vertel dit dan aan uw arts, die zal beslissen of u de behandeling voortzet.
Borstvoeding
Er zijn kleine hoeveelheden domperidon aangetroffen in de moedermelk. Domperidon kan bijwerkingen veroorzaken op het hart van de baby die borstvoeding krijgt. Domperidon mag alleen worden gebruikt tijdens het geven van borstvoeding als uw arts dit strikt noodzakelijk acht.Vraag uw arts om advies voordat u dit geneesmiddel inneemt.
Rijvaardigheid en het gebruik van machines:
Het geneesmiddel heeft geen of een verwaarloosbare invloed op de rijvaardigheid of het vermogen om machines te bedienen.
Belangrijke informatie over enkele bestanddelen van RAXAR 10 mg, orodispergeerbare tabletten: glucose, zwaveldioxide (E220).
Dosis, wijze en tijdstip van toediening Hoe Raxar te gebruiken: Dosering
Volg deze instructies strikt op, tenzij uw arts u andere instructies heeft gegeven.
Duur van de behandeling:
Symptomen verdwijnen gewoonlijk binnen 3-4 dagen na inname van dit geneesmiddel.Gebruik RAXAR niet langer dan 7 dagen zonder uw arts te raadplegen.
Volwassenen en adolescenten van 12 jaar en ouder die 35 kg of meer wegen: De gebruikelijke dosering is driemaal daags één tablet, bij voorkeur vóór de maaltijd.
Neem niet meer dan drie tabletten per dag.
De orodispergeerbare tablet is niet geschikt voor kinderen die minder dan 35 kg wegen.
Kinderen moeten worden behandeld met de orale suspensie.
Wijze van toediening
Oraal gebruik.
De orodispergeerbare tablet lost snel op met speeksel in de mond en kan zonder water worden ingenomen.
Laat de tablet in uw mond oplossen zonder erop te kauwen.
De tabletten kunnen ook worden opgelost in een half glas water door ze vlak voor toediening te schudden.
De tabletten moeten voor de maaltijd worden ingenomen. Als de tablet na de maaltijd wordt ingenomen, kan de opname in het lichaam worden vertraagd.
Leverfunctiestoornis:
Gecontra-indiceerd bij matige of ernstige leverinsufficiëntie. In geval van een lichte leverfunctiestoornis is geen dosisaanpassing vereist.
Nierfunctiestoornis
In geval van nierinsufficiëntie kan het nodig zijn de frequentie en dosis van de toediening te verlagen. Cardiovasculair effect Vanwege cardiovasculaire effecten dient domperidon in een minimale effectieve dosis te worden gebruikt. Voorzichtigheid is geboden bij patiënten met een reeds bestaande verlenging van het hartgeleidingsinterval, significante stoornissen of een onderliggende hartziekte.
Overdosering Wat moet u doen als u te veel Raxar heeft ingenomen?
Als u te veel RAXAR heeft ingenomen, neem dan onmiddellijk contact op met uw arts, apotheker of het dichtstbijzijnde antigifcentrum, vooral als een kind te veel heeft ingenomen. In het geval van een overdosis kan een symptomatische behandeling worden toegepast. Echocardiografische monitoring kan worden uitgevoerd, gezien de mogelijkheid van een hartprobleem dat QT-verlenging wordt genoemd.
Wat u moet doen wanneer u bent vergeten RAXAR 10 mg orodispergeerbare tabletten in te nemen:
Neem het geneesmiddel in zodra u eraan denkt. Als het bijna tijd is voor uw volgende dosis, wacht dan tot uw volgende dosis en ga dan verder zoals u gewend bent.Neem geen dubbele dosis om een vergeten dosis in te halen.
Bijwerkingen Wat zijn de bijwerkingen van Raxar
Zoals alle geneesmiddelen kunnen RAXAR 10 mg, orodispergeerbare tabletten bijwerkingen hebben, al krijgt niet iedereen daarmee te maken.
Zeer vaak: komt voor bij meer dan 1 op de 10 patiënten
Vaak: komt voor bij 1 tot 10 op de 100 patiënten
Soms: treft 1 tot 10 gebruikers op 1.000
Zelden: treft 1 tot 10 gebruikers op 10.000
Zeer zelden: komt voor bij minder dan 1 op de 10.000 patiënten
Niet bekend: frequentie kan met de beschikbare gegevens niet worden bepaald
Erg zeldzaam:
- Immuunsysteemaandoeningen: allergische reacties (bijv.huiduitslag, jeuk, kortademigheid, piepende ademhaling en/of gezwollen gezicht). Als dit gebeurt, stop dan onmiddellijk met de behandeling en raadpleeg onmiddellijk uw arts of apotheker.
- Zenuwstelselaandoeningen: Convulsies, slaperigheid, hoofdpijn, abnormale spierbewegingen of tremoren (trillen) kunnen optreden. Het begin van abnormale spierbewegingen is van groter belang wanneer het voorkomt bij pasgeborenen en zuigelingen.
- Psychische stoornissen: agitatie, nervositeit
- Onderzoeken: leverfunctietest abnormaal
- Diarree.
Bijzonder:
- Verhoogde niveaus van prolactine (hormoon dat de melkstroom induceert), galactorroe (uitscheiding van melk buiten de borstvoedingsperioden), gynaecomastie (abnormale borstontwikkeling bij mannen), amenorroe (onregelmatige of afwezige menstruatie), gastro-intestinale stoornissen waaronder zeer zeldzame en voorbijgaande manifestaties van spier krampen.
Aangezien RAXAR 10 mg orodispergeerbare tablet zwaveldioxide (E220) bevat, bestaat er in zeldzame gevallen een risico op ernstige allergische reacties en ademhalingsproblemen.
Niet bekend (frequentie kan met de beschikbare gegevens niet worden bepaald):
- Hartaandoeningen: hartritmestoornissen, plotselinge dood
Cardiovasculaire systeemaandoeningen zijn gemeld: hartritmestoornissen (snel of onregelmatig hartritme); bij dergelijke klachten moet u de behandeling onmiddellijk stopzetten. Domperidon kan in verband worden gebracht met een verhoogd risico op hartritmestoornissen en hartstilstand. Dit risico kan groter zijn bij patiënten ouder dan 60 jaar of die doses van meer dan 30 mg per dag gebruiken. Domperidon dient bij volwassenen en kinderen in de laagste effectieve dosering te worden gebruikt.
Melding van bijwerkingen
Krijgt u last van bijwerkingen, neem dan contact op met uw arts of apotheker.Dit geldt ook voor mogelijke bijwerkingen die niet in deze bijsluiter staan. U kunt bijwerkingen ook rechtstreeks melden via het nationale meldsysteem op https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse
Door bijwerkingen te melden, kunt u ons helpen meer informatie te verkrijgen over de veiligheid van dit geneesmiddel.
Vervaldatum en retentie
Buiten het zicht en bereik van kinderen houden.
Niet gebruiken na de vervaldatum die staat vermeld op de verpakking na EXP. De vervaldatum verwijst naar de laatste dag van die maand.
Niet bewaren boven 30°C. Houd de blister goed gesloten ter bescherming tegen vocht.
Gooi geneesmiddelen niet weg via het afvalwater of met het huisvuil.Vraag uw apotheker wat u met geneesmiddelen moet doen die u niet meer gebruikt.Dit helpt het milieu te beschermen.
Wat bevat RAXAR 10, orodispergeerbare tabletten:
Het actieve ingrediënt is domperidon
Eén orodispergeerbare tablet bevat 10 mg domperidon.
De andere ingrediënten zijn:
Microkristallijne cellulose, crospovidon, citroensmaak*, magnesiumstearaat, natriumsacharine, natriumlaurylsulfaat, watervrij hydrofoob colloïdaal silica. * citroensmaak: maltodextrine (bron van glucose), arabische gom, gebutyleerd hydroxyanisol, zwaveldioxide (E220), alfa-pineen, beta-pineen, myrceen, limoneen, gamma-terpineen, neral en geranial.
Hoe ziet RAXAR 10 mg orodispergeerbare tablet eruit en wat is de inhoud van de verpakking:
RAXAR 10 mg orodispergeerbare tabletten zijn witte tot gebroken witte, ronde en biconvexe orodispergeerbare tabletten.
Het is verkrijgbaar in verpakkingen van 10, 20, 30, 40, 60 en 100 tabletten. Mogelijk worden niet alle verpakkingsgrootten in de handel gebracht.
Bron Bijsluiter: AIFA (Italiaans Geneesmiddelenbureau). Inhoud gepubliceerd in januari 2016. De aanwezige informatie is mogelijk niet up-to-date.
Om toegang te hebben tot de meest actuele versie, is het raadzaam om de website van AIFA (Italian Medicines Agency) te bezoeken. Disclaimer en nuttige informatie.
01.0 NAAM VAN HET GENEESMIDDEL
RAXAR 10 MG GOUD DISPERGEERBARE TABLETTEN
▼ Geneesmiddel onderworpen aan aanvullende monitoring. Dit zal de snelle identificatie van nieuwe veiligheidsinformatie mogelijk maken. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden. Zie rubriek 4.8 voor informatie over het melden van bijwerkingen.
02.0 KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
Eén orodispergeerbare tablet bevat 10 mg domperidon.
Hulpstoffen: glucose, zwaveldioxide (E 220).
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1.
03.0 FARMACEUTISCHE VORM
Orodispergeerbare tablet.
Witte of bijna witte, ronde, biconvexe tablet.
04.0 KLINISCHE INFORMATIE
04.1 Therapeutische indicaties
RAXAR is geïndiceerd om de symptomen van misselijkheid en braken te verlichten.
04.2 Dosering en wijze van toediening
Het verdient de voorkeur dat kinderen worden behandeld met de orale suspensie.
RAXAR moet worden gebruikt in de laagste effectieve dosis voor de kortst mogelijke duur om misselijkheid en braken onder controle te houden.
Het wordt aanbevolen om RAXAR oraal in te nemen vóór de maaltijd. Als het na de maaltijd wordt ingenomen, is de absorptie van het medicijn nogal vertraagd.
Patiënten moeten proberen elke dosis op het juiste tijdstip in te nemen.Als een dosis wordt gemist, moet deze worden overgeslagen en moet het gebruikelijke doseringsschema worden hervat. Er mag geen dubbele dosis worden ingenomen om een vergeten dosis in te halen.
In de regel mag de maximale behandelingsduur niet langer zijn dan een week.
Volwassenen en adolescenten (12 jaar of ouder en 35 kg of meer)
Eén tablet van 10 mg tot driemaal daags voor een maximale dosis van 30 mg per dag.
De orodispergeerbare tablet lost snel op in de mond met behulp van speeksel en kan met of zonder water worden ingenomen. Indien ingenomen zonder water, moet de tablet op de tong worden gelegd en in de mond worden opgelost voordat deze wordt doorgeslikt. Indien van toepassing kan deze worden gedronken later een glas water.
De orodispergeerbare tablet kan ook worden opgelost door hem vlak voor toediening in een half glas water te schudden.
leverfunctiestoornis
RAXAR is gecontra-indiceerd bij matige en ernstige leverinsufficiëntie (zie rubriek 4.3). Bij een lichte leverfunctiestoornis is echter geen dosisaanpassing nodig (zie rubriek 5.2).
Nierfunctiestoornis
Aangezien de halfwaardetijd van domperidon verlengd is bij ernstige nierinsufficiëntie, dient bij herhaalde toediening de frequentie van toediening van RAXAR te worden verlaagd tot een- of tweemaal daags, afhankelijk van de ernst van de nierinsufficiëntie, en de ernst van de nierinsufficiëntie moet mogelijk worden Dergelijke patiënten die langdurig worden behandeld, moeten regelmatig worden gecontroleerd (zie rubrieken 4.4 en 5.2).
Vanwege cardiovasculaire effecten dient domperidon in de laagste effectieve dosis te worden gebruikt. Bij patiënten met bestaande verlenging van het hartgeleidingsinterval, significante stoornissen of onderliggende hartziekte is voorzichtigheid geboden (zie rubriek 4.4).
04.3 Contra-indicaties
Dit geneesmiddel is gecontra-indiceerd in de volgende situaties:
• Bekende overgevoeligheid voor domperidon of voor één van de hulpstoffen.
• Prolactine-afgevende hypofysetumoren (prolactinomen).
• Bij patiënten met een matige of ernstige leverfunctiestoornis (zie rubriek 5.2).
• Bij patiënten met een bekende verlenging van de hartgeleidingsintervallen, met name het QTc-interval, bij patiënten met significante elektrolytenstoornissen en een reeds bestaande hartaandoening, bijv. congestief hartfalen (zie rubriek 4.4).
• Gelijktijdige toediening van alle geneesmiddelen die het QT-interval verlengen (zie rubriek 4.5).
• Gelijktijdige toediening van krachtige CYP3A4-remmers (ongeacht hun effecten op de verlenging van het QT-interval) (zie rubriek 4.5).
Dit geneesmiddel mag niet worden gebruikt in gevallen waarin stimulatie van de maagmotiliteit schadelijk kan zijn: gastro-intestinale bloeding, mechanische obstructie of darmperforatie.
04.4 Bijzondere waarschuwingen en passende voorzorgen bij gebruik
Nierfunctiestoornis
De eliminatiehalfwaardetijd van domperidon is verlengd bij ernstige nierinsufficiëntie.In geval van herhaalde toediening moet de doseringsfrequentie van domperidon worden verlaagd tot één- of tweemaal daags, afhankelijk van de ernst van de stoornis.
Inname met krachtige CYP3-remmers A4
Gelijktijdige toediening met orale ketoconazol, erytromycine of andere krachtige remmers van CYP3 A4 die het QTc-interval verlengen, moet worden vermeden (zie rubriek 4.5 Interacties met andere geneesmiddelen en andere vormen van interactie).
Patiënten met zeldzame erfelijke aandoeningen van galactose-intolerantie, bijv. galactosemie of glucose-galactose malabsorptie mag dit geneesmiddel niet gebruiken.
Cardiovasculaire effecten
Domperidon is in verband gebracht met verlenging van het QT-interval op het elektrocardiogram. Tijdens postmarketingsurveillance zijn zeer zeldzame gevallen van verlenging van het QT-interval gevonden wendingen van punt bij patiënten die domperidon gebruiken. Dergelijke gevallen omvatten patiënten met verstorende risicofactoren, elektrolytstoornissen en gelijktijdige behandeling die mogelijk bijdragende factoren waren (zie rubriek 4.8).
Epidemiologische onderzoeken hebben aangetoond dat domperidon in verband werd gebracht met een verhoogd risico op ernstige ventriculaire aritmieën of plotselinge hartdood (zie rubriek 4.8). Een verhoogd risico is waargenomen bij patiënten ouder dan 60 jaar, bij patiënten die een dagelijkse dosis van meer dan 30 mg gebruiken en bij patiënten die gelijktijdig QT-verlengende geneesmiddelen of CYP3A4-remmers gebruiken.
Domperidon dient bij volwassenen en kinderen in de laagste effectieve dosis te worden gebruikt.
Domperidon is gecontra-indiceerd bij patiënten met bekende bestaande verlenging van de hartgeleidingsintervallen, met name het QTc-interval, bij patiënten met significante elektrolytstoornissen (hypocalciëmie, hypercalciëmie, hypomagnesiëmie) of bradycardie, of bij patiënten met een reeds bestaande hartaandoening zoals insufficiëntie congestief hart vanwege het verhoogde risico op ventriculaire aritmie (zie rubriek 4.3).
Het is bekend dat elektrolytenstoornissen (hypocalciëmie, hypercalciëmie, hypomagnesiëmie) of bradycardie aandoeningen zijn die het pro-aritmische risico verhogen.
De behandeling met domperidon dient te worden gestaakt bij tekenen of symptomen die verband houden met hartritmestoornissen en patiënten dienen hun arts te raadplegen.
Patiënten moeten worden geadviseerd om hartsymptomen onmiddellijk te melden.
04.5 Interacties met andere geneesmiddelen en andere vormen van interactie
Domperidon wordt voornamelijk gemetaboliseerd door CYP3A4.
Gegevens uit in vitro-onderzoeken suggereren dat gelijktijdig gebruik van geneesmiddelen die CYP3 A4 significant remmen, kan leiden tot verhoogde plasmaspiegels van domperidon.
Verhoogd risico op verlenging van het QT-interval als gevolg van farmacodynamische en/of farmacokinetische interacties.
Gelijktijdige inname van de volgende stoffen is gecontra-indiceerd:
Geneesmiddelen die het QTc-interval verlengen
• klasse IA anti-aritmica (bijv. disopyramide, hydrokinidine, kinidine)
• klasse III anti-aritmica (bijv. amiodaron, dofetilide, dronedarone, ibutilide, sotalol)
• sommige antipsychotica (bijv. haloperidol, pimozide, sertindol)
• sommige antidepressiva (bijv. citalopram, escitalopram)
• sommige antibiotica (bijvoorbeeld erytromycine, levofloxacine, moxifloxacine, spiramycine)
• sommige antischimmelmiddelen (bijv. pentamidine)
• sommige antimalariamiddelen (met name halofantrine, lumefantrine)
• sommige maagdarmmedicijnen (bijv. cisapride, dolasetron, prucalopride)
• sommige antihistaminica (bijv. mechitazine, mizolastine)
• sommige geneesmiddelen die worden gebruikt bij de behandeling van kanker (bijvoorbeeld toremifen, vandetanib, vincamine)
• sommige andere geneesmiddelen (bijv. bepridil, difemanil, methadon) (zie rubriek 4.3).
Krachtige CYP3A4-remmers (ongeacht hun QT-verlengende effecten), bijvoorbeeld:
• proteaseremmers
• systemische azol-antischimmelmiddelen
• sommige macroliden (erytromycine, claritromycine en telithromycine) (zie rubriek 4.3).
Gelijktijdig gebruik van de volgende stoffen wordt niet aanbevolen
Matige remmers van CYP3A4, bijv. diltiazem, verapamil en sommige macroliden. (zie paragraaf 4.3)
De gelijktijdige inname van de volgende stoffen vereist voorzichtigheid bij het gebruik:
Voorzichtigheid is geboden in het geval van geneesmiddelen die bradycardie en hypocalciëmie induceren, evenals met de volgende macroliden die betrokken zijn bij verlenging van het QT-interval: azitromycine en roxitromycine (claritromycine is gecontra-indiceerd omdat het een krachtige remmer van CYP3A4) is.
Bovenstaande lijst van stoffen is indicatief en niet uitputtend.
04.6 Zwangerschap en borstvoeding
Zwangerschap :
Er zijn beperkte gegevens over het gebruik van domperidon bij zwangere vrouwen; er zijn geen risico's voor het embryo, de foetus of de pasgeborene vastgesteld na blootstelling aan domperidon tijdens de zwangerschap.
Studies bij één diersoort hebben reproductietoxiciteit aangetoond die geassocieerd is met maternale toxiciteit na toediening van zeer hoge doses (zie rubriek 5.3).
Als voorzorgsmaatregel heeft het de voorkeur om het gebruik van domperidon tijdens het eerste trimester van de zwangerschap te vermijden. Indien nodig kan het gebruik van domperidon tijdens het tweede en derde trimester van de zwangerschap worden overwogen.
Borstvoeding
Domperidon wordt uitgescheiden in de moedermelk en zuigelingen die borstvoeding krijgen, krijgen minder dan 0,1% van de dosis aangepast aan het gewicht van de moeder. Het optreden van bijwerkingen, met name cardiale effecten, kan niet worden uitgesloten na blootstelling via de moedermelk.In dit geval moet worden besloten of de borstvoeding moet worden gestaakt of dat de behandeling met domperidon moet worden gestaakt/beëindigd door de voordelen van borstvoeding voor de zuigeling te evalueren en de voordelen van therapie voor de moeder Voorzichtigheid is geboden in geval van risicofactoren die het QTc-interval verlengen bij zuigelingen die borstvoeding krijgen.
04.7 Beïnvloeding van de rijvaardigheid en het vermogen om machines te bedienen
Het geneesmiddel heeft geen of een verwaarloosbare invloed op de rijvaardigheid of het vermogen om machines te bedienen.
04.8 Bijwerkingen
Bijwerkingen zijn hieronder gerangschikt naar frequentie met gebruikmaking van de volgende conventie: zeer vaak (≥1/10); gemeenschappelijk (≥1 / 100,
1 Domperidon kan verhoogde prolactinespiegels veroorzaken omdat de hypofyse zich buiten de bloed-hersenbarrière bevindt.
In zeldzame gevallen kan deze hyperprolactinemie neuro-endocriene bijwerkingen veroorzaken, zoals galactorroe, gynaecomastie en amenorroe.
2 Extrapiramidale bijwerkingen zijn zeer zeldzaam bij zuigelingen en jonge kinderen en uitzonderlijk bij volwassenen.
Deze effecten verdwijnen spontaan en volledig bij stopzetting van de behandeling.
3 Andere aan het centrale zenuwstelsel gerelateerde effecten zoals convulsies, opwinding en slaperigheid zijn zeer zeldzaam en zijn voornamelijk gemeld bij zuigelingen en kinderen.
Door de aanwezigheid van zwaveldioxide (E220) bestaat het risico dat in zeldzame gevallen overgevoeligheidsreacties en bronchospasmen optreden.
Melding van vermoedelijke bijwerkingen
Het melden van vermoedelijke bijwerkingen die optreden na toelating van het geneesmiddel is belangrijk omdat het een continue monitoring van de baten/risicoverhouding van het geneesmiddel mogelijk maakt. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via het nationale meldsysteem. "adres https: //www.aifa.gov.it/content/segnalazioni-reazioni-avverse.
04.9 Overdosering
Symptomen
Gevallen van overdosering zijn voornamelijk gemeld bij zuigelingen en kinderen. Symptomen van overdosering kunnen zijn: agitatie, veranderingen in bewustzijn, toevallen, desoriëntatie, slaperigheid en extrapiramidale manifestaties.
Behandeling
Er is geen specifiek antidotum voor domperidon. In het geval van een overdosis moet onmiddellijk een standaard symptomatische behandeling worden gegeven. ECG-bewaking moet worden uitgevoerd vanwege de mogelijkheid van verlenging van het QT-interval.
Maagspoeling en het gebruik van actieve kool kunnen nuttig zijn.
Anticholinergica en antiparkinsongeneesmiddelen kunnen nuttig zijn bij het beheersen van extrapiramidale reacties.
05.0 FARMACOLOGISCHE EIGENSCHAPPEN
05.1 Farmacodynamische eigenschappen
Farmacotherapeutische categorie: prokinetiek.
ATC-code: A03F A 03.
Domperidon is een dopamine-antagonist met anti-emetische eigenschappen, die niet gemakkelijk de bloed-hersenbarrière passeert.
Bij patiënten die met domperidon worden behandeld, vooral bij volwassenen, zijn extrapiramidale bijwerkingen zeer zeldzaam, maar domperidon bevordert de afgifte van prolactine uit de hypofyse.Het anti-emetische effect van domperidon kan het gevolg zijn van de combinatie van perifere (gastrokinetische) effecten en antagonisme van dopaminerge receptoren in de "chemoreceptor-triggerzone", die zich buiten de bloed-hersenbarrière in het postrema-gebied bevindt. Dierstudies wijzen, volgens de lage concentraties die in de hersenen worden gevonden, op een overwegend perifeer effect van domperidon op dopaminerge receptoren.
Studies bij mensen hebben aangetoond dat oraal domperidon de druk van de lagere slokdarmsfincter verhoogt, de anthroduodenale motiliteit verbetert en de maaglediging versnelt.Het heeft geen effect op de maagsecretie.
Een grondig QT-intervalonderzoek werd uitgevoerd in overeenstemming met de ICH-E14-richtlijnen. Dit onderzoek omvatte een placebo, een actieve comparator en een positieve controle en werd uitgevoerd bij gezonde proefpersonen met een domperidondosering tot 80 mg per dag in doses van 10 of 20 mg 4 keer per dag toegediend. Deze studie identificeerde een maximaal verschil in gecorrigeerd QT-interval (QTc) tussen domperidon en placebo in LS-gemiddelde (kleinste kwadraten) in de verandering ten opzichte van baseline van 3,4 msec voor 20 mg domperidon 4 keer per dag toegediend op dag 4. Het bidirectionele betrouwbaarheidsinterval van 90% (1,0 tot 5,9 msec) was niet langer dan 10 msec. In dit onderzoek werden geen relevante effecten op het QTc-interval waargenomen. wanneer domperidon werd gegeven in een dosis tot 80 mg/ dag (bijv. meer dan tweemaal de maximaal aanbevolen dosis).
Twee eerdere onderzoeken naar geneesmiddelinteracties hebben echter aanwijzingen opgeleverd voor verlenging van het QTc-interval wanneer domperidon als monotherapie werd gegeven (10 mg 4 maal daags).
Het maximale met de tijd overeenkomende gemiddelde verschil in het door Fridericia gecorrigeerde QT-interval (QTcF) tussen domperidon en placebo was respectievelijk 5,4 msec (95% BI: -1,7 tot 12,4) en 7,5 msec (95 BI). %: 0,6 tot 14,4).
05.2 "Farmacokinetische eigenschappen
Absorptie
Domperidon wordt snel geabsorbeerd na orale toediening, met piekplasmaconcentraties die ongeveer 1 uur na toediening optreden. De Cmax- en AUC-waarden van domperidon namen proportioneel toe met doses variërend van 10 mg tot 20 mg. Een 2- of 3-voudige accumulatie van de AUC van domperidon werd waargenomen bij herhaalde toediening van viermaal daags (elke 5 uur) domperidon gedurende 4 dagen.
Hoewel de biologische beschikbaarheid van domperidon verhoogd is bij gezonde proefpersonen wanneer het na een maaltijd wordt ingenomen, dienen patiënten met gastro-intestinale stoornissen het geneesmiddel 15-30 minuten voor een maaltijd in te nemen. Verminderde maagzuurgraad verslechtert de absorptie van domperidon Orale biologische beschikbaarheid wordt verminderd door eerdere gelijktijdige toediening van cimetidine en natriumbicarbonaat.
De tijd tot piekabsorptie is enigszins vertraagd en de AUC is enigszins verhoogd wanneer het geneesmiddel na een maaltijd oraal wordt ingenomen.
Verdeling
Oraal domperidon vertoont geen accumulatie- of metabolische zelfinductieverschijnselen; 90 minuten na toediening bleek een piekplasmaspiegel van 21 ng/ml, na twee weken orale toediening bij een dagelijkse dosis van 30 mg, bijna vergelijkbaar te zijn met die van 18 ng/ml verkregen na de eerste dosis. Domperidon is voor 91-93% gebonden aan plasma-eiwitten.
Distributiestudies bij dieren, uitgevoerd met radioactief gelabeld medicijn, toonden "brede weefseldistributie maar lage hersenconcentraties. Kleine hoeveelheden van het medicijn passeren de placenta bij ratten."
Metabolisme
Domperidon ondergaat een snel en uitgebreid levermetabolisme door hydroxylering en N-dealkylering. Metabolisme studies in vitro met diagnostische remmers geven aan dat CYP3A4 de vorm van cytochroom P-450 is die het meest betrokken is bij de N-dealkylering van domperidon, terwijl CYP3A4, CYP1A2 en CYP2E1 betrokken zijn bij de aromatische hydroxylering van domperidon.
uitscheiding
Urine- en fecale excretie bedragen respectievelijk 31% en 66% van de orale dosis.Het aandeel onveranderd geneesmiddel dat wordt uitgescheiden is klein (10% van de fecale excretie en ongeveer 1% van de urinaire excretie).
De plasmahalfwaardetijd na een enkelvoudige orale dosis is 7-9 uur bij gezonde vrijwilligers, maar is verlengd bij patiënten met ernstige nierinsufficiëntie.
leverfunctiestoornis
Bij proefpersonen met een matige leverfunctiestoornis (Pugh-score 7 tot 9, Child-Pugh-classificatie B) zijn de AUC en Cmax van domperidon respectievelijk 2,9 en 1,5 keer hoger dan bij gezonde proefpersonen.
De ongebonden fractie wordt met 25% verhoogd en de terminale eliminatiehalfwaardetijd wordt verlengd van 15 tot 23 uur.Proefpersonen met een lichte leverfunctiestoornis hebben een iets lagere systemische blootstelling dan gezonde proefpersonen op basis van Cmax- en AUC-waarden, zonder veranderingen in eiwitbinding of terminale halfwaardetijd Proefpersonen met een ernstige leverfunctiestoornis zijn niet onderzocht Domperidon is gecontra-indiceerd bij patiënten met een matige of ernstige leverfunctiestoornis (zie rubriek 4.3).
Nierfunctiestoornis
Bij proefpersonen met een ernstige nierfunctiestoornis (creatinineklaring 2) nam de eliminatiehalfwaardetijd van domperidon toe van 7,4 tot 20,8 uur, maar de plasmaspiegels van het geneesmiddel waren lager dan bij gezonde vrijwilligers.
Aangezien een zeer kleine hoeveelheid onveranderd geneesmiddel via de nieren wordt uitgescheiden (ongeveer 1%), is het onwaarschijnlijk dat de dosis van een eenmalige toediening moet worden aangepast bij patiënten met nierinsufficiëntie.
In geval van herhaalde toediening moet de doseringsfrequentie echter worden verlaagd tot een- of tweemaal daags, afhankelijk van de ernst van de aandoening en moet de dosering mogelijk worden verlaagd.
05.3 Gegevens uit het preklinisch veiligheidsonderzoek
Elektrofysiologische studies in vitro En in vivo wijzen op een matig algemeen risico op verlenging van het QTc-interval bij mensen voor domperidon. In in vitro-experimenten op geïsoleerde cellen die zijn getransfecteerd met hERG en op geïsoleerde myocyten van cavia's, varieerden de blootstellingsratio's van 26 tot 47 keer, gebaseerd op IC50-waarden die stromen door IKr-ionkanalen remmen in vergelijking met vrije plasmaconcentraties in de "menselijke na toediening van de maximale dagelijkse dosis van 10 mg, driemaal per dag toegediend De veiligheidsmarges voor verlenging van de duur van de actiepotentiaal in in vitro experimenten op geïsoleerde hartweefsels waren 45 keer hoger dan de vrije plasmaconcentraties in "menselijke bij de maximale dagelijkse dosis (10 mg 3 maal per dag toegediend) De veiligheidsmarges in pro-aritmische modellen in vitro (geïsoleerd hart en geperfuseerde Langendorff) waren 9 tot 45 keer hoger dan de vrije plasmaconcentraties bij mensen bij maximale dagelijkse dosis (10 mg toegediend 3 maal per dag). keer per dag). In modellen in vivo geen effect-niveaus voor verlengd gecorrigeerd QT-interval (QTc) bij honden en inductie van aritmieën in een konijnenmodel dat gesensibiliseerd was voor torsades de pointes, waren respectievelijk meer dan 22-voudig en 435-voudig boven de vrije plasmaconcentraties bij de maximale dagelijkse dosis (10 mg 3 maal daags toegediend) In het model met verdoofde cavia na intraveneuze infusies was er geen effect op het gecorrigeerde QT-interval (QTc) bij totale plasmaconcentraties van 45,4 ng/ml, die 3 keer hoger zijn dan de totale plasmaspiegels bij mensen bij de maximale dagelijkse dosis (10 mg driemaal daags toegediend) De relevantie van dit laatste onderzoek voor mensen na blootstelling aan oraal toegediend domperidon is onzeker.
In aanwezigheid van remming van het metabolisme door CYP3A4 kunnen de vrije plasmaconcentraties van domperidon verdrievoudigen.
Bij een hoge maternaal toxische dosering (meer dan 40 maal de aanbevolen dosis voor de mens) werden teratogene effecten waargenomen bij ratten. Er werd geen teratogeniteit waargenomen bij muizen en konijnen.
06.0 FARMACEUTISCHE INFORMATIE
06.1 Hulpstoffen
Microkristallijne cellulose, crospovidon, citroensmaak*, magnesiumstearaat, natriumsacharine, natriumlaurylsulfaat, watervrij hydrofoob colloïdaal silica.
* citroensmaak: maltodextrine (bron van glucose), arabische gom, gebutyleerd hydroxyanisol, zwaveldioxide (E220), alfa-pineen, beta-pineen, myrceen, limoneen, gamma-terpineen, neral en geranial.
06.2 Incompatibiliteit
Niet relevant.
06.3 Geldigheidsduur
3 jaar.
06.4 Speciale voorzorgsmaatregelen bij bewaren
Niet bewaren boven 30°C.
Houd de blister goed gesloten ter bescherming tegen vocht.
06.5 Aard van de primaire verpakking en inhoud van de verpakking
10, 20, 30, 40, 60 en 100 tabletten in blisterverpakkingen (PVC / PVDC / Aluminium).
Mogelijk worden niet alle verpakkingsgrootten in de handel gebracht.
06.6 Instructies voor gebruik en verwerking
Geen speciale instructies.
07.0 HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
CRINOS S.p.A., Via Pavia 6, 20136 Milaan
08.0 NUMMER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
RAXAR 10 mg orodispergeerbare tabletten, 10 tabletten in blisterverpakking PVC / PVDC / Al AIC N. 039200011
RAXAR 10 mg orodispergeerbare tabletten, 20 tabletten in PVC / PVDC / Al AIC blisterverpakking nr. 039200023
RAXAR 10 mg orodispergeerbare tabletten, 30 tabletten in PVC / PVDC / Al AIC N.039200035
RAXAR 10 mg orodispergeerbare tabletten, 40 tabletten in PVC / PVDC / Al AIC blisterverpakking nr. 039200047
RAXAR 10 mg orodispergeerbare tabletten, 60 tabletten in PVC / PVDC / Al AIC blisterverpakking nr. 039200050
RAXAR 10 mg orodispergeerbare tabletten, 100 tabletten in PVC / PVDC / Al AIC blisterverpakking nr. 039200062
09.0 DATUM VAN EERSTE VERGUNNING OF VERLENGING VAN DE VERGUNNING
20 november 2009/7 november 2012
10.0 DATUM VAN HERZIENING VAN DE TEKST
maart 2015