Actieve ingrediënten: Docetaxel
TAXOTERE 20 mg/0,5 ml concentraat en oplosmiddel voor oplossing voor infusie
Taxotere bijsluiters zijn beschikbaar voor verpakkingen:- TAXOTERE 20 mg/0,5 ml concentraat en oplosmiddel voor oplossing voor infusie
- TAXOTERE 80 mg / 2 ml concentraat en oplosmiddel voor oplossing voor infusie
- TAXOTERE 20 mg/1 ml concentraat voor oplossing voor infusie
- TAXOTERE 80 mg / 4 ml concentraat voor oplossing voor infusie
- TAXOTERE 160 mg / 8 ml concentraat voor oplossing voor infusie
Waarom wordt Taxotere gebruikt? Waar is het voor?
De naam van dit medicijn is TAXOTERE. De naam van het actieve ingrediënt is docetaxel.
Docetaxel is een stof die is afgeleid van de naaldachtige bladeren van de taxusplant en behoort tot de groep van kankerbestrijders die taxanen worden genoemd.
TAXOTERE is door uw arts voorgeschreven voor de behandeling van borstkanker, bepaalde vormen van longkanker (niet-kleincellige longkanker), prostaatkanker, maagkanker of hoofd-halskanker:
- Voor de behandeling van gevorderde borstkanker kan TAXOTERE alleen of in combinatie met doxorubicine, trastuzumab of capecitabine worden toegediend.
- Voor de behandeling van vroege borstkanker met of zonder betrokkenheid van de lymfeklieren, kan TAXOTERE worden toegediend in combinatie met doxorubicine en cyclofosfamide.
- Voor de behandeling van longkanker kan TAXOTERE alleen of in combinatie met cisplatine worden toegediend.
- voor de behandeling van prostaatkanker wordt TAXOTERE gegeven in combinatie met prednison of prednisolon.
- voor de behandeling van uitgezaaide maagkanker wordt TAXOTERE toegediend in combinatie met cisplatine en 5-fluorouracil.
- voor de behandeling van hoofd-halskanker wordt TAXOTERE gegeven in combinatie met cisplatine en 5-fluorouracil.
Contra-indicaties Wanneer Taxotere niet mag worden gebruikt
U mag TAXOTERE niet gebruiken
- als u allergisch (overgevoelig) bent voor docetaxel of voor één van de andere bestanddelen van Taxotere;
- als uw aantal witte bloedcellen te laag is;
- als u ernstige leverproblemen heeft;
Voorzorgen bij gebruik Wat u moet weten voordat u Taxotere inneemt
Voor elke behandeling met TAXOTERE is het noodzakelijk om de bloedtesten uit te voeren die nodig zijn om vast te stellen of er voldoende bloedcellen zijn en of de lever voldoende actief is.In het geval van veranderingen in de witte bloedcellen, kunnen ook koorts of infecties optreden.
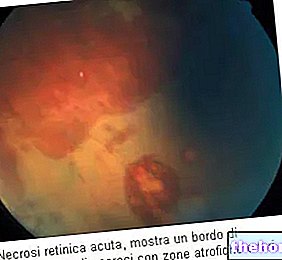
Vertel het uw arts, ziekenhuisapotheker of verpleegkundige als u problemen met uw gezichtsvermogen heeft Als u problemen heeft met uw gezichtsvermogen, met name wazig zien, moet u onmiddellijk uw ogen en gezichtsvermogen laten controleren.
Als u acute longproblemen krijgt of als uw bestaande symptomen erger worden (koorts, kortademigheid of hoesten), vertel dit dan onmiddellijk aan uw arts, ziekenhuisapotheker of verpleegkundige.Uw arts kan de behandeling onmiddellijk stopzetten.
U wordt gevraagd om een dag voor de toediening van TAXOTERE een preventieve behandeling met orale corticosteroïden zoals dexamethason te nemen en daarna één of twee dagen door te gaan om sommige bijwerkingen te verminderen die kunnen optreden na een infusie van TAXOTERE, in het bijzonder allergische reacties en vochtretentie (zwelling van de handen, voeten, benen of gewichtstoename).
Tijdens de behandeling heeft u mogelijk medicijnen nodig om het aantal bloedcellen op peil te houden.
Interacties Welke medicijnen of voedingsmiddelen kunnen het effect van Taxotere veranderen
Vertel uw arts of ziekenhuisapotheker als u andere geneesmiddelen gebruikt of kort geleden heeft gebruikt. Dit geldt ook voor geneesmiddelen die u zonder voorschrift kunt krijgen. Dit is omdat TAXOTERE of andere geneesmiddelen mogelijk niet werken zoals verwacht en u meer vatbaar kunt zijn voor bijwerkingen.
Waarschuwingen Het is belangrijk om te weten dat:
Zwangerschap, borstvoeding en vruchtbaarheid
Vraag uw arts om advies voordat u een geneesmiddel inneemt.
TAXOTERE mag NIET worden toegediend als u zwanger bent, tenzij duidelijk aangegeven door uw arts.
U mag niet zwanger worden terwijl u met dit geneesmiddel wordt behandeld en u moet adequate anticonceptiemaatregelen nemen tijdens de behandeling omdat TAXOTERE gevaarlijk kan zijn voor de baby. Als u tijdens de behandeling zwanger wordt, informeer dan onmiddellijk uw arts. U mag geen borstvoeding geven tijdens het gebruik van TAXOTERE.
Als u een man bent die wordt behandeld met TAXOTERE, wordt aangeraden om zich niet voort te planten tijdens en tot 6 maanden na de behandeling en om vóór de behandeling te informeren naar de opslag van sperma, aangezien docetaxel de mannelijke vruchtbaarheid kan schaden.
Rijvaardigheid en het gebruik van machines:
Er is geen onderzoek gedaan naar de effecten op de rijvaardigheid en op het vermogen om machines te bedienen.
Dosering en wijze van gebruik Hoe gebruikt u Taxotere: Dosering
TAXOTERE wordt aan u toegediend door een beroepsbeoefenaar in de gezondheidszorg.
Gebruikelijke dosering:
De dosering is afhankelijk van uw gewicht en algemene gezondheidstoestand. Uw arts berekent uw lichaamsoppervlak in vierkante meters (m2) en bepaalt de dosis die u moet krijgen.
Wijze van toediening en wijze van toediening:
TAXOTERE zal aan u worden toegediend via intraveneuze infusie (intraveneus gebruik). De infusie duurt ongeveer 1 uur en vindt plaats in het ziekenhuis.
Frequentie van toediening:
De infusie zal normaal gesproken eenmaal per 3 weken aan u worden toegediend.
Uw arts kan de dosis en frequentie van toediening aanpassen in verband met uw bloedonderzoek, uw algemene toestand en uw reactie op TAXOTERE. Vertel het uw arts in het bijzonder als u diarree, een zere mond, gevoelloosheid, tintelingen of koorts heeft en laat de resultaten van uw bloedonderzoek zien. Met deze informatie kan hij beslissen of een dosisverlaging nodig is. Als u nog vragen heeft over het gebruik van dit geneesmiddel, raadpleeg dan uw arts of ziekenhuisapotheker.
Bijwerkingen Wat zijn de bijwerkingen van Taxotere
Zoals elk geneesmiddel kan ook dit geneesmiddel bijwerkingen hebben, al krijgt niet iedereen daarmee te maken.
Uw arts zal dit met u bespreken en de mogelijke risico's en voordelen van de behandeling uitleggen.
De meest gemelde bijwerkingen van alleen TAXOTERE zijn: verminderd aantal rode of witte bloedcellen, haaruitval, misselijkheid, braken, ontsteking in de mond, diarree en vermoeidheid
Als TAXOTERE aan u wordt gegeven in combinatie met andere chemotherapeutische middelen, kan de ernst van de bijwerkingen toenemen.
De volgende allergische reacties kunnen optreden tijdens de infusie in het ziekenhuis (kunnen voorkomen bij meer dan 1 op de 10 mensen):
- blozen, huidreacties, jeuk
- beklemd gevoel op de borst, moeite met ademhalen
- koorts of koude rillingen
- rugpijn
- lage druk
Er kunnen meer ernstige reacties optreden.
Uw toestand wordt tijdens de behandeling nauwlettend gevolgd door het ziekenhuispersoneel. Vertel het het ziekenhuispersoneel onmiddellijk als u een van deze effecten opmerkt.
De onderstaande bijwerkingen kunnen optreden in de tijd tussen twee TAXOTERE-infusies, en de frequentie kan variëren afhankelijk van de combinatiemedicatie die u gebruikt:
Zeer vaak (kan voorkomen bij meer dan 1 op de 10 mensen):
- infecties, verminderd aantal rode bloedcellen (bloedarmoede) of witte bloedcellen (de laatste zijn belangrijk bij het bestrijden van infecties) en bloedplaatjes
- koorts: in dit geval moet u uw arts onmiddellijk informeren
- allergische reacties zoals hierboven beschreven
- verlies van eetlust (anorexia)
- slapeloosheid
- gevoel van gevoelloosheid of tintelingen of pijn in de gewrichten of spieren
- hoofdpijn
- veranderde smaakzin
- ontsteking van het oog of toegenomen tranenvloed aan het oog
- zwelling veroorzaakt door onvoldoende lymfedrainage
- moeite met ademhalen
- verlies van slijm uit de neus; ontsteking van de keel en neus; hoest
- neusbloedingen
- ontsteking in de mond
- maagklachten waaronder misselijkheid, braken en diarree, constipatie
- buikpijn
- indigestie
- haaruitval (de haargroei keert in de meeste gevallen terug naar normaal)
- roodheid en zwelling van de handpalmen of voetzolen, wat vervelling van de huid kan veroorzaken (dit kan ook gebeuren op de armen, het gezicht of het lichaam)
- verandering in de kleur van de nagels, die kan loslaten
- spierpijn; rugpijn of botpijn
- veranderingen of afwezigheid van de menstruatie
- zwelling van de handen, voeten, benen
- vermoeidheid of griepsymptomen
- gewichtstoename of -verlies
Vaak (komen voor bij minder dan 1 op de 10 gebruikers):
- orale candidiasis
- uitdroging
- duizeligheid
- slechthorend
- verlaging van de bloeddruk; onregelmatige of snelle hartslag
- hartfalen
- oesofagitis
- droge mond
- moeite of pijn bij het slikken
- bloeding
- verhoogde leverenzymen (vandaar de noodzaak van regelmatige bloedtesten)
Soms (komen voor bij minder dan 1 op de 100 gebruikers):
- flauwvallen
- op de injectieplaats huidreacties, flebitis (ontsteking van de aderen) of zwelling
- ontsteking van de dikke darm, dunne darm; darmperforatie.
- vorming van bloedstolsels
Frequentie niet bekend:
- interstitiële longziekte (longontsteking die hoesten en ademhalingsmoeilijkheden kan veroorzaken. Longontsteking kan zich ook ontwikkelen wanneer behandeling met docetaxel gelijktijdig met radiotherapie wordt gegeven)
- longontsteking (longinfecties)
- longfibrose (littekens en verdikking in de longen die kortademigheid veroorzaken)
- wazig zien door zwelling van het netvlies in het oog (cystoïd macula-oedeem)
- daling van het natriumgehalte in het bloed.
Melding van bijwerkingen
Krijgt u last van bijwerkingen, neem dan contact op met uw arts, ziekenhuisapotheker of verpleegkundige.Dit geldt ook voor mogelijke bijwerkingen die niet in deze bijsluiter staan.U kunt bijwerkingen ook rechtstreeks melden via het nationale meldsysteem zoals vermeld in aanhangsel V*. Door bijwerkingen te melden, kunt u ons helpen meer informatie te verkrijgen over de veiligheid van dit geneesmiddel.
Vervaldatum en retentie
Buiten het zicht en bereik van kinderen houden.
Gebruik dit geneesmiddel niet meer na de uiterste houdbaarheidsdatum. Die is te vinden op de doos, blister en injectieflacon.
Niet bewaren boven 25°C of beneden 2°C.
Bewaar het geneesmiddel in de oorspronkelijke verpakking om het tegen direct licht te beschermen
De voorverdunde oplossing moet onmiddellijk na bereiding worden gebruikt, zelfs als de chemisch-fysische stabiliteit van deze oplossing is aangetoond gedurende een periode van 8 uur indien bewaard tussen + 2 ° C en + 8 ° C of bij kamertemperatuur (beneden 25 C ) .
De oplossing moet binnen 4 uur worden gebruikt indien bewaard bij kamertemperatuur (beneden 25°C).
Wat bevat de injectieflacon TAXOTERE concentraat:
Het werkzame bestanddeel is docetaxel (als trihydraat). Elke ml docetaxeloplossing bevat 40 mg docetaxel (watervrij). Eén injectieflacon bevat 20 mg/0,5 ml docetaxel. De andere stoffen in dit middel zijn polysorbaat 80 en citroenzuur.
Wat bevat de injectieflacon met oplosmiddel:
13% (w/w) 95% ethanol in water voor injecties.
Beschrijving van hoe TAXOTERE eruit ziet en de inhoud van de verpakking:
TAXOTERE 20 mg/0,5 ml concentraat voor oplossing voor infusie is een heldere, stroperige, gele tot geelbruine oplossing.
Elke verpakking bevat:
- een injectieflacon met een enkelvoudige dosis concentraat en,
- een injectieflacon met een enkele dosis oplosmiddel
De volgende informatie is alleen bedoeld voor beroepsbeoefenaren in de gezondheidszorg.
BEREIDINGSGIDS VOOR TAXOTERE 20 mg / 0,5 ml CONCENTRAAT VOOR OPLOSSING VOOR INFUSIE EN AANVERWANT OPLOSMIDDEL VOOR TAXOTERE
Het is belangrijk dat u de volledige inhoud van deze gids leest voordat u zowel de TAXOTERE voorverdunde oplossing als de TAXOTERE oplossing voor infusie bereidt.
1. FORMULERING
TAXOTERE 20 mg/0,5 ml concentraat voor oplossing voor infusie is een heldere, viskeuze gele tot geelbruine oplossing die 40 mg/ml docetaxel (watervrij) in polysorbaat 80 en citroenzuur bevat. Het TAXOTERE-oplosmiddel is een 13% (w/w) oplossing van 95% ethanol in water voor injecties.
2. PRESENTATIE
TAXOTERE wordt geleverd in injectieflacons voor eenmalig gebruik.
Elke verpakking bevat één injectieflacon TAXOTERE (20 mg/0,5 ml) en één injectieflacon met het overeenkomstige oplosmiddel voor TAXOTERE in blisterverpakkingen.
TAXOTERE injectieflacons moeten worden bewaard tussen + 2 ° C en + 25 ° C, beschermd tegen licht.
TAXOTERE mag niet worden gebruikt na de vervaldatum die staat vermeld op de doos, blister en injectieflacon.
2.1 Injectieflacons TAXOTERE 20 mg / 0,5 ml:
- De injectieflacon TAXOTERE 20 mg / 0,5 ml, heeft een inhoud van 7 ml, is gemaakt van helder glas met een verwijderbare groene dop.
- De injectieflacon TAXOTERE 20 mg/0,5 ml bevat een oplossing van docetaxel in polysorbaat 80 in een concentratie van 40 mg/ml.
- Elke injectieflacon TAXOTERE 20 mg / 0,5 ml bevat 0,5 ml 40 mg / ml oplossing van docetaxel in polysorbaat 80 (vulvolume: 24,4 mg / 0,61 ml). Deze overdosis werd vastgesteld tijdens de ontwikkeling van TAXOTERE om te compenseren voor het verlies van vloeistof tijdens de bereiding van de voorverdunde oplossing (zie rubriek 4) als gevolg van schuimvorming, hechting aan de flaconwanden en 'dode ruimte'. Deze overdosis zorgt ervoor dat na verdunning met de volledige inhoud van de flacon met oplosmiddel die is meegeleverd met TAXOTERE, het minimale extraheerbare volume van de voorverdunde oplossing is 2 ml, die 10 mg/ml docetaxel bevat, wat overeenkomt met de op het etiket vermelde inhoud van 20 mg/0,5 ml per injectieflacon.
2.2 Oplosmiddel voor TAXOTERE 20 mg / 0,5 ml injectieflacons:
- Het oplosmiddel voor TAXOTERE 20 mg/0,5 ml zit in een doorzichtige glazen injectieflacon van 7 ml met een doorzichtige flip-off dop.
- Het oplosmiddel voor TAXOTERE 20 mg/0,5 ml bestaat uit een 13% (w/w) oplossing van 95% ethanol in water voor injecties.
- Elke injectieflacon met oplosmiddel voor TAXOTERE 20 mg/0,5 ml bevat 1,98 ml oplossing. Dit volume werd berekend op basis van het werkelijke volume van de TAXOTERE 20 mg / 0,5 ml injectieflacons. Door de volledige inhoud van de injectieflacon met oplosmiddel toe te voegen aan die van TAXOTERE 20 mg / 0,5 ml, wordt een voorverdunde oplossing van 10 mg / ml docetaxel verkregen.
3. AANBEVELINGEN VOOR VEILIGE HANTERING
TAXOTERE is een antineoplastisch geneesmiddel en, net als bij andere potentieel toxische producten, is voorzichtigheid geboden bij het hanteren en bereiden van oplossingen. Het gebruik van handschoenen wordt aanbevolen.
Als TAXOTERE in geconcentreerde, voorverdunde vorm of oplossing voor infusie in contact komt met de huid, was dan onmiddellijk en grondig met water en zeep. Indien TAXOTERE in geconcentreerde, voorverdunde vorm of in oplossing voor infusie in contact komt met de slijmvliezen, onmiddellijk en grondig wassen met water.
4. VOORBEREIDING VOOR INTRAVENEUZE TOEDIENING
4.1 Bereiding van de voorverdunde oplossing van TAXOTERE (10 mg docetaxel / ml)
4.1.1 Als de injectieflacons in de koelkast worden bewaard, laat het vereiste aantal dozen TAXOTERE dan 5 minuten op kamertemperatuur (beneden 25°C).
4.1.2 Zuig met behulp van een maatspuit met naald aseptisch de volledige inhoud van de injectieflacon met oplosmiddel voor TAXOTERE op door de injectieflacon gedeeltelijk om te keren.
4.1.3 Injecteer de volledige inhoud van de spuit in de bijbehorende injectieflacon TAXOTERE
4.1.4 Verwijder de spuit en naald en meng de oplossing handmatig door deze gedurende 45 seconden herhaaldelijk om te keren.Niet schudden.
4.1.5 Laat de injectieflacon met voorverdunde oplossing 5 minuten staan bij kamertemperatuur (beneden 25°C) en controleer vervolgens of de oplossing helder en homogeen is (schuimvorming is normaal, zelfs na 5 minuten vanwege het polysorbaatgehalte 80 in de tekst) .
De voorverdunde oplossing bevat 10 mg/ml docetaxel en moet onmiddellijk na bereiding worden gebruikt, zelfs als de chemisch-fysische stabiliteit van deze oplossing is aangetoond gedurende een periode van 8 uur indien bewaard tussen + 2 ° C en + 8 C of omgevingstemperatuur temperatuur (beneden 25 C).
4.2 Bereiding van de oplossing voor infusie
4.2.1 Er kunnen meerdere injectieflacons met voorverdunde oplossing nodig zijn om de vereiste dosis voor de patiënt te verkrijgen. Op basis van de vereiste dosis voor de patiënt in mg, trekt u aseptisch het overeenkomstige volume van de voorverdunde oplossing met 10 mg/ml docetaxel op uit een geschikt aantal injectieflacons met behulp van een maatspuit met naald. Voor een dosis van 140 mg docetaxel moet bijvoorbeeld 14 ml docetaxel voorverdunde oplossing worden opgezogen.
4.2.2 Injecteer het benodigde volume van de voorverdunde oplossing in een zak of fles van 250 ml die 5% glucose-oplossing of 9 mg/ml natriumchloride (0,9%) oplossing voor infusie bevat. Als een dosis docetaxel hoger dan 200 mg nodig is, gebruik dan een groter volume oplossing voor infusie zodat de docetaxelconcentratie niet hoger wordt dan 0,74 mg/ml.
4.2.3 Meng de zak of fles handmatig met een draaiende beweging.
4.2.4 De TAXOTERE oplossing voor infusie dient binnen 4 uur te worden gebruikt en dient aseptisch te worden toegediend als een 1 uur durende infusie, bij kamertemperatuur (beneden 25 C) en onder normale lichtomstandigheden. Document beschikbaar gesteld door AIFA op 27-05-2015 243
4.2.5 Zoals met alle producten voor parenteraal gebruik, moeten de voorverdunde oplossing en de infusieoplossing van TAXOTERE vóór gebruik visueel worden onderzocht, oplossingen die precipitaten bevatten moeten worden weggegooid.
5. WIJZE VAN VERWIJDERING
Alle hulpmiddelen die zijn gebruikt om TAXOTERE te verdunnen of toe te dienen, moeten worden behandeld in overeenstemming met de standaardprocedures. Gooi medicijnen niet door de gootsteen. Vraag uw apotheker wat u met geneesmiddelen moet doen die u niet meer gebruikt. Dit helpt het milieu te beschermen.
Bron Bijsluiter: AIFA (Italiaans Geneesmiddelenbureau). Inhoud gepubliceerd in januari 2016. De aanwezige informatie is mogelijk niet up-to-date.
Om toegang te hebben tot de meest actuele versie, is het raadzaam om naar de website van AIFA (Italian Medicines Agency) te gaan. Disclaimer en nuttige informatie.
01.0 NAAM VAN HET GENEESMIDDEL
TAXOTERE 20 MG / 0,5 ML
02.0 KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
Elke injectieflacon met een enkelvoudige dosis TAXOTERE 20 mg/0,5 ml concentraat met docetaxel in de vorm van trihydraat, overeenkomend met 20 mg docetaxel (watervrij). De viskeuze oplossing bevat 40 mg/ml docetaxel (watervrij).
Hulpstof: Elke injectieflacon met een enkelvoudige dosis oplosmiddel bevat 13% (w/w) 95% ethanol in water voor injecties.
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1.
03.0 FARMACEUTISCHE VORM
Concentraat en oplosmiddel voor oplossing voor infusie.
Het concentraat is een heldere, stroperige, gele tot geelbruine oplossing.
Het oplosmiddel is een kleurloze oplossing.
04.0 KLINISCHE INFORMATIE
04.1 Therapeutische indicaties
Borstkanker:
TAXOTERE in combinatie met doxorubicine en cyclofosfamide is geïndiceerd voor de adjuvante behandeling van patiënten met:
- operabele lymfeklierpositieve borstkanker;
- operabele kliernegatieve borstkanker.
Bij patiënten met operabele kliernegatieve borstkanker dient adjuvante behandeling te worden beperkt tot patiënten die in aanmerking komen voor chemotherapie volgens internationale criteria voor de primaire behandeling van borstkanker in een vroeg stadium. (zie rubriek 5.1).
TAXOTERE in combinatie met doxorubicine is geïndiceerd voor de behandeling van patiënten met lokaal gevorderde of gemetastaseerde borstkanker die niet eerder met cytotoxische therapie voor deze ziekte zijn behandeld.
TAXOTERE als monotherapie is geïndiceerd voor de behandeling van patiënten met lokaal gevorderde of gemetastaseerde borstkanker na falen van cytotoxische therapie. Eerdere chemotherapie moet een antracycline of een alkyleringsmiddel bevatten.
TAXOTERE in combinatie met trastuzumab is geïndiceerd voor de behandeling van patiënten met gemetastaseerde borstkanker met HER2-overexpressie en die niet eerder chemotherapie hebben gekregen voor gemetastaseerde ziekte.
TAXOTERE in combinatie met capecitabine is geïndiceerd voor de behandeling van patiënten met lokaal gevorderde of gemetastaseerde borstkanker nadat cytotoxische chemotherapie heeft gefaald.
Bij eerdere chemotherapie moet een antracycline zijn gebruikt. Niet-kleincellige longkanker TAXOTERE is geïndiceerd voor de behandeling van patiënten met lokaal gevorderde of gemetastaseerde niet-kleincellige longkanker nadat eerdere chemotherapie heeft gefaald.
TAXOTERE in combinatie met cisplatine is geïndiceerd voor de behandeling van patiënten met inoperabele, lokaal gevorderde of gemetastaseerde niet-kleincellige longkanker die niet eerder chemotherapie hebben gekregen voor deze aandoening.
Prostaatkanker:
TAXOTERE in combinatie met prednison of prednisolon is geïndiceerd voor de behandeling van patiënten met hormoonongevoelige gemetastaseerde prostaatkanker.
Adenocarcinoom van de maag:
TAXOTERE in combinatie met cisplatine en 5-fluorouracil is geïndiceerd voor de behandeling van patiënten met gemetastaseerd adenocarcinoom van de maag, inclusief adenocarcinoom van de gastro-oesofageale overgang, die niet eerder chemotherapie hebben gekregen voor hun gemetastaseerde ziekte.
Hoofd-halskanker:
TAXOTERE in combinatie met cisplatine en 5-fluorouracil is geïndiceerd voor de inductiebehandeling van patiënten met lokaal gevorderd plaveiselcelcarcinoom van het hoofd-halsgebied.
04.2 Dosering en wijze van toediening
Het gebruik van docetaxel dient te worden beperkt tot afdelingen die gespecialiseerd zijn in de toediening van cytotoxische therapieën en de toediening ervan dient plaats te vinden onder toezicht van een arts die gespecialiseerd is in het gebruik van chemotherapie tegen kanker (zie rubriek 6.6).
Aanbevolen dosis:
Voor borstkanker, niet-kleincellige longkanker, maagadenocarcinoom en hoofd-halskanker, premedicatie met een oraal corticosteroïd zoals dexamethason 16 mg/dag (bijv. 8 mg BID) gedurende 3 dagen vanaf 1 dag voorafgaand aan de toediening van docetaxel (zie rubriek 4.4) G-CSF-profylaxe kan worden gebruikt om het risico op hematologische toxiciteit te verminderen.
Voor prostaatkanker is, gezien het gelijktijdige gebruik van prednison of prednisolon, de aanbevolen premedicatie oraal dexamethason 8 mg 12 uur, 3 uur en 1 uur voorafgaand aan de docetaxel-infusie (zie rubriek 4.4).
Docetaxel wordt elke drie weken toegediend als een infuus van één uur.
Borstkanker:
Voor adjuvante therapie van operabele klierpositieve en kliernegatieve borstkanker is de aanbevolen dosis docetaxel 75 mg/m2 toegediend 1 uur na doxorubicine 50 mg/m2 en cyclofosfamide 500 mg/m2 elke 3 weken gedurende 6 cycli (TAC-regime) ) (zie ook Dosisaanpassing tijdens de behandeling).
Voor de behandeling van patiënten met lokaal gevorderde of gemetastaseerde borstkanker is de aanbevolen dosis docetaxel monotherapie 100 mg/m2. Bij eerstelijnsbehandeling wordt docetaxel 75 mg/m2 toegediend in combinatie met doxorubicine (50 mg/m2).
In combinatie met trastuzumab is de aanbevolen dosis docetaxel 100 mg/m2 elke 3 weken, waarbij trastuzumab wekelijks wordt toegediend. In het hoofdonderzoek werd de eerste docetaxel-infusie gestart op de dag na de eerste toediening van trastuzumab. Daaropvolgende doses docetaxel werden onmiddellijk na de trastuzumab-infusie toegediend als de vorige dosis trastuzumab goed werd verdragen. Voor dosering en toediening van trastuzumab, zie de samenvatting van de productkenmerken van trastuzumab.
In combinatie met capecitabine is de aanbevolen dosering van docetaxel 75 mg/m2 elke drie weken, in combinatie met capecitabine in een dosis van 1250 mg/m2 tweemaal daags (binnen 30 minuten na een maaltijd) gedurende 2 weken gevolgd door een interval van 1 week . Zie de samenvatting van de productkenmerken van capecitabine voor de berekening van de dosis capecitabine per lichaamsoppervlak.
Niet-kleincellige longkanker:
Bij patiënten die nog nooit chemotherapie hebben gekregen voor niet-kleincellige longkanker, is de aanbevolen dosis docetaxel 75 mg/m2 onmiddellijk gevolgd door cisplatine 75 mg/m2 gedurende 30-60 minuten. Voor behandeling na falen van eerdere platinabevattende chemotherapie is de aanbevolen dosis 75 mg/m2 als monotherapie.
Prostaatkanker:
De aanbevolen dosis docetaxel is 75 mg/m2. Prednison of prednisolon 5 mg oraal tweemaal daags wordt toegediend voor de duur van de behandeling (zie rubriek 5.1).
Adenocarcinoom van de maag:
De aanbevolen dosis docetaxel is 75 mg/m2 als infusie van 1 uur, gevolgd door cisplatine 75 mg/m2, als infusie van 1-3 uur (beide alleen op dag 1), gevolgd door 5-fluorouracil 750 mg/m2 per dag toegediend als een continue 24-uurs infusie gedurende 5 dagen, te beginnen vanaf het einde van de cisplatine-infusie. De behandeling wordt elke drie weken herhaald. Patiënten dienen premedicatie te krijgen met anti-emetica en voldoende hydratatie voor toediening van cisplatine.
G-CSF-profylaxe moet worden gebruikt om het risico op hematologische toxiciteiten te verminderen (zie ook Dosisaanpassing tijdens de behandeling).
Hoofd-halskanker:
Patiënten dienen premedicatie anti-emetica en adequate hydratatie te krijgen (vóór en na toediening van cisplatine). Profylaxe met G-CSF kan zodanig worden uitgevoerd dat het risico op hematologische toxiciteiten wordt verminderd. Alle met docetaxel behandelde patiënten van de onderzoeken TAX 323 en TAX 324 kregen antibiotica profylaxe.
Inductiechemotherapie gevolgd door radiotherapie (TAX 323):
Voor de inductiebehandeling van patiënten met lokaal gevorderd inoperabel plaveiselcelcarcinoom van het hoofd-halsgebied (SCCHN), is de aanbevolen dosis docetaxel 75 mg/m2 als een 1 uur durende infusie gevolgd door 75 mg/m2 cisplatine gedurende meer dan 1 uur, op dag 1, gevolgd door 5-fluorouracil 750 mg/m2 per dag toegediend als een continue 24-uurs infusie gedurende 5 dagen. Dit doseringsschema wordt elke 3 weken gedurende 4 cycli toegediend. Na chemotherapie moeten patiënten radiotherapie krijgen.
Inductiechemotherapie gevolgd door chemoradiotherapie (TAX 324):
Voor de inductiebehandeling van patiënten met lokaal gevorderd plaveiselcelcarcinoom van het hoofd-hals (SCCHN) (technisch onbruikbaar, met een lage kans op chirurgisch succes en met het oog op orgaanbehoud) is de aanbevolen dosis docetaxel 75 mg/m2 als een 1 uur durende infusie op dag 1, gevolgd door cisplatine 100 mg/m2 toegediend als een infusie van 30 minuten tot drie uur, gevolgd door 5-fluorouracil 1000 mg/m2 per dag, toegediend in een continue infusie van 1 - 4 dagen. Dit doseringsschema wordt elke drie weken gedurende drie cycli gegeven. Na chemotherapie moeten patiënten chemo-radiotherapie krijgen.
Zie de specifieke samenvatting van de productkenmerken voor dosisaanpassingen van 5-fluorouracil en cisplatine. Doseringsaanpassing tijdens de behandeling:
Algemeen
Docetaxel dient te worden toegediend wanneer het aantal neutrofielen 3 1500 cellen/mm3 is.
Bij patiënten die febriele neutropenie, neutrofiele ernstige perifere neuropathie hebben ervaren tijdens behandeling met docetaxel, moet de dosis docetaxel worden verlaagd van 100 mg/m2 naar 75 mg/m2 en/of van 75 naar 60 mg/m2. Als de patiënt bij 60 mg/m2 deze reacties blijft ervaren, moet de behandeling worden stopgezet.
Adjuvante therapie voor borstkanker:
Primaire G-CSF-profylaxe moet worden overwogen bij patiënten die adjuvante therapie krijgen met docetaxel, doxorubicine en cyclofosfamide (TAC) voor borstkanker. Bij patiënten met febriele neutropenie en/of neutropenische infectie moet de docetaxel-dosis in alle volgende kuren worden verlaagd tot 60 mg/m2 (zie rubrieken 4.4 en 4.8). Bij patiënten die graad 3 of 4 stomatitis ervaren, moet de dosis worden verlaagd tot 60 mg/m2
In combinatie met cisplatine:
Voor patiënten die aanvankelijk werden behandeld met docetaxel 75 mg/m2 in combinatie met cisplatine en bij wie het dieptepunt van het aantal bloedplaatjes in de vorige behandelingskuur was
In combinatie met capecitabine:
Voor dosisaanpassing van capecitabine, zie de Samenvatting van de productkenmerken van capecitabine.
Bij patiënten die voor het eerst een graad 2 toxiciteit ontwikkelen die aanhoudt op het moment van daaropvolgende toediening van docetaxel/capecitabine, dient de behandeling te worden uitgesteld tot herstel tot graad 0-1, en dan hervat met 100% van de aanvangsdosis.
Bij patiënten die op enig moment in de loop van de therapie voor de tweede keer graad 2 toxiciteit ontwikkelen, of voor het eerst graad 3 toxiciteit ontwikkelen, moet de behandeling worden uitgesteld tot herstel tot graad 0-1, en dan worden hervat met docetaxel 55 mg/m2. .
Voor elk volgend optreden van toxiciteit of voor elke graad 4 toxiciteit, moet de behandeling met docetaxel worden gestaakt.
Voor dosisaanpassingen van trastuzumab, zie de Samenvatting van de productkenmerken van trastuzumab.
In combinatie met cisplatine en 5-fluorouracil:
Als ondanks het gebruik van G-CSF een episode van febriele neutropenie, langdurige neutropenie of infectie-neutropenie optreedt, moet de docetaxel-dosis worden verlaagd van 75 naar 60 mg/m 2. Als zich verdere episodes van gecompliceerde neutropenie voordoen, moet de docetaxel-dosis worden verlaagd van 60 mg/m2. tot 45 mg/m2.Voor trombocytopenie graad 4 moet de dosis docetaxel worden verlaagd van 75 naar 60 mg/m2. Patiënten mogen niet opnieuw worden behandeld met docetaxel totdat de neutrofielen terugkeren tot een niveau > 1.500 cellen / mm3 en de bloedplaatjes terugkeren tot een niveau > 100.000 cellen / mm3. Beëindig de behandeling als deze toxiciteiten aanhouden (zie rubriek 4.4). Aanbevolen dosisaanpassingen vanwege toxiciteit bij patiënten die worden behandeld met docetaxel in combinatie met cisplatine en 5-fluorouracil (5-FU):
Voor dosisaanpassingen van cisplatine en 5-fluorouracil, zie de specifieke samenvatting van de productkenmerken.
In de hoofdstudie SCCHN bij patiënten die gecompliceerde neutropenie doormaakten (inclusief langdurige neutropenie, febriele neutropenie of infectie), werd het gebruik van GCSF voorgesteld om profylactische dekking te bieden (bijv. dagen 6-15) in alle volgende cycli.
Speciale populaties:
Patiënten met leverinsufficiëntie:
Gebaseerd op farmacokinetische gegevens met docetaxel 100 mg/m2 gegeven als enkelvoudige behandeling, bij patiënten met verhogingen in transaminasen (ALAT en/of ASAT) van meer dan 1,5 maal de bovengrens van normaal en alkalische fosfatase meer dan 2,5 maal de bovengrens van normaal is de aanbevolen dosis docetaxel 75 mg/m2 (zie rubrieken 4.4 en 5.2). Voor patiënten met serumbilirubine boven de bovengrens van normaal en/of ALT en ASAT > 3,5 keer de bovengrens van normaal geassocieerd met alkalische fosfatase hoger dan 6 keer de bovengrens van normaal, kan geen dosisverlaging worden aanbevolen en docetaxel zal dit niet doen. moet worden toegediend, behalve in gevallen waar dit strikt is aangegeven.
In combinatie met cisplatine en 5-fluorouracil voor de behandeling van patiënten met adenocarcinoom van de maag, sloot het klinische hoofdonderzoek patiënten uit met ALT en/of ASAT > 1,5 maal de bovengrens van normaal geassocieerd met een alkalische fosfatasewaarde > 2,5 maal de bovengrens normaal en bij een bilirubinewaarde > 1 maal de bovengrens van normaal; voor deze patiënten kan geen dosisverlaging worden aanbevolen en docetaxel mag niet worden gebruikt tenzij strikt geïndiceerd. Er zijn geen gegevens beschikbaar over patiënten met een leverfunctiestoornis die voor de andere indicaties worden behandeld met docetaxel in combinatie.
Pediatrische populatie:
De veiligheid en werkzaamheid van TAXOTERE bij nasofaryngeale kanker bij kinderen in de leeftijd van 1 maand tot jonger dan 18 jaar zijn niet vastgesteld.
Er zijn geen gegevens over het gebruik van TAXOTERE bij pediatrische patiënten voor de indicaties borstkanker, niet-kleincellige longkanker, prostaatkanker, maagkanker en hoofd-halskanker, met uitzondering van minder gedifferentieerde type II en III nasofaryngeale kanker.
Bejaarden.
Op basis van populatiefarmacokinetiek zijn er geen speciale instructies voor gebruik bij ouderen.
In combinatie met capecitabine wordt voor patiënten van 60 jaar en ouder een verlaging van de aanvangsdosis tot 75% aanbevolen (zie de Samenvatting van de productkenmerken van capecitabine).
04.3 Contra-indicaties
Overgevoeligheid voor de werkzame stof of voor één van de hulpstoffen.
Docetaxel mag niet worden gebruikt bij patiënten met een aanvankelijke neutrofielentelling
Docetaxel mag niet worden gebruikt bij patiënten met een ernstige leverfunctiestoornis vanwege een gebrek aan beschikbare gegevens (zie rubrieken 4.2 en 4.4).
Contra-indicaties voor andere geneesmiddelen gelden ook bij gebruik in combinatie met docetaxel.
04.4 Bijzondere waarschuwingen en passende voorzorgen bij gebruik
Tenzij gecontra-indiceerd, premedicatie met orale corticosteroïden, zoals dexamethason 16 mg per dag (bijv. 8 mg BID) gedurende 3 dagen, beginnend op de dag vóór toediening van docetaxel, gedurende 3 dagen vanaf de dag vóór toediening van docetaxel voor borst- en niet-kleincellige longkankers, kan de incidentie en ernst van vochtretentie evenals de ernst van overgevoeligheidsreacties verminderen. Voor prostaatkanker is premedicatie oraal dexamethason 8 mg, 12 uur, 3 uur en 1 uur voorafgaand aan de docetaxel-infusie (zie paragraaf 4.2).
hematologie:
Neutropenie is de meest voorkomende van de bijwerkingen die met docetaxel zijn waargenomen. Neutrofiele nadirs verschenen na 7 dagen (mediane waarde), maar bij zwaar voorbehandelde patiënten kan dit interval worden verkort. Bij alle patiënten die docetaxel krijgen, dient regelmatig een volledige bloedtelling te worden uitgevoerd.Patiënten mogen niet opnieuw met docetaxel worden behandeld totdat de neutrofielenwaarde terugkeert naar 3 1.500 cellen/mm3 (zie rubriek 4.2).
In het geval van ernstige neutropenie (
Bij patiënten die werden behandeld met docetaxel in combinatie met cisplatine en 5-fluorouracil (TCF), traden febriele neutropenie en neutropenische infectie op met een lagere incidentie wanneer patiënten profylactisch G-CSF kregen. Patiënten die met TCF worden behandeld, moeten G-CSF als profylaxe krijgen om het risico op gecompliceerde neutropenie (febriele neutropenie, langdurige neutropenie of neutropenische infectie) te verminderen. Patiënten die TCF krijgen, moeten zeer nauwlettend worden gecontroleerd (zie rubrieken 4.2 en 4.8).
Bij patiënten die werden behandeld met docetaxel in combinatie met doxorubicine en cyclofosfamide (TAC-regime), trad febriele neutropenie en/of neutropenische infectie op met een "lagere incidentie wanneer patiënten primaire G-CSF-profylaxe kregen. Primaire G-CSF-profylaxe. CSF moet worden overwogen bij patiënten die adjuvante CT-therapie krijgen voor borstkanker om het risico op gecompliceerde neutropenie (febriele neutropenie, langdurige neutropenie of neutropenische infectie) te verminderen Patiënten die een CT-scan krijgen, moeten nauwlettend worden gecontroleerd (zie rubrieken 4.2 en 4.8).
Overgevoeligheidsreacties:
Patiënten moeten nauwlettend worden gecontroleerd op het mogelijke optreden van overgevoeligheidsreacties, vooral tijdens de eerste en tweede infusie. Overgevoeligheidsreacties kunnen optreden binnen enkele minuten na het starten van de docetaxel-infusie, daarom moeten middelen beschikbaar zijn om hypotensie en bronchospasme te behandelen. Als overgevoeligheidsreacties met lichte symptomen zoals blozen of plaatselijke huidreacties optreden, is het niet nodig om de behandeling te staken. Ernstige reacties, zoals ernstige hypotensie, bronchospasme of gegeneraliseerde huiduitslag/erytheem, vereisen echter onmiddellijke stopzetting van de docetaxel-infusie en een passende behandeling. Patiënten die ernstige overgevoeligheidsreacties ervaren, mogen docetaxel niet langer gebruiken.
Huidreacties:
Gelokaliseerd huiderytheem in de extremiteiten (handpalm en voetzool) met oedeem gevolgd door afschilfering is waargenomen. Ernstige symptomen zoals huiduitslag gevolgd door vervelling, leidend tot tijdelijke of definitieve stopzetting van de docetaxelbehandeling, zijn gemeld (zie rubriek 4.2).
Vloeistofretentie:
Patiënten met ernstige vochtretentie, zoals pleurale, pericardiale en ascites-effusies, moeten nauwlettend worden gecontroleerd.
Patiënten met leverdisfunctie:
Bij patiënten die worden behandeld met 100 mg/m2 docetaxel alleen toegediend en die serumtransaminasespiegels (ALAT en/of ASAT) hebben die hoger zijn dan 1,5 keer de bovengrens van normaal, gelijktijdig met serum alkalische fosfatasespiegels hoger dan 2,5 keer de bovengrens van normaal, c "is een hoger risico op het ontwikkelen van ernstige bijwerkingen zoals toxische dood, waaronder gastro-intestinale sepsis en bloedingen die fataal kunnen zijn, febriele neutropenie, infecties, trombocytopenie, stomatitis en asthenie. Daarom is bij patiënten met hoge leverfunctietests de aanbevolen dosis docetaxel 75 mg/m2 en leverfunctietesten moeten worden uitgevoerd voordat de behandeling wordt gestart en vóór elke cyclus (zie rubriek 4.2).
Bij patiënten die serumbilirubinewaarden hebben die hoger zijn dan de bovengrens van normaal en/of ALT- en AST-waarden die groter zijn dan 3,5 keer de bovengrens van normaal met alkalische fosfatase hoger dan 6 keer de bovengrens van normaal, een dosisverlaging kan niet worden aanbevolen en docetaxel mag niet worden gebruikt tenzij strikt aangegeven.
In combinatie met cisplatine en 5-fluorouracil voor de behandeling van patiënten met adenocarcinoom van de maag, sloot het klinische hoofdonderzoek patiënten uit met ALT en/of ASAT > 1,5 maal de bovengrens van normaal geassocieerd met een alkalische fosfatasewaarde > 2,5 maal de bovengrens normaal en bij een bilirubinewaarde > 1 maal de bovengrens van normaal; voor deze patiënten kan geen dosisverlaging worden aanbevolen en docetaxel mag niet worden gebruikt tenzij strikt geïndiceerd.Er zijn geen gegevens beschikbaar over patiënten met een leverfunctiestoornis die worden behandeld met docetaxel in combinatie bij de andere indicaties.
Patiënten met een verminderde nierfunctie:
Er zijn geen gegevens beschikbaar over patiënten met een ernstige nierfunctiestoornis die met docetaxel worden behandeld.
Zenuwstelsel:
Het optreden van ernstige perifere neurotoxiciteit vereist dosisverlaging (zie rubriek 4.2).
Cardiale toxiciteit:
Hartfalen is waargenomen bij patiënten die werden behandeld met docetaxel in combinatie met trastuzumab, met name na chemotherapie met antracyclines (doxorubicine of epirubicine).
Deze bleek matig tot ernstig te zijn en is in verband gebracht met overlijden (zie rubriek 4.8).
Wanneer patiënten in aanmerking komen voor docetaxel in combinatie met contrastuzumab, moeten ze een hartonderzoek bij baseline ondergaan. De hartfunctie moet verder worden gecontroleerd tijdens de behandeling (bijv. elke drie maanden) om patiënten te identificeren die hartafwijkingen kunnen ontwikkelen. Zie de samenvatting van de productkenmerken van trastuzumab voor meer details.
Ander:
Tijdens de behandeling dienen voor zowel mannen als vrouwen als voor mannen gedurende ten minste zes maanden na stopzetting van de behandeling anticonceptieve maatregelen te worden genomen (zie rubriek 4.6).
Aanvullende voorzorgsmaatregelen voor adjuvante behandeling van borstkanker
Gecompliceerde neutropenie:
Voor patiënten met gecompliceerde neutropenie (langdurige neutropenie, febriele neutropenie of infectie), dienen G-CSF-therapie en dosisverlaging te worden overwogen (zie rubriek 4.2).
Gastro-intestinale bijwerkingen:
Symptomen zoals buikpijn en malaise, koorts, diarree met of zonder neutropenie, kunnen vroege manifestaties zijn van ernstige gastro-intestinale toxiciteit en moeten onmiddellijk worden geëvalueerd en behandeld.
Congestief hartfalen:
Patiënten moeten worden gecontroleerd op symptomen die kunnen leiden tot congestief hartfalen tijdens de behandeling en de follow-upperiode.
Leukemie:
Bij patiënten die worden behandeld met docetaxel, doxorubicine en cyclofosfamide (TAC) vereist het risico op vertraagde myelodysplasie of myeloïde leukemie hematologische follow-up.
Patiënten met 4 of meer positieve lymfeklieren:
De baten-risicoverhouding van CT-therapie bij patiënten met 4 of meer positieve lymfeklieren is niet volledig vastgesteld met de tussentijdse analyse (zie rubriek 5.1).
Bejaarden:
Er zijn beperkte gegevens beschikbaar over patiënten ouder dan 70 jaar die worden behandeld met docetaxel in combinatie met doxorubicine en cyclofosfamide.
In een onderzoek naar prostaatkanker onder 333 patiënten die om de drie weken met docetaxel werden behandeld, waren 209 patiënten 65 jaar of ouder en 68 patiënten ouder dan 75. Bij patiënten die om de drie weken met docetaxel werden behandeld, veranderde de incidentie van geneesmiddelgerelateerde nagelplaten, bij patiënten van 65 jaar of ouder, waren meer dan 10% hoger dan bij jongere patiënten. De incidentie van geneesmiddelgerelateerde koorts, diarree, anorexia en perifeer oedeem bij patiënten van 75 jaar en ouder was meer dan 10% hoger dan bij patiënten jonger dan 65 jaar.
Van de 300 patiënten (221 in het fase III-onderzoek en 79 in het fase II-onderzoek) die in het maagkankeronderzoek werden behandeld met docetaxel in combinatie met cisplatine en 5-fluorouracil, waren er 74 65 jaar of ouder en 4 75 jaar of ouder. De incidentie van ernstige bijwerkingen was hoger bij ouderen dan bij jongere patiënten De incidentie van bijwerkingen was hoger bij ouderen dan bij jonge patiënten. De incidentie van de volgende bijwerkingen (alle gradaties): lethargie, stomatitis en neutropenische infectie kwamen voor met een frequentie> 10% bij patiënten van 65 jaar of ouder in vergelijking met jongere patiënten.Oudere patiënten die met TCF worden behandeld, moeten zeer zorgvuldig worden gecontroleerd.
04.5 Interacties met andere geneesmiddelen en andere vormen van interactie
In vitro-onderzoeken hebben aangetoond dat het metabolisme van docetaxel kan worden gewijzigd door gelijktijdige toediening van verbindingen die cytochroom P450-3A induceren of remmen of die daardoor worden gemetaboliseerd (en daardoor het enzym competitief kunnen remmen), zoals ciclosporine, terfenadine, ketoconazol , erytromycine en troleandomycine Daarom is voorzichtigheid geboden bij de gelijktijdige behandeling van patiënten met dergelijke geneesmiddelen vanwege het potentiële risico op belangrijke interacties.
Docetaxel is sterk eiwitgebonden (> 95%). Hoewel de mogelijke in vivo interactie tussen docetaxel en gelijktijdige therapieën niet specifiek is onderzocht, hadden de in vitro interacties tussen nauw aan eiwit gebonden geneesmiddelen zoals erytromycine, difenhydramine, propranolol, propafenon, fenytoïne, salicylaten, sulfamethoxazol en natriumvalproaat geen invloed op de binding. van docetaxel aan eiwitten. Bovendien verandert dexamethason de eiwitbinding van docetaxel niet. Docetaxel heeft geen invloed op de binding van digitoxine De farmacokinetiek van docetaxel, doxorubicine en cyclofosfamide stoorde niet tijdens gelijktijdige toediening. Beperkte gegevens van een enkele ongecontroleerde studie lijken een interactie tussen docetaxel en carboplatine aan te geven Bij gebruik in combinatie met docetaxel was de klaring van carboplatine ongeveer 50% hoger dan eerder gerapporteerde waarden voor alleen gebruik.
De farmacokinetiek van docetaxel in aanwezigheid van prednison is onderzocht bij patiënten met gemetastaseerde prostaatkanker. Docetaxel wordt gemetaboliseerd door CYP3A4 en prednison veroorzaakt inductie van CYP3A4. Er werd geen statistisch significant effect van prednison op de farmacokinetiek van docetaxel waargenomen.
Docetaxel dient met voorzichtigheid te worden toegediend aan patiënten die gelijktijdig een krachtige CYP3A4-remmer gebruiken (bijv. proteaseremmers zoals ritonavir, azol-antischimmelmiddelen zoals ketoconazol of itraconazol). Een geneesmiddelinteractiestudie uitgevoerd bij patiënten die ketoconazol en docetaxel gebruikten, toonde aan dat de klaring van docetaxel gehalveerd wordt als gevolg van ketoconazol, mogelijk omdat het docetaxelmetabolisme CYP3A4 als de belangrijkste metabole route omvat. Verminderde tolerantie voor docetaxel kan optreden, zelfs bij lage doses.
04.6 Zwangerschap en borstvoeding
Er is geen informatie over het gebruik van docetaxel bij zwangere vrouwen In onderzoeken bij ratten en konijnen is docetaxel embryotoxisch en foetotoxisch en vermindert het de vruchtbaarheid bij ratten Zoals met andere cytotoxische geneesmiddelen kan docetaxel schade aan de foetus veroorzaken bij toediening aan zwangere vrouwen. reden waarom docetaxel niet aan zwangere vrouwen mag worden toegediend, tenzij duidelijk aangegeven.
Vrouwen in de vruchtbare leeftijd/anticonceptie:
Vrouwen in de vruchtbare leeftijd die met docetaxel worden behandeld, moeten worden geadviseerd het risico op zwangerschap te vermijden en hun arts onmiddellijk op de hoogte te stellen als dit gebeurt.
Tijdens de behandeling moet een effectieve anticonceptiemethode worden gebruikt.
In niet-klinische onderzoeken heeft docetaxel genotoxische effecten en kan het de mannelijke vruchtbaarheid aantasten (zie rubriek 5.3). Daarom wordt aanbevolen dat mannen die met docetaxel worden behandeld, zich tijdens en tot 6 maanden na de behandeling niet voortplanten en voorafgaand aan de behandeling informeren naar de opslag van sperma.
Voedertijd:
Docetaxel is een lipofiele stof, maar het is niet bekend of het wordt uitgescheiden in de moedermelk. Gezien de mogelijkheid van bijwerkingen bij de zuigeling, dient de borstvoeding daarom te worden gestaakt tijdens de behandeling met docetaxel.
04.7 Beïnvloeding van de rijvaardigheid en het vermogen om machines te bedienen
Er is geen onderzoek gedaan naar de effecten op de rijvaardigheid of op het vermogen om machines te bedienen.
04.8 Bijwerkingen
Bijwerkingen die mogelijk of waarschijnlijk verband hielden met de toediening van docetaxel werden verkregen in:
1312 en 121 patiënten die respectievelijk docetaxel 100 mg/m2 en 75 mg/m2 als monotherapie kregen.
258 patiënten die docetaxel kregen in combinatie met doxorubicine.
406 patiënten die docetaxel kregen in combinatie met cisplatine.
92 patiënten behandeld met docetaxel in combinatie met trastuzumab.
255 patiënten die docetaxel kregen in combinatie met capecitabine.
332 patiënten die docetaxel kregen in combinatie met prednison of prednisolon (klinisch relevante behandelingsgerelateerde bijwerkingen worden weergegeven).
1276 patiënten (respectievelijk 744 en 532 in TAX 316 en GEICAM 9805) die docetaxel kregen in combinatie met doxorubicine en cyclofosfamide (klinisch relevante behandelingsgerelateerde bijwerkingen worden weergegeven).
300 patiënten met adenocarcinoom van de maag (221 in de fase III-studie en 79 in de fase II-studie) die werden behandeld met docetaxel in combinatie met cisplatine en 5-fluorouracil (klinisch belangrijke behandelingsgerelateerde bijwerkingen traden op).
174 patiënten met hoofd-halskanker die werden behandeld met docetaxel in combinatie met cisplatine en 5-fluorouracil (klinisch belangrijke bijwerkingen gerelateerd aan de behandeling zijn opgetreden).
Deze reacties zijn beschreven met de NCI Common Toxicity Criteria (graad 3 = G3; graad 3- -4 = G3/4; graad 4 = G4) en met de termen COSTART en MedDRA. Frequenties worden gedefinieerd als:
zeer vaak (≥ 1/10); vaak (≥ 1/100 tot
Binnen elke frequentieklasse worden bijwerkingen gerapporteerd in afnemende volgorde van ernst.
De meest frequent gemelde bijwerkingen tijdens het gebruik van alleen docetaxel zijn: neutropenie (reversibel en niet-cumulatief; gemiddelde dag tot dieptepunt was dag 7 en gemiddelde duur van ernstige neutropenie (anemie, alopecia, misselijkheid, braken, stomatitis, diarree en asthenie) Het aantal bijwerkingen van docetaxel kan toenemen wanneer docetaxel wordt toegediend in combinatie met andere chemotherapeutische middelen.
Voor combinatie met trastuzumab werden bijwerkingen (alle gradaties) gerapporteerd als een percentage van 10% Er was een verhoogde incidentie van ernstige bijwerkingen (40% vs 31%) en graad 4 bijwerkingen (34% vs 23%) in de trastuzumab-combinatiegroep versus docetaxel-monotherapie. Voor combinatie met capecitabine zijn de meest voorkomende behandelingsgerelateerde bijwerkingen (≥ 5%) die zijn waargenomen in een klinische fase III-studie bij borstkankerpatiënten na falen van de antracyclinetherapie gemeld (zie samenvatting van de productkenmerken van capecitabine).
De volgende bijwerkingen zijn vaak waargenomen met docetaxel:
Immuunsysteemaandoeningen:
Overgevoeligheidsreacties traden gewoonlijk op binnen enkele minuten na aanvang van de docetaxel-infusie en waren over het algemeen licht tot matig van ernst. De meest gemelde symptomen waren opvliegers, huiduitslag met of zonder jeuk, beklemd gevoel op de borst, rugpijn, dyspneu en koorts of koude rillingen. Ernstige reacties werden gekenmerkt door hypotensie en/of bronchospasme of gegeneraliseerde huiduitslag/erytheem (zie rubriek 4.4)
Zenuwstelselaandoeningen:
De ontwikkeling van ernstige perifere neurotoxiciteit vereist dosisverlaging (zie rubrieken 4.2 en 4.4).
Milde tot matige sensorineurale verschijnselen worden gekenmerkt door paresthesie, dysesthesie of pijn, waaronder een branderig gevoel. Neuromotorische gebeurtenissen worden voornamelijk gekenmerkt door zwakte.
Huid- en onderhuidaandoeningen:
Omkeerbare huidreacties zijn waargenomen en worden over het algemeen als licht tot matig ernstig beschouwd. De reacties werden gekenmerkt door huiduitslag, waaronder plaatselijke erupties, voornamelijk in de voeten en handen (waaronder ernstig hand-voetsyndroom), maar ook in de armen, het gezicht of de borstkas, vaak geassocieerd met pruritus. Uitbarstingen traden over het algemeen op binnen een week na de docetaxel-infusie Minder frequente ernstige symptomen zoals erupties gevolgd door afschilfering zijn gemeld, waarbij zelden tijdelijke of permanente stopzetting van de behandeling nodig was (zie rubrieken 4.2 en 4.4 Ernstige symptomen zijn gemeld nagelveranderingen gekarakteriseerd door hypopigmentatie of hyperpigmentatie, soms pijn en onycholyse.
Algemene aandoeningen en toedieningsplaatsstoornissen:
Reacties op de infusieplaats waren over het algemeen mild en werden gekenmerkt door hyperpigmentatie, ontsteking, roodheid en droogheid van de huid, flebitis of extravasatie, "verhoogde doorlaatbaarheid" van de ader.
Vochtretentie, waaronder gevallen van perifeer oedeem en minder vaak gevallen van pleurale, pericardiale effusies, ascites en gewichtstoename. Perifeer oedeem begint meestal in de onderste ledematen en kan veralgemeend worden met een gewichtstoename van 3 kg of meer Vochtretentie is cumulatief in incidentie en intensiteit (zie rubriek 4.4).
TAXOTERE 100 mg/m2 als monotherapie
Aandoeningen van het bloed en het lymfestelsel
Zelden: bloedingsepisodes geassocieerd met graad 3/4 trombocytopenie.
Zenuwstelselaandoeningen
Reversibiliteitsgegevens zijn beschikbaar bij 35,3% van de patiënten die neurotoxiciteit ontwikkelden na behandeling met docetaxel 100 mg/m2 monotherapie. De voorvallen waren spontaan omkeerbaar binnen 3 maanden.
Huid- en onderhuidaandoeningen
Zeer zelden: één geval van niet-reversibele alopecia aan het einde van het onderzoek. 73% van de huidreacties was binnen 21 dagen omkeerbaar.
Algemene aandoeningen en toedieningsplaatsstoornissen
De gemiddelde cumulatieve dosis bij stopzetting van de behandeling was meer dan 1.000 mg/m2 en de mediane tijd tot reversibiliteit van vochtretentie was 16,4 weken (bereik 0 tot 42 weken). Het begin van matige tot ernstige retentie (gemiddelde cumulatieve dosis: 818,9 mg/m2) is vertraagd bij patiënten die premedicatie kregen in vergelijking met patiënten zonder premedicatie (gemiddelde cumulatieve dosis: 489,7 mg/m2); bij sommige patiënten is het echter gemeld tijdens de eerste therapiekuren.
TAXOTERE 75 mg/m2 als monotherapie
TAXOTERE 75 mg/m2 in combinatie met doxorubicine
TAXOTERE 75 mg/m2 in combinatie met cisplatine
TAXOTERE 100 mg/m2 in combinatie met trastuzumab
Cardiale pathologieën
Symptomatisch hartfalen werd gemeld bij 2,2% van de patiënten die docetaxel in combinatie met trastuzumab kregen, vergeleken met 0% van de patiënten die alleen docetaxel kregen. In de docetaxel- en trastuzumab-groep had 64% van de patiënten eerder antracyclines als adjuvante therapie gekregen, vergeleken met 55% van de patiënten die alleen met docetaxel werden behandeld.
Aandoeningen van het bloed en het lymfestelsel
Zeer vaak: De hematologische toxiciteit was verhoogd bij patiënten behandeld met trastuzumab en docetaxel in vergelijking met patiënten behandeld met alleen docetaxel (graad 3/4 neutropenie 32% vs 22% volgens NCI-CTC-criteria). Merk op dat dit waarschijnlijk een onderschatting is, aangezien bekend is dat docetaxel alleen in een dosis van 100 mg/m2 leidt tot neutropenie bij 97% van de patiënten, graad 4 bij 76%, gebaseerd op het dieptepunt van het aantal neutrofielen. De incidentie van febriele neutropenie/neutropenische sepsis was ook verhoogd bij patiënten behandeld met Herceptin en docetaxel (23% versus 17% van de patiënten behandeld met alleen docetaxel).
TAXOTERE 75 mg/m2 in combinatie met capecitabine
TAXOTERE 75 mg/m2 in combinatie met prednison of prednisolon
Adjuvante therapie met TAXOTERE 75 mg/m2 in combinatie met doxorubicine en cyclofosfamide bij patiënten met klierpositieve (TAX 316) en kliernegatieve (GEICAM 9805) borstkanker - cumulatieve gegevens:
Zenuwstelselaandoeningen
Tijdens de follow-up hadden 12 van de 83 patiënten die aan het einde van de chemotherapie perifere sensorische neuropathie hadden ervaren, nog steeds symptomen van perifere sensorische neuropathie.
Cardiale pathologieën
Congestief hartfalen (CHF) werd gemeld bij 18 van de 1276 patiënten tijdens de follow-upperiode. In de klierpositieve studie (TAX316) stierf één patiënt in elke behandelingsgroep aan hartfalen.
Huid- en onderhuidaandoeningen
Tijdens de follow-up hadden 25 van de 736 patiënten die alopecia kregen aan het einde van de chemotherapie nog steeds alopecia.
Ziekten van het voortplantingssysteem en de borst
Tijdens de follow-up hadden 140 van de 251 patiënten die amenorroe kregen aan het einde van de chemotherapie nog steeds symptomen van amenorroe.
Algemene aandoeningen en toedieningsplaatsstoornissen
Tijdens de follow-up hadden 18 van de 112 patiënten die perifeer oedeem ervoeren aan het einde van chemotherapie in onderzoek TAX 316 nog steeds symptomen van perifeer oedeem, terwijl 4 van de 5 patiënten die lymfoedeem kregen aan het einde van chemotherapie in GEICAM 9805 nog steeds symptomen hadden van perifeer oedeem Symptomen van lymfoedeem.
Acute leukemie / myelodysplastisch syndroom.
Bij een gemiddelde follow-up van 77 maanden trad acute leukemie op bij 1 van de 532 (0,2%) patiënten die docetaxel, doxorubicine en cyclofosfamide kregen in GEICAM 9805. Er werden geen gevallen gemeld bij patiënten die fluorouracil, doxorubicine en cyclofosfamide kregen. In geen van de behandelingsgroepen werden gevallen van myelodysplastisch syndroom gediagnosticeerd. De onderstaande tabel laat zien dat de incidentie van graad 4 neutropenie, febriele neutropenie en neutropenische infectie verminderd was bij patiënten die primaire G-CSF-profylaxe kregen nadat dit verplicht werd in de TAC-arm - GEICAM-studie.
Neutropenische complicaties bij patiënten die CT kregen met of zonder primaire G-CSF-profylaxe (GEICAM 9805)
TAXOTERE 75 mg/m2 in combinatie met cisplatine en 5-fluorouracil voor maagadenocarcinoom
Aandoeningen van het bloed en het lymfestelsel
Febriele neutropenie en neutropenische infectie kwamen voor bij respectievelijk 17,2% en 13,5% van de patiënten, ongeacht het gebruik van G-CSF. G-CSF werd gebruikt voor secundaire profylaxe bij 19,3% van de patiënten (10,7% van de kuren). Febriele neutropenie en neutropenische infectie kwamen respectievelijk voor bij 12,1% en 3,4% van de patiënten die G-CSF als profylaxe kregen, bij 15,6% en 12,9% van de patiënten zonder profylaxe met G-CSF (zie rubriek 4.2).
TAXOTERE 75 mg/m2 in combinatie met cisplatine en 5-fluorouracil voor hoofd-halskanker
Inductiechemotherapie gevolgd door radiotherapie (TAX 323)
Inductiechemotherapie gevolgd door chemoradiotherapie (TAX324)
Postmarketingervaring:
Neoplasmata, goedaardig, kwaadaardig en niet gespecificeerd (inclusief cysten en poliepen)
Zeer zeldzame gevallen van acute myeloïde leukemie en myelodysplastisch syndroom zijn gemeld bij gebruik van docetaxel in combinatie met andere chemotherapeutische en/of radiotherapeutische middelen.
Aandoeningen van het bloed en het lymfestelsel
Beenmergsuppressie en andere hematologische bijwerkingen zijn gemeld. Gedissemineerde intravasculaire stolling is vaak gemeld in verband met sepsis of multi-orgaanfalen.
Aandoeningen van het immuunsysteem
Er zijn enkele gevallen van anafylactische shock gemeld, waarvan sommige fataal.
Zenuwstelselaandoeningen
Zeldzame gevallen van convulsies of tijdelijk bewustzijnsverlies zijn waargenomen na toediening van docetaxel. Deze reacties treden soms op tijdens de infusie.
Oogaandoeningen
Zeer zeldzame gevallen van voorbijgaande visuele veranderingen (flitsen, lichtflitsen, scotoma) en in combinatie met overgevoeligheidsreacties zijn typisch opgetreden tijdens de infusie van het geneesmiddel Deze waren reversibel na stopzetting van de infusie. Gevallen van tranenvloed met of zonder conjunctivitis zijn zelden gemeld, zoals gevallen van traankanaalobstructie als gevolg van overmatig scheuren.
Oor- en labyrintaandoeningen
Zeldzame gevallen van ototoxiciteit, gehoorbeschadiging en/of gehoorverlies zijn gemeld.
Cardiale pathologieën
Zeldzame gevallen van myocardinfarct zijn gemeld.
Vasculaire pathologieën
Veneuze trombo-embolische voorvallen zijn zelden gemeld.
Ademhalingsstelsel-, borstkas- en mediastinumaandoeningen
Acuut respiratoir distress syndroom, interstitiële pneumonie en longfibrose zijn zelden gemeld. Zeldzame gevallen van door bestraling geïnduceerde pneumonie zijn gemeld bij patiënten die ook bestralingstherapie ondergingen.
Maagdarmstelselaandoeningen
Zeldzame episoden van dehydratie zijn gemeld als gevolg van gastro-intestinale stoornissen, gastro-intestinale perforatie, ischemische colitis, colitis en neutropenische enterocolitis. Zeldzame gevallen van ileum- en darmobstructie zijn gemeld.
Lever- en galaandoeningen
Zeer zeldzame gevallen van hepatitis, soms fataal, zijn voornamelijk gemeld bij patiënten met een reeds bestaande leverziekte.
Huid- en onderhuidaandoeningen
Gevallen van lupus erythematosus huid- en bulleuze erupties zoals erythema multiforme, Stevens-Johnson-syndroom, toxische epidermale necrolyse. In sommige gevallen kunnen andere bijkomende factoren hebben bijgedragen aan de ontwikkeling van deze effecten. Schlerodermie-achtige manifestaties, gewoonlijk voorafgegaan door perifeer lymfoedeem, zijn gemeld tijdens de behandeling met docetaxel.
Algemene aandoeningen en toedieningsplaatsstoornissen
Stralingsverschijnselen zijn zelden gemeld.
Vochtretentie was niet geassocieerd met acute episodes van oligurie of hypotensie. Uitdroging en longoedeem zijn zelden gemeld.
04.9 Overdosering
Er zijn enkele gevallen van overdosering gemeld Er is geen antidotum bekend voor overdosering met docetaxel. In het geval van een overdosis moet de patiënt op een gespecialiseerde afdeling worden gehouden en moeten de vitale functies nauwlettend worden gecontroleerd.In het geval van een overdosis kan een verergering van bijwerkingen worden verwacht. De belangrijkste te verwachten complicaties bij overdosering zijn beenmergsuppressie, perifere neurotoxiciteit en mucositis. Patiënten dienen zo snel mogelijk therapeutisch G-CSF te krijgen na tekenen van overdosering. Indien nodig moeten andere passende symptomatische maatregelen worden genomen.
05.0 FARMACOLOGISCHE EIGENSCHAPPEN
05.1 Farmacodynamische eigenschappen
Farmacotherapeutische categorie: taxanen, ATC-code: L01CD 02
Preklinische gegevens:
Docetaxel is een antineoplastisch geneesmiddel dat de aggregatie van tubuline in stabiele microtubuli bevordert en hun afbraak remt, wat leidt tot een significante afname van de vrije tubuline. De binding van docetaxel aan microtubuli verandert het aantal protofilamenten niet. in vitro het verbreekt het cellulaire microtubulaire systeem dat essentieel is voor vitale celfuncties zoals mitose en interfase.
de docetaxel in vitro het is cytotoxisch voor verschillende tumorlijnen van muizen en mensen en menselijke tumoren die recentelijk zijn verwijderd in de uitgevoerde klonogene tests. Docetaxel bereikt hoge en langdurige intracellulaire concentraties. Verder is docetaxel actief op sommige cellijnen (maar niet alle) die een overmaat p-glycoproteïne tot expressie brengen, gecodeerd door het multidrug-resistentiegen. In vivo, heeft docetaxel experimenteel een breed werkingsspectrum tegen gevorderde muizentumoren en getransplanteerde menselijke tumoren, ongeacht het doseringsschema.
Klinische gegevens:
Borstkanker
TAXOTERE in combinatie met doxorubicine en cyclofosfamide: adjuvante behandeling.
Patiënten met operabele knooppositieve borstkanker (TAX 316)
Gegevens uit een open-label, gerandomiseerde multicenter studie ondersteunen het gebruik van docetaxel als adjuvante behandeling bij patiënten met operabele klierpositieve borstkanker en KPS 3 80% in de leeftijd van 18 tot 70 jaar. Na stratificatie naar aantal positieve lymfeklieren (1-3 , meer dan 4), werden 1491 patiënten gerandomiseerd om docetaxel 75 mg/m2 toegediend te krijgen 1 uur na doxorubicine 50 mg/m2 en cyclofosfamide 500 mg/m2 (TAC-groep) of doxorubicine 50 mg/m2 gevolgd door fluorouracil 500 mg/m2 en cyclofosfamide 500 mg/m2 (FAC-groep). Beide regimes werden eenmaal per 3 weken toegediend gedurende 6 cycli. Docetaxel werd toegediend als een 1 uur durende infusie, alle andere geneesmiddelen werden toegediend als intraveneuze bolus op dag 1. G-CSF werd toegediend als secundaire profylaxe voor patiënten met gecompliceerde neutropenie (febriele neutropenie, langdurige neutropenie of infectie).
Patiënten in de TAC-groep kregen antibioticaprofylaxe met ciprofloxacine 500 mg oraal of gelijkwaardige antibiotica tweemaal daags gedurende 10 dagen, beginnend op dag 5 van elke cyclus. In beide groepen kregen patiënten die positief waren voor oestrogeen- en/of progestageenreceptoren na de laatste chemotherapiekuur 5 jaar lang 20 mg tamoxifen/dag adjuvante bestralingstherapie volgens de richtlijnen die in elk deelnemend centrum gelden en aan 69 % van de patiënten die TAC kregen en tot 72% van de patiënten die FAC kregen.
Een tussentijdse analyse werd uitgevoerd bij een mediane follow-up van 55 maanden. De ziektevrije overleving was significant verhoogd in de TAC-groep in vergelijking met de FAC-groep.
De incidentie van recidief na 5 jaar was verminderd bij patiënten die TAC kregen vergeleken met degenen die FAC kregen (respectievelijk 25% versus 32%), dwz een absolute risicovermindering van 7% (p = 0,001). De totale overleving na 5 jaar was ook significant verhoogd met TAC vergeleken met FAC (respectievelijk 87% versus 81%) dwz een absolute vermindering van 6% van het risico op overlijden (p = 0,008). De subgroepen van patiënten die werden behandeld met TAC in overeenstemming met de belangrijkste prognostische factoren die a priori waren gedefinieerd, werden geanalyseerd:
* hazard ratio kleiner dan 1 geeft aan dat TAC geassocieerd is met ziektevrije overleving en algehele overleving superieur aan FAC
Bij de tussentijdse analyse werd het therapeutische voordeel van TAC bij patiënten met 4 of meer lymfeklieren (37% van de bevolking) niet aangetoond. Het therapeutische voordeel van TAC lijkt minder evident dan dat waargenomen bij patiënten met 1 tot 3 positieve lymfeklieren De risico-batenverhouding bij patiënten met 4 of meer positieve lymfeklieren was daarom in dit stadium van de analyse niet volledig gedefinieerd.
Patiënten met operabele kliernegatieve borstkankerkandidaten voor chemotherapie (GEICAM 9805):
Gegevens van een multicenter, open, gerandomiseerde studie ondersteunen het gebruik van TAXOTERE voor adjuvante therapie bij patiënten met operabele kliernegatieve borstkanker die in aanmerking komen voor chemotherapie.1060 patiënten werden gerandomiseerd om TAXOTERE 75 mg/m2 toegediend 1 uur na doxorubicine te krijgen.50 mg/m2 en cyclofosfamide 500 mg/m2 (539 patiënten in de TAC-arm), of doxorubicine 50 mg/m2 gevolgd door fluorouracil 500 mg/m2 en cyclofosfamide 500 mg/m2 (521 patiënten in de FAC-arm) als adjuvante therapie bij kanker van de operabele borst-negatieve lymfeklier met hoog risico op terugval volgens de St. Gallen-criteria van 1998 (tumorgrootte > 2 cm en/of ER- en PR-negatief en/of hoge histologische/nucleaire graad (graad 2 tot 3) en/of leeftijd
De mediane duur van de follow-up was 77 maanden. Er werd een statistisch significante toename van de ziektevrije overleving aangetoond voor de TAC-arm in vergelijking met de FAC-arm. Patiënten die werden behandeld met TAC hadden een vermindering van 32% van het risico op terugval in vergelijking met degenen die werden behandeld met FAC (hazard ratio = 0,68, 95% BI (0,49-0,93), p = 0,01). De totale overleving (OS) was ook langer in de TAC-arm met een vermindering van 24% van het risico op overlijden voor patiënten die met TAC werden behandeld in vergelijking met FAC (hazard ratio = 0,76, 95% BI (0,46-1, 26, p = 0,29) De verdeling van de totale overleving was echter niet significant verschillend tussen de twee groepen.
Subgroepen van patiënten die werden behandeld met TAC werden geanalyseerd, verdeeld volgens prospectief gedefinieerde belangrijkste prognostische factoren (zie onderstaande tabel):
Subgroepanalyse - Studie van adjuvante therapie bij patiënten met kliernegatieve borstkanker (intent-to-treat-analyse)
* een hazard ratio (TAC/FAC) van minder dan 1 geeft aan dat TAC geassocieerd is met een langere ziektevrije overleving dan FAC.
Verkennende subgroepanalyses voor ziektevrije overleving bij patiënten die voldeden aan de St. Gallen-criteria van 2009 voor chemotherapie - (ITT-populatie) werden uitgevoerd en worden weergegeven in de onderstaande tabel:
TAC = docetaxel, doxorubicine en cyclofosfamide
FAC = 5-fluorouracil, doxorubicine en cyclofosfamide
BI = betrouwbaarheidsinterval; ER = oestrogeenreceptor
PR = progesteronreceptor
a ER/PR-negatief of Graad 3 of tumorgrootte > 5 cm
De hazard ratio werd geschat met het Cox proportionele risicomodel, waarbij de therapiegroep als factor werd gebruikt.
TAXOTERE als enige behandeling
Twee fase III gerandomiseerde vergelijkende studies met docetaxel in aanbevolen doseringen en een regime van 100 mg/m2 elke 3 weken werden uitgevoerd bij patiënten met uitgezaaide borstkanker, waarvan 326 na falen van alkylerende behandeling en 392 na falen van een behandeling met antracyclines.
Bij patiënten bij wie behandeling met alkylerende middelen niet effectief bleek te zijn, werd docetaxel vergeleken met doxorubicine (75 mg/m2 elke 3 weken). Docetaxel verhoogde het responspercentage (52% versus 37%, p = 0,01) en verminderde de responstijd (12 weken versus 23 weken, p = 0,007), zonder de overlevingstijd te veranderen (15 maanden voor docetaxel versus 14 maanden voor doxorubicine, p = 0,38) of tijd tot progressie (27 weken voor docetaxel versus 23 weken voor doxorubicine, p = 0,54). Drie met docetaxel behandelde patiënten (2%) moesten de behandeling staken vanwege vochtretentie, terwijl 15 met doxorubicine behandelde patiënten (9%) moesten stoppen vanwege harttoxiciteit (drie overlijdens door congestief hartfalen).
Bij patiënten bij wie de behandeling met antracycline niet effectief was, werd docetaxel vergeleken met de combinatie van mitomycine C en vinblastine (12 mg/m2 elke 6 weken en 6 mg/m2 elke 3 weken). Docetaxel verhoogde het responspercentage (33% vs 12%, p
Het verdraagbaarheidsprofiel van docetaxel tijdens deze twee fase III-onderzoeken was in overeenstemming met het verdraagbaarheidsprofiel dat werd gevonden in de fase II-onderzoeken (zie rubriek 4.8).
Een gerandomiseerde, open-label, multicenter fase III-studie waarin docetaxel monotherapie werd vergeleken met paclitaxel werd uitgevoerd bij de behandeling van gevorderde borstkanker bij patiënten bij wie eerdere therapie al een "antracycline" omvatte. In totaal werden 449 patiënten gerandomiseerd om ofwel docetaxel monotherapie te krijgen. mg/m2 als infusie van 1 uur of paclitaxel 175 mg/m2 als infusie van 3 uur, waarbij de twee behandelingen elke 3 weken worden toegediend.
Docetaxel verlengde de mediane tijd tot progressie (24,6 weken vs 15,6 weken; p
TAXOTERE in combinatie met doxorubicine
Er werd een gerandomiseerde fase III-studie uitgevoerd bij 429 patiënten met niet-voorbehandelde uitgezaaide kanker waarbij doxorubicine (50 mg/m2) in combinatie met docetaxel (75 mg/m2) (AT-arm) werd vergeleken met doxorubicine (60 mg/m2) in combinatie met cyclofosfamide (600 mg/m2) (AC-arm). Beide regimes werden elke drie weken op dag 1 toegediend.
De tijd tot progressie (TTP) was significant langer in de AT-arm vergeleken met die van de AC-arm, p = 0,0138. De mediane TTP was 37,3 weken (95% BI: 33,4 - 42,1) in de AT-arm en 31,9 weken (95% BI: 27,4 - 36,0) in de AC-arm.
Het waargenomen responspercentage was significant hoger in de AT-arm dan in de AC-arm, p = 0,009. Dit percentage was 59,3% (95% BI: 52,8 - 65,9) in de AT-arm vergeleken met 46,5% (95% BI: 39,8 - 53,2) in de AC-arm.
In deze studie had de AT-arm een hogere incidentie dan de AC-arm van ernstige neutropenie (90% vs. 68,6%), febriele neutropenie (33,3% vs. 10%), infecties (8% vs. 2,4%), diarree (7,5% vs. 1,4%), asthenie (8,5% versus 2,4%) en pijn (2,8% versus 0%). Aan de andere kant vertoonde de AC-arm een hogere incidentie van ernstige anemie dan de AT-arm (15,8% versus 8,5%) en een hogere incidentie van cardiale toxiciteit: congestief hartfalen (3,8% versus 2, 8%), absolute afname van LVEF 3 20% (13,1% vs. 6,1%), absolute afname in LVEF ≥ 30% (6,2% vs. 1,1%) Toxische dood trad op bij 1 patiënt in de AT-arm (congestief hartfalen) en bij 4 patiënten in de AC-arm (1 vanwege septische shock en 3 vanwege congestief hartfalen).
In beide armen was de kwaliteit van leven, gemeten met de EORTC-vragenlijst, vergelijkbaar en stabiel tijdens behandeling en follow-up.
TAXOTERE in combinatie met trastuzumab
Docetaxel in combinatie met trastuzumab is geëvalueerd bij de behandeling van patiënten met gemetastaseerde borstkanker met overexpressie van HER2 en die niet eerder chemotherapie hebben gekregen voor gemetastaseerde ziekte. 186 patiënten werden gerandomiseerd om docetaxel (100 mg/m2) met of zonder trastuzumab te krijgen; 60% van de patiënten kreeg eerder adjuvante chemotherapie met anthracyclines. Docetaxel met trastuzumab was effectief bij patiënten die al dan niet eerder adjuvante antracyclinetherapie hadden gekregen. De meest gebruikte test om HER2-positiviteit in dit centrale onderzoek te bepalen, was immunohistochemie (IHC). Fluorescentie in situ-assay (FISH) werd gebruikt voor een kleiner aantal patiënten. In deze studie had 87% van de patiënten een ziekte die IHC 3+ was en 95% van de ingeschreven patiënten had de ziekte van IHC 3+ en/of FISH-positief. De werkzaamheidsresultaten zijn samengevat in de onderstaande tabel:
TTP = tijd tot progressie; "ne" geeft aan dat het niet kan worden geschat of nog niet is
bereikt.
1 Intent-to-treat-populatie
2 Geschatte mediane overleving
TAXOTERE in combinatie met capecitabine
Gegevens uit een multicenter, gerandomiseerde, gecontroleerde klinische fase III-studie ondersteunen het gebruik van docetaxel in combinatie met capecitabine voor de behandeling van patiënten met lokaal gevorderde of gemetastaseerde borstkanker na falen van cytotoxische chemotherapie met een antracycline. In deze studie werden 255 patiënten gerandomiseerd voor behandeling met docetaxel (75 mg/m2 als een 1 uur durende intraveneuze infusie elke 3 weken) en capecitabine (1250 mg/m2 tweemaal daags gedurende 2 weken gevolgd door een rustperiode van 1 week.). 256 patiënten werden gerandomiseerd naar behandeling met alleen docetaxel (100 mg/m2 als intraveneuze infusie van 1 uur elke 3 weken). De overleving was superieur in de combinatiearm met docetaxel + capecitabine (p = 0,0126). De mediane overleving was 442 dagen (docetaxel + capecitabine) vergeleken met 352 dagen (alleen docetaxel). Het algehele objectieve responspercentage in de gehele gerandomiseerde populatie (beoordeling door de onderzoeker) was 41,6% (docetaxel + capecitabine) versus 29,7% (docetaxel alleen); p = 0,0058. De tijd tot ziekteprogressie was superieur in de combinatie-arm met docetaxel + capecitabine (p
Niet-kleincellige longkanker
Patiënten die eerder zijn behandeld met chemotherapie met of zonder radiotherapie
In een klinische fase III-studie waren bij voorbehandelde patiënten de tijd tot progressie (12,3 weken versus 7 weken) en de overleving significant verhoogd met docetaxel van 75 mg/m2 in vergelijking met Best Supportive Treatment (MTS).
De 1-jaarsoverleving was significant hoger met docetaxel (40%) dan met MTS (16%).
Er werd minder morfine gebruikt bij patiënten die werden behandeld met docetaxel van 75 mg/m2 (p niet-morfine-analgetica (p
Bij evalueerbare patiënten was het totale responspercentage 6,8% en de gemiddelde duur van de respons was 26,1 weken.
TAXOTERE in combinatie met platinaderivaten bij patiënten die nooit met chemotherapie zijn behandeld
In een fase III-onderzoek werden 1218 patiënten met inoperabele stadium IIIB of IV niet-kleincellige longkanker, met een Karnofsky Performance Status van 70% en hoger, die niet eerder chemotherapie hadden gekregen voor deze aandoening, gerandomiseerd naar docetaxel (T ) 75 mg / m2 als infusie van een uur, onmiddellijk gevolgd door cisplatine (TCis) 75 mg/m2 gedurende 30-60 minuten elke drie weken, docetaxel 75 mg/m2 als infusie van één uur in combinatie met carboplatine (AUC 6 mg/ml. min) gedurende 30-60 minuten elke drie weken, of vinorelbine (VCis) 25 mg/m2 toegediend gedurende 6-10 minuten op dag 1, 8, 15, 22 gevolgd door cisplatine 100 mg/m2 toegediend op de eerste dag van de cyclus herhaald elke 4 weken.
Gegevens over overleving, gemiddelde tijd tot progressie en responspercentage voor twee onderzoeksarmen worden weergegeven in de onderstaande tabel.
*: Gecorrigeerd voor meerdere vergelijkingen en gecorrigeerd voor stratificatiefactoren (ziektestadium en behandelgebied), gebaseerd op de evalueerbare patiëntenpopulatie.
Secundaire eindpunten waren onder meer verandering in pijn, globale beoordeling van de kwaliteit van leven door EuroQoL-5D, Lung Cancer Symptom Scale (LCSS) en verandering in de prestatiestatus van Karnofsky. De resultaten van deze doelstellingen bevestigden de resultaten van de primaire doelstellingen.
Voor de combinatie docetaxel/carboplatine was het niet mogelijk om gelijkwaardigheid of non-inferioriteit van werkzaamheid aan te tonen met betrekking tot de referentiebehandeling: de VCis-combinatie.
Prostaatkanker
De verdraagbaarheid en werkzaamheid van docetaxel in combinatie met prednison of prednisolon bij patiënten met hormoonresistente gemetastaseerde prostaatkanker werden geëvalueerd in een multicenter gerandomiseerde fase III-studie.In totaal werden 1006 patiënten met KPS 60 gerandomiseerd naar de volgende therapeutische groepen:
Docetaxel 75 mg/m2 elke 3 weken gedurende 10 cycli.
Docetaxel 30 mg/m2 wekelijks toegediend gedurende de eerste 5 weken van een cyclus van 6 weken voor in totaal 5 cycli.
Mitoxantron 12 mg/m2 elke 3 weken gedurende 10 cycli.
Alle drie de regimes werden toegediend in combinatie met prednison of prednisolon 5 mg tweemaal daags, continu.
Patiënten die om de drie weken docetaxel kregen, vertoonden een significant langere algehele overleving dan patiënten die met mitoxantron werden behandeld. De toename in overleving die wekelijks werd waargenomen in de met docetaxel behandelde groep was niet statistisch significant in vergelijking met de met mitoxantron behandelde controlegroep. De werkzaamheidsparameters verkregen in de met docetaxel behandelde groepen vergeleken met de controlegroep zijn samengevat in de volgende tabel:
† Gestratificeerde log rank test
* Limiet voor statistische significantie = 0,0175
** PSA: prostaatspecifiek antigeen
Aangezien docetaxel elke week een iets beter verdraagbaarheidsprofiel had dan docetaxel elke 3 weken, is het mogelijk dat sommige patiënten baat kunnen hebben bij wekelijkse docetaxeltherapie.
Er was geen statistisch significant verschil in algehele kwaliteit van leven tussen de behandelingsgroepen.
Adenocarcinoom van de maag
Er werd een multicenter, gerandomiseerd, open-label onderzoek uitgevoerd om de veiligheid en werkzaamheid van docetaxel te evalueren bij de behandeling van patiënten met gemetastaseerd adenocarcinoom van de maag, waaronder adenocarcinoom van de gastro-oesofageale overgang, die niet eerder chemotherapie hadden gekregen voor hun gemetastaseerde ziekte. In totaal werden 445 patiënten met KPS> 70 behandeld met docetaxel (T) (75 mg/m2 op dag 1) in combinatie met cisplatine (C) (75 mg/m2 op dag 1) en 5-fluorouracil (F) (750 mg/m2 per dag gedurende 5 dagen) of met cisplatine (100 mg/m2 op dag 1) en 5-fluorouracil (1000 mg/m2 per dag gedurende 5 dagen). De duur van een behandelingscyclus was 3 weken voor de TCF-arm en 4 weken voor de CF-arm. Het gemiddelde aantal toegediende cycli per patiënt was 6 (met een bereik van 1-16) voor de TCF-arm en 4 (met een bereik van 1-12) voor de CF-arm. Tijd tot progressie (TTP) was het primaire eindpunt. De vermindering van het risico op progressie was 32,1% en was geassocieerd met een significant langere TTP (p = 0,0004) voor de TCF-arm. De totale overleving was ook significant langer (p = 0,0201) voor de TCF-arm met een risicoreductie van mortaliteit van 22,7% De werkzaamheidsresultaten zijn samengevat in de volgende tabel:
Werkzaamheid van docetaxel bij de behandeling van patiënten met maagadenocarcinoom
* Niet-gestratificeerde logrank-test
Subgroepanalyses voor leeftijd, geslacht en ras gaven consequent de voorkeur aan de TCF-arm boven de CF-arm.
Een bijgewerkte overlevingsanalyse uitgevoerd met een gemiddelde follow-uptijd van 41,6 maanden toonde geen statistisch significant verschil meer, zij het altijd in het voordeel van het TCF-regime en benadrukte dat het voordeel van TCF boven CF duidelijk is. -omhoog.
Over het algemeen wezen de resultaten op het gebied van kwaliteit van leven (QoL) en klinische voordelen consequent op verbetering in het voordeel van de TCF-arm. Patiënten die werden behandeld met TCF hadden een 5% langere tijd tot verslechtering van de gezondheidsstatus op de QLQ-C30-vragenlijst (p = 0,0121) en een langere tijd tot definitieve verslechtering van de Karnofsky-prestatiestatus (p = 0, 0088) in vergelijking met patiënten behandeld met CF .
Hoofd-halskanker
Inductiechemotherapie gevolgd door radiotherapie (TAX 323)
De veiligheid en werkzaamheid van docetaxel bij de inductiebehandeling van patiënten met plaveiselcelcarcinoom van het hoofd-halsgebied (SCCHN) werden geëvalueerd in een open-label, multicenter gerandomiseerd fase III-onderzoek (TAX323). gevorderd inoperabel SCCHN met WHO-prestatiestatus 0 - 1 werden gerandomiseerd van één naar twee armen.Patiënten die docetaxel (T) 75 mg / m2 kregen gevolgd door cisplatine (P) 75 mg / m2 gevolgd door 5-fluorouracil (F) 750 mg / m2 per dag als continu infuus gedurende 5 dagen Dit doseringsschema wordt elke drie weken gedurende 4 cycli toegediend, na 2 cycli werd een minimale respons (> 25% tumorkrimp gemeten in twee dimensies) waargenomen. minimale interval van 4 weken en maximaal zeven weken, patiënten bij wie de ziekte niet voortschrijdt, krijgen gedurende 7 weken radiotherapie (RT), in overeenstemming met de institutionele richtlijnen. en (TPF/RT). Patiënten in de vergelijkingsarm kregen cisplatine (P) 100 mg/m2 gevolgd door 5-fluorouracil (F) 1000 mg/m2 dagelijks gedurende 5 dagen. Dit doseringsschema werd elke drie weken gedurende 4 cycli toegediend als na 2 cycli ten minste één respons (≥ 25% vermindering van de gemeten tweedimensionale tumorgrootte) werd waargenomen. Aan het einde van de chemotherapie, met een minimum interval van 4 weken en een maximum interval van 7 weken, kregen patiënten bij wie de ziekte niet was gevorderd gedurende 7 weken radiotherapie (RT) volgens de richtlijn (PF/RT). Locoregionale bestralingstherapie werd toegepast op een conventionele fractie (1,8 Gy-2,0 Gy eenmaal daags, 5 dagen per week voor een totale dosis van 66 tot 70 Gy), of op versnelde/hypergefractioneerde radiotherapieregimes (tweemaal daags, met een minimum interval van fracties van 6 uur, van 5 dagen per week). Een totaal van 70 Gy werd voorgesteld voor de versnelde regimes en 74 Gy voor de hypergefractioneerde schema's. Chirurgische resectie is toegestaan na chemotherapie, voor of na radiotherapie. Patiënten in de TPF-arm kregen oraal ciprofloxacine 500 mg tweemaal daags gedurende 10 dagen, beginnend op dag 5 van elke cyclus, of equivalent, als profylaxe. Het primaire eindpunt in deze studie, progressievrije overleving (PFS), was significant langer in de TPF-arm dan in de PF-arm, p = 0,0042 (mediane PFS: respectievelijk 11,4 versus 8,3 maanden) met een mediane tijd van 33,7 maanden. overleving was ook significant langer voor de TPF-arm in vergelijking met de PF (mediane OS: respectievelijk 18,6 versus 14,5 maanden) met een afname van 28% van het sterfterisico, p = 0,0128. De werkzaamheidsresultaten worden weergegeven in de onderstaande tabel:
Werkzaamheid van docetaxel bij de inductiebehandeling van patiënten met lokaal gevorderd inoperabel SCCHN. (Intent-to-Treat-analyse).
Hazard ratio lager dan 1 ten gunste van de combinatie docetaxel + cisplatine + 5-FU
* Cox-model (aanpassing voor primaire tumorplaats, stadiëring op T en N en PS-WHO)
** Logrank-test
*** Chikwadraattoets
Parameters om de kwaliteit van leven te definiëren.
Patiënten die met TPF worden behandeld, vertonen een significant verminderde verslechtering van hun algehele gezondheid in vergelijking met patiënten die met PF zijn behandeld (p = 0,01, met gebruikmaking van de EORTC QLQ-C30-schaal).
Parameters om de klinische voordelen te definiëren
De prestatieschaal voor hoofd en nek (PSS-HN), die gericht was op het meten van spraakverstaan, de mogelijkheid om in het openbaar te eten en de normaliteit van het dieet, bleek significant gunstig te zijn voor de TPF-arm in vergelijking met de PF-arm . De mediane tijd tot de eerste verslechtering van de WHO-prestatieconditie was significant langer in de TPF-arm dan in de PF-arm. De pijnintensiteitsschaal laat in beide groepen verbetering zien tijdens de behandeling, wat aangeeft dat pijnbestrijding adequaat is.
Inductiechemotherapie gevolgd door chemo-radiotherapie (TAX324)
De veiligheid en werkzaamheid van docetaxel bij de inductiebehandeling van patiënten met lokaal gevorderd plaveiselcelcarcinoom in het hoofd-halsgebied (SCCHN) werd geëvalueerd in een fase III, gerandomiseerd, open-label, multicenter klinisch onderzoek (TAX 324). lokaal gevorderde SCCHN met WHO-prestatiestatus 0 of 1. De onderzoekspopulatie omvatte ook technisch inoperabele patiënten, patiënten met een lage kans op succesvolle chirurgische resectie en patiënten die gericht waren op orgaanconservering. veiligheids- en werkzaamheidsprofiel werd alleen rekening gehouden met de overlevingseindpunten, terwijl het succes bij orgaanconservering niet formeel werd overwogen.
Met docetaxel behandelde patiënten kregen docetaxel (T) 75 mg/m2 als intraveneuze infusie op dag 1 gevolgd door cisplatine (P) 100 mg/m2 toegediend als intraveneuze infusie van 30 minuten tot drie uur, gevolgd door continue intraveneuze infusie van 5- fluorouracil (F) 1000 mg/m2/dag van dag 1 tot dag 4. De cycli werden elke drie weken herhaald gedurende 3 cycli.
Alle patiënten die geen ziekteprogressie vertoonden, zouden volgens protocol (TPF/CRT) chemoradiotherapie (CRT) krijgen. Patiënten in de vergelijkingsarm kregen cisplatine (P) 100 mg/m2 toegediend als een infusie van 30 minuten tot drie uur op dag 1, gevolgd door 5-fluorouracil (F) 1000 mg/m2/dag van dag 1 tot dag 5. Cycli werden elke drie weken herhaald gedurende 3 cycli. Alle patiënten die geen ziekteprogressie vertoonden, zouden protocolconforme CRT's (PF/CRT) krijgen.
Patiënten in beide behandelarmen kregen 7 dagen CRT na inductiechemotherapie met een minimum interval van 3 weken en niet langer dan 8 weken na het begin van de laatste cyclus (dag 22 tot dag 56. Tijdens radiotherapie werd carboplatine (AUC 1.5) toegediend als een één uur durende intraveneuze infusie voor maximaal 7 doses. De straling werd toegediend met een hoogspanningsinstrument met dagelijkse fractionering (2Gy per dag, 5 dagen per week gedurende 7 weken, voor een totale dosis van 70-72 Gy). Chirurgie op de plaats van de primaire tumor en/of nek kan op elk moment worden overwogen na voltooiing van de CRT. Alle onderzoekspatiënten in de docetaxel-arm kregen antibioticaprofylaxe. Het primaire werkzaamheidseindpunt van deze studie, overleving (OS) was significant langer (log-rank test p = 0,0058) met het docetaxelbevattende regime in vergelijking met PF (mediane OS: respectievelijk 70,6 vs. 30,1 maanden), met een vermindering van 30% in het risico op overlijden door PF (hazard ratio (HP) = 0,70, 95% betrouwbaarheidsinterval (BI) = 0,54-0,90) bij een mediane follow-up van 41,9 maanden Het secundaire eindpunt, PFS, toonde een afname van 29% in de risico op progressie of overlijden en een verbetering van de mediane PFS van 22 maanden (35,5 maanden voor TPF en 13,1 maanden voor PF). Dit was ook statistisch significant met een HR van 0,71, 95% BI 0,56-0,90; log-rank test p = 0,004. De werkzaamheidsresultaten worden weergegeven in de volgende tabel:
Hazard ratio lager dan 1 in het voordeel van de combinatie docetaxel + cisplatine + 5-fluorouracil
* log rank test aanpassing
** log rank test aanpassing, geen aanpassing voor meerdere vergelijkingen
*** Chi-kwadraattoets, geen correctie voor meerdere vergelijkingen
NVT - niet van toepassing
Het Europees Geneesmiddelenbureau heeft vrijstelling verleend van de verplichting om de resultaten te verstrekken van onderzoeken met TAXOTERE bij alle subgroepen van patiënten van de pediatrische populatie met borstkanker, niet-kleincellige longkanker, prostaatkanker, maagkanker en hoofd-halskanker, met uitzondering van minder gedifferentieerd type II en type III nasofarynxcarcinoom (zie rubriek 4.2 voor informatie over pediatrisch gebruik).
05.2 "Farmacokinetische eigenschappen
De farmacokinetiek van docetaxel is onderzocht bij kankerpatiënten na toediening van 20-115 mg/m2 in onderzoeken in fase I. Het kinetische profiel van docetaxel is niet dosisafhankelijk en komt overeen met een farmacokinetisch model met drie compartimenten, met halfwaardetijden per fase a, b en b respectievelijk van 4 min., 36 min. en 11.1 uur. De late fase is deels te wijten aan de relatief trage terugkeer van docetaxel uit het perifere compartiment. Na toediening van 100 mg/m2 als een één uur durende infusie, werd een gemiddelde piekplasmaspiegel van 3,7 mcg/ml verkregen, met een overeenkomstige AUC van 4,6 u mcg/ml.De gemiddelde totale klaringswaarden en het distributievolume bij steady-state waren 21 1 / h / m2 en 113 L. Interindividuele veranderingen in totale klaring waren ongeveer 50% Docetaxel is voor meer dan 95% gebonden aan plasma-eiwitten.
Een studie met 14C-docetaxel werd uitgevoerd bij drie kankerpatiënten. Docetaxel werd geëlimineerd in zowel urine als feces door cytochroom P450-gemedieerde oxidatie van de tertbutylestergroep; binnen zeven dagen wordt ongeveer 6% en 75% van de toegediende radioactiviteit uitgescheiden in respectievelijk de urine en feces. Ongeveer 80% van de radioactiviteit die in de feces wordt aangetroffen, wordt binnen de eerste 48 uur uitgescheiden als één belangrijke metaboliet en drie inactieve minder belangrijke metabolieten en zeer kleine hoeveelheden van het oorspronkelijke geneesmiddel.
Er werd een farmacokinetisch populatieonderzoek uitgevoerd bij 577 patiënten. De farmacokinetische parameters berekend door het model lagen zeer dicht bij die waargenomen in de fase I-onderzoeken. De farmacokinetiek van docetaxel werd niet gewijzigd door de leeftijd of het geslacht van de patiënt. Bij een klein aantal patiënten (n = 23) met biochemische resultaten. dysfunctie (ALAT, ASAT 3 1,5 keer de bovengrens van normaal, geassocieerd met alkalische fosfatase 3 2,5 bovengrens van normaal), totale klaring daalde gemiddeld met 27% (zie rubriek 4.2) Docetaxelklaring wordt niet beïnvloed bij patiënten met lichte of matige vochtretentie Er zijn geen gegevens beschikbaar over patiënten met ernstige vochtretentie.
Bij gebruik in combinatie heeft docetaxel geen invloed op de klaring van doxorubicine en de plasmaspiegels van doxorubicinol (een metaboliet van doxorubicine). De farmacokinetiek van docetaxel, doxorubicine en cyclofosfamide wordt niet beïnvloed door hun gelijktijdige toediening.
Een fase I-onderzoek waarin de effecten van capecitabine op de farmacokinetiek van docetaxel en vice versa werden geëvalueerd, toonde aan dat er geen effect is van capecitabine op de farmacokinetiek van docetaxel (Cmax en AUC) en dat er geen effect is van docetaxel op de farmacokinetiek van een metaboliet. relevant voor capecitabine, 5 "-DFUR.
De klaring van docetaxel in combinatietherapie met cisplatine was vergelijkbaar met die waargenomen tijdens monotherapie. Het farmacokinetische profiel van cisplatine dat kort na de docetaxel-infusie wordt toegediend, is vergelijkbaar met dat waargenomen met cisplatine alleen.
De gecombineerde toediening van docetaxel, cisplatine en 5-fluorouracil bij 12 patiënten met solide tumoren had geen invloed op de farmacokinetiek van de afzonderlijke geneesmiddelen.
Het effect van prednison op de farmacokinetiek van docetaxel toegediend met standaard premedicatie met dexamethason werd onderzocht bij 42 patiënten.Er werd geen effect van prednison op de farmacokinetiek van docetaxel waargenomen.
05.3 Gegevens uit het preklinisch veiligheidsonderzoek
Het carcinogene potentieel van docetaxel is niet onderzocht.
Docetaxel bleek mutageen te zijn in de test in vitro van chromosomale aberratie in CHO-K1-cellen e in vivo in de micronucleus-test van de muis. Docetaxel is echter niet mutageen in de Ames-test of de CHO/HGPRT-genmutatietest. Deze resultaten zijn consistent met de farmacologische activiteit van docetaxel.
Bijwerkingen op de mannelijke geslachtsorganen, waargenomen in toxiciteitsstudies bij knaagdieren, suggereren dat docetaxel de mannelijke vruchtbaarheid kan aantasten.
06.0 FARMACEUTISCHE INFORMATIE
06.1 Hulpstoffen
Flacon met concentraat:
polysorbaat 80, citroenzuur.
flacon met oplosmiddel:
95% ethanol, water voor injecties.
06.2 Incompatibiliteit
Het geneesmiddel mag niet worden gemengd met andere producten dan die vermeld in rubriek 6.6.
06.3 Geldigheidsduur
2 jaar.
Voorgemengde oplossing: de voorverdunde oplossing bevat 10 mg/ml docetaxel en moet onmiddellijk na bereiding worden gebruikt, zelfs als de chemisch-fysische stabiliteit van deze oplossing is aangetoond gedurende een periode van 8 uur indien bewaard tussen + 2° C en +8 ° C of bij kamertemperatuur (beneden 25 ° C).
Oplossing voor infusie: De oplossing voor infusie, bewaard bij kamertemperatuur (beneden 25°C), moet binnen 4 uur worden gebruikt.
06.4 Speciale voorzorgsmaatregelen bij bewaren
Niet bewaren boven 25°C of beneden 2°C.
Bewaar in de originele verpakking om het uit de buurt van licht te houden.
Voor de bewaarcondities van het verdunde geneesmiddel, zie rubriek 6.3.
06.5 Aard van de primaire verpakking en inhoud van de verpakking
Elke blisterverpakking bevat:
één injectieflacon met een enkelvoudige dosis concentraat en één injectieflacon met een enkelvoudige dosis oplosmiddel.
Injectieflacon TAXOTERE 20 mg/0,5 ml concentraat voor oplossing voor infusie:
7 ml Type I heldere glazen injectieflacon met groene flip-off dop.
De injectieflacon bevat een oplossing van docetaxel in 0,5 ml polysorbaat 80 en een concentratie van 40 mg/ml (vulvolume: 24,4 mg/0,61 ml). Dit vulvolume is tijdens de ontwikkeling van TAXOTERE vastgesteld om het vloeistofverlies tijdens de bereiding van de voorverdunde oplossing door schuimvorming, hechting aan de flaconwanden en 'dode ruimte' te compenseren. De overvulling zorgt ervoor dat na de verdunning met de gehele inhoud van de flacon met oplosmiddel die bij TAXOTERE is geleverd, is het minimale extraheerbare volume van de voorverdunde oplossing 2 ml, die 10 mg/ml docetaxel bevat, wat overeenkomt met de op het etiket vermelde inhoud van 20 mg/0,5 ml per injectieflacon.
Flacon met oplosmiddel:
Type I heldere glazen injectieflacon van 7 ml met kleurloze heldere flip-off dop.
De injectieflacon met oplosmiddel bevat 1,5 ml 13% (g/w) oplossing van 95% ethanol in water voor injecties (vulvolume: 1,98 ml). Door de volledige inhoud van de injectieflacon met oplosmiddel toe te voegen aan die van TAXOTERE 20 mg/0,5 ml, concentraat voor oplossing voor infusie, zorgt u ervoor dat een voorgemengde oplossing wordt verkregen met een concentratie van 10 mg/ml docetaxel.
06.6 Instructies voor gebruik en verwerking
TAXOTERE is een antineoplastisch geneesmiddel en, net als bij andere potentieel toxische producten, is voorzichtigheid geboden bij het hanteren en bereiden van oplossingen. Het gebruik van handschoenen wordt aanbevolen Als TAXOTERE in geconcentreerde, voorverdunde vorm of oplossing voor infusie in contact komt met de huid, was dan onmiddellijk en grondig met water en zeep Als TAXOTERE in geconcentreerde, voorverdunde vorm of oplossing voor infusie in contact komen met de slijmvliezen, onmiddellijk en grondig wassen met water.
Voorbereiding voor intraveneuze toediening
a) Bereiding van de gebruiksklare oplossing van TAXOTERE (10 mg docetaxel / ml)
Als de injectieflacons in de koelkast worden bewaard, laat het vereiste aantal dozen TAXOTERE dan 5 minuten op kamertemperatuur (beneden 25°C).
Gebruik een maatspuit met naald om de volledige inhoud van de injectieflacon met oplosmiddel voor TAXOTERE op te zuigen door de injectieflacon gedeeltelijk om te keren.
Injecteer de volledige inhoud van de spuit in de overeenkomstige injectieflacon met TAXOTERE.
Verwijder de spuit en naald en meng de oplossing handmatig door deze gedurende 45 seconden herhaaldelijk om te keren. Niet schudden.
Laat de injectieflacon met de voorverdunde oplossing 5 minuten staan bij kamertemperatuur (beneden 25°C) en controleer vervolgens of de oplossing helder en homogeen is. (Schuimvorming is zelfs na 5 minuten normaal vanwege het polysorbaat 80-gehalte in de formulering).
De voorverdunde oplossing bevat 10 mg/ml docetaxel en moet onmiddellijk na bereiding worden gebruikt, ook als de chemisch-fysische stabiliteit van deze oplossing is aangetoond gedurende een periode van 8 uur indien bewaard tussen + 2 ° C en + 8 ° C of bij kamertemperatuur (beneden 25 ° C).
b) Bereiding van de oplossing voor infusie
Er kunnen meerdere injectieflacons met voorverdunde oplossing nodig zijn om de vereiste dosis voor de patiënt te verkrijgen. Op basis van de dosis die nodig is voor de patiënt, uitgedrukt in mg, trekt u aseptisch het overeenkomstige volume voorverdunde oplossing met 10 mg/ml docetaxel op uit een geschikt aantal injectieflacons met voorverdunde oplossing met behulp van een maatspuit met naald. Voor een dosis van 140 mg docetaxel moet bijvoorbeeld 14 ml docetaxel voorverdunde oplossing worden opgezogen. Injecteer het benodigde volume voorverdunde oplossing in een zak of fles van 250 ml die 5% glucose-oplossing of oplossing voor infusie met 9 mg/ml natriumchloride (0,9%) bevat.
Als een dosis docetaxel hoger dan 200 mg nodig is, gebruik dan een groter volume van de oplossing voor infusie, zodat de concentratie docetaxel niet hoger wordt dan 0,74 mg/ml. Meng de zak of fles handmatig met een draaiende beweging.
De TAXOTERE-oplossing voor infusie moet binnen 4 uur worden gebruikt en moet aseptisch worden toegediend als een infusie van 1 uur, bij kamertemperatuur (beneden 25°C) en onder normale lichtomstandigheden.
Zoals met alle producten voor parenteraal gebruik, moeten de voorverdunde oplossing en de perfusie-oplossing van TAXOTERE vóór gebruik visueel worden onderzocht, oplossingen die precipitaten bevatten, moeten worden weggegooid.
Ongebruikte producten en afval afkomstig van dit geneesmiddel moeten worden vernietigd in overeenstemming met de lokale wettelijke voorschriften.
07.0 HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Aventis Pharma S.A., 20 Avenue Raymond Aron, 92165 Antony Cedex, Frankrijk
08.0 NUMMER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
EU / 1/95/002/001
09.0 DATUM VAN EERSTE VERGUNNING OF VERLENGING VAN DE VERGUNNING
Datum eerste vergunning: 27 november 1995
Datum van laatste verlenging: 27 november 2005.