Sommige functies van Huntington kunnen worden beheerd met:
- Logopedie, psychotherapie en cognitieve revalidatie kunnen zowel de lichamelijke als de psychische symptomen van de ziekte verbeteren. Deze therapieën zijn met name nuttig om de communicatie en het autonoom uitvoeren van dagelijkse activiteiten te bevorderen. Een beter begrip van gedrags- en cognitieve stoornissen kan ook helpen bij het ontwikkelen van strategieën om zich aan te passen aan de veranderingen die worden veroorzaakt door de progressie van de ziekte van Huntington;
- Fysiotherapie en regelmatige lichaamsbeweging: dragen bij tot het behoud van de bewegingscoördinatie. In de vroege stadia van de ziekte wordt zachte fysieke activiteit (zwemmen, wandelen, enz.) aanbevolen;
- Gebruik van specifieke hulpmiddelen om ZvH-patiënten, die coördinatieproblemen hebben, te helpen zelfstandig te lopen;
- Medicijnen: Ze zijn geïndiceerd wanneer belangrijke symptomen optreden. Chorea en agitatie kunnen bijvoorbeeld gedeeltelijk worden onderdrukt met geneesmiddelen die dopaminereceptoren blokkeren of uitputten. Veel geneesmiddelen kunnen echter bijwerkingen veroorzaken en bij verschillende patiënten ook verschillende effecten hebben. Daarom moet de ideale balans van medicamenteuze therapie worden vastgesteld. per geval door de specialist, op basis van symptomen en individuele respons op behandelingen.
, bij de behandeling van de ziekte van Huntington. De klinische fase is zeer veeleisend, vooral omdat de ziekte een langzame progressie heeft en een "brede klinische heterogeniteit". Er zijn schalen voor evaluatie van de ziekte van Huntington en ze zijn bijna hetzelfde in alle klinieken. voorspellende genetica, biedt het de mogelijkheid om een behandeling te proberen tijdens de beginfase van de ziekte. Momenteel zijn de studies gericht op het zoeken naar gevoelige en stabiele biormarkers van verandering, om in te grijpen bij de eerste manifestaties van de ziekte.
Momenteel hebben neuroimaging-technieken de beste biomarkers geboden tijdens de prodromale fase (die voorafgaat aan de klinische symptomen van de ziekte); bovendien zorgen ze voor een correlatie tussen de therapieën die worden uitgevoerd op diermodellen en op mensen.
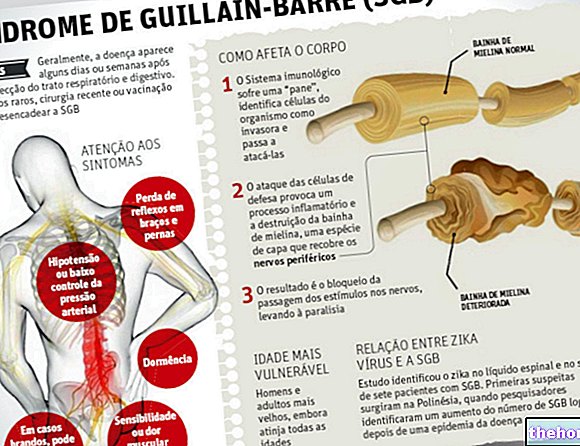
Zoals vermeld, is striatumatrofie vroeg en vordert het in de loop van de ziekte.Andere hersengebieden, zoals subcorticale en corticale witte stofstructuren, blijken ook te worden aangetast in de prodromale periode.
Door functionele beeldvorming kan het ook bepaalde afwijkingen bij individuen identificeren tijdens de prodromale periode.Deze techniek kan ook gevoelig genoeg zijn om detecteerbare structuuronregelmatigheden of gedragsveranderingen te identificeren.
Ten slotte zou de identificatie van moleculaire biomarkers, zoals lactaat of andere cellulaire stressproducten, mogelijk kunnen worden gemaakt dankzij magnetische resonantiespectroscopietechnieken.
de selectieve degeneratie van neuronen bij de ziekte van Huntington is nog niet volledig opgehelderd; daarom is het nodig om mogelijke nieuwe therapeutische strategieën te onderzoeken. In het bijzonder is gevonden dat er bij de ziekte van Huntington een selectief verlies is van cannabinoïdereceptoren van het CB1-type in de basale ganglia, wat een van de vroegste neurochemische veranderingen is. Om deze reden onderzoeken momenteel onderzoeken de neuroprotectieve rol van cannabinoïden bij de ziekte van Huntington.
Voor meer informatie: Cannabinoïde-receptorenZiekte van Huntington: CB1-receptoren
De betrokkenheid van het endocannabinoïdesysteem, in het bijzonder de CB1-receptoren, bij de ziekte van Huntington wordt al lang verondersteld. Het is inderdaad aangetoond dat een van de eerste duidelijke veranderingen bij individuen die door de ziekte worden getroffen, het selectieve verlies van CB1-receptoren in de basale kernen is. Dit receptorverlies gaat vooraf aan het begin van striatum-neuropathie. In transgene diermodellen voor de ziekte van Huntington is het Er werd een verandering waargenomen in zowel de CB1-receptorexpressie als de endocannabinoïdeniveaus. Deze bewijzen hebben geleid tot de hypothese dat een ontregeling van het endocannabinoïdesysteem een doelwit zou kunnen zijn voor de ontwikkeling van nieuwe therapeutische strategieën.
In zeer recente studies is aangetoond dat de deletie van CB1-receptoren in transgene modellen voor de ziekte van Huntington resulteerde in een verslechtering van het motorische fenotype, in een "striatumatrofie en een ophoping van het huntingtine-eiwit, terwijl een chronische behandeling met een cannabisagonist , tetrahydrocannibol (Δ9-THC), gunstig was.
Ten slotte worden CB1-receptoren sterk tot expressie gebracht in GABAerge neuronen, die 90-95% uitmaken van de neuronen in het striatum, het hersengebied dat wordt aangetast bij de ziekte van Huntington, zoals uitgelegd in de vorige paragrafen.
Stimulatie van CB1-receptoren leidt tot een afname van de afgifte van de remmende neurotransmitter GABA. Deze vermindering zou schadelijk kunnen zijn voor patiënten met de ziekte van Huntington, aangezien door het verminderen van de remmende tonus die wordt uitgeoefend door GABA, er een buitensporige toename zou zijn van de prikkelende tonus, bepaald door glutamaat, en bijgevolg van het fenomeen van excitotoxiciteit. Er wordt gedacht dat excitotoxiciteit bijdraagt aan de dood van projectie-neuronen in het striatum. CB1-receptoren bevinden zich echter ook in glutamaat-neuronen, zij het in mindere mate. Er werd verondersteld dat stimulatie van deze receptoren ook zou leiden tot een lagere afgifte van glutamaat het verminderen van excitotoxiciteit Het feit dat chronische behandeling met Δ9-THC gunstig was, suggereert dat de bijdrage van CB1-receptoren bij het mediëren van de respons op cannabinoïde-agonisten in specifieke neuronen kan veranderen in ziekteprogressie.
Toekomstperspectieven
Op dit moment wordt er gezocht naar een remedie voor de ziekte van Huntington en zijn er verschillende klinische onderzoeken gaande om de werkzaamheid te evalueren van verschillende farmacologische middelen en/of niet-farmacologische benaderingen (bijv. gentherapie, stamceltransplantatie) die de productie van huntingtine kunnen verminderen of de neuronale overleving verbeteren, de progressie van de ziekte voorkomen of vertragen.
Bijvoorbeeld genuitschakeling met behulp van RNA-interferentie (RNAi) of antisense-oligonucleotiden (ASO). De ASO's binden zich met name aan het "messenger-RNA dat informatie draagt" van het gemuteerde gen, blokkeren de translatie ervan en stimuleren de afbraak ervan zodat het huntingtine-eiwit niet wordt geproduceerd. Stamceltherapie daarentegen bestaat uit het vervangen van beschadigde neuronen, dankzij de transplantatie van stamcellen, in de aangetaste hersengebieden. Proeven in diermodellen en in voorlopige klinische proeven hebben tegenstrijdige resultaten opgeleverd met deze techniek, dus er is meer bewijs nodig om de effectiviteit ervan vast te stellen.
Bibliografie
- Caron, NS, Wright, G.E.B. & Hayden, MR. De ziekte van Huntington. GeneReviews ((R)) Ziekte van Huntington. Seattle (WA), 2018.
- Neurobiol Dis. 2012 maart;45:983-91. doi: 10.1016 / j.nbd.2011.12.017. Epub 23 december 2011. Onbalans van CB1-receptoren uitgedrukt in GABAerge en glutamaterge neuronen in een transgeen muismodel van de ziekte van Huntington. Chiodi V, Uchigashima M, Beggiato S, Ferrante A, Armida M, Martire A, Potenza RL, Ferraro L, Tanganelli S, Watanabe M, Domenici MR, Popoli P.