Eenmaal gebioactiveerd, leidt tetrachloorkoolstof (CCl4, een complex molecuul en op zichzelf niet erg toxisch) tot een reeks gebeurtenissen en de vorming van talrijke toxische verbindingen. Dit molecuul is ook bekend onder de naam FREON 10.
Freon 10 werd in het verleden gebruikt als component in de vloeistof van brandblussers, koelkasten, airconditioners, vlekverwijderaars en stomerij.
Freon 10 is erg gevaarlijk omdat het een elektron verliest wanneer het wordt gemetaboliseerd tot trichloormethyleen (CCl3); deze laatste metaboliet heeft een ongepaard elektron, dus het wordt een radicaal, dus een zeer reactieve verbinding.Trichloormethyleen heeft veel gevaarlijke effecten:
- het bindt gemakkelijk aan de -EME-groep van eiwitten;
- blokkeert de activiteit van cytochroom P450 (aangezien cytochroom een "hemoproteïne" is);
- werkt op andere cellulaire eiwitten;
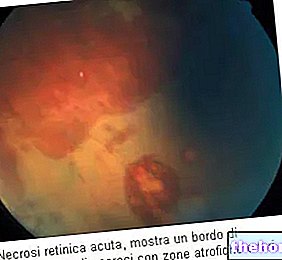
- kan levernecrose en kanker veroorzaken;
- het kan nefropathieën veroorzaken;
- interactie met de vetzuren van de membraanlipiden, leidt dit tot de vorming van chloroform, wat bij oxidatie leidt tot de vorming van fosgeen.
Vroeger werd chloroform gebruikt als verdovingsmiddel; het is eigenlijk een zeer giftige stof omdat het leidt tot de vorming van een zeer giftige tetrachloorkoolstofmetaboliet.

Ook uit Freon 10 verkrijgen we FOSGENE, een zeer giftige metaboliet. Met name van alle metabolieten die worden gevormd bij de metabolisatie van Freon 10, is fosgeen duidelijk het meest toxisch in vergelijking met de andere.
De fosgeenmetaboliet in ons lichaam wordt geremd met een "hydrolyse-actie die het splitst in zoutzuur (HCl) en koolstofdioxide (CO2). Als dit remmingssysteem echter onvoldoende is, bindt het fosgeen zich onomkeerbaar via covalente bindingen aan alle eiwitten.
Andere artikelen over "Koolstoftetrachloride of Freon 10"
- Dibroomethaan: gezondheidseffecten
- Toxiciteit en toxicologie
- Aromatische amines en voedsel koken