Actieve ingrediënten: Lercanidipine (lercanidipinehydrochloride)
LERCADIP 10 mg filmomhulde tabletten
LERCADIP 20 mg filmomhulde tabletten
Indicaties Waarom wordt Lercadip gebruikt? Waar is het voor?
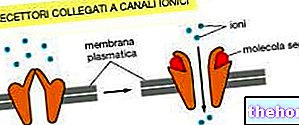
Lercadip, lercanidipinehydrochloride, behoort tot een groep geneesmiddelen die calciumkanaalblokkers (dihydropyridinederivaten) worden genoemd en die de bloeddruk verlagen.
Lercadip wordt gebruikt voor de behandeling van hoge bloeddruk, ook bekend als hypertensie, bij volwassenen ouder dan 18 jaar (niet aanbevolen bij kinderen jonger dan 18 jaar).
Contra-indicaties Wanneer Lercadip niet mag worden gebruikt
Neem Lercadip niet in
- Als u allergisch (overgevoelig) bent voor lercanidipinehydrochloride of voor één van de andere bestanddelen van Lercadip tabletten.
- Als u allergische reacties heeft gehad op geneesmiddelen die vergelijkbaar zijn met Lercadip-tabletten (bijvoorbeeld amlodipine, nicardipine, felodipine, isradipine, nifedipine of lacidipine).
- Als u aan bepaalde hartaandoeningen lijdt, zoals:
- ongecontroleerd hartfalen
- obstructie van de bloedstroom vanuit het hart
- onstabiele angina (angina in rust of progressief verergeren)
- hartaanval minder dan een maand oud.
- Als u ernstige lever- of nierproblemen heeft.
- Als u geneesmiddelen gebruikt die het CYP3A4-iso-enzym remmen, zoals:
- antischimmelmiddelen (bijv. ketoconazol of itraconazol)
- macrolide-antibiotica (bijv. erytromycine of troleandomycine)
- antivirale middelen (bijv. ritonavir).
- Als u een ander geneesmiddel gebruikt, ciclosporine genaamd (gebruikt na transplantaties om orgaanafstoting te voorkomen).
- Met grapefruit of grapefruitsap.
Gebruik Lercadip niet als u zwanger bent of borstvoeding geeft (zie de rubriek Zwangerschap, borstvoeding en vruchtbaarheid voor meer informatie).
Voorzorgen bij gebruik Wat u moet weten voordat u Lercadip inneemt
Neem contact op met uw arts of apotheker voordat u Lercadip inneemt:
- Als u andere hartaandoeningen heeft die niet zijn behandeld met het inbrengen van een pacemaker of als u reeds bestaande angina heeft.
- Als u lever- of nierproblemen heeft of dialyse ondergaat.
Vertel het uw arts als u denkt zwanger te zijn (of te worden) of borstvoeding geeft (zie rubriek Zwangerschap, borstvoeding en vruchtbaarheid).
Kinderen en adolescenten
De veiligheid en werkzaamheid van Lercadip bij kinderen tot 18 jaar zijn niet vastgesteld.Er zijn geen gegevens beschikbaar.
Interacties Welke medicijnen of voedingsmiddelen kunnen het effect van Lercadip . veranderen
Vertel het uw arts of apotheker als u andere geneesmiddelen gebruikt, kort geleden heeft gebruikt of in de nabije toekomst gaat gebruiken.
Vertel het uw arts of apotheker:
- Als u bètablokkers gebruikt zoals metoprolol, diuretica of ACE-remmers (geneesmiddelen om hoge bloeddruk te behandelen).
- Als u cimetidine gebruikt (meer dan 800 mg, een geneesmiddel tegen maagzweren, indigestie of brandend maagzuur).
- Als u digoxine gebruikt (een geneesmiddel om hartproblemen te behandelen).
- Als u midazolam gebruikt (een geneesmiddel dat u helpt te slapen).
- Als u rifampicine gebruikt (een geneesmiddel om tuberculose te behandelen).
- Als u astemizol of terfenadine gebruikt (geneesmiddelen om allergieën te behandelen).
- Als u amiodaron of kinidine gebruikt (geneesmiddelen om een snelle hartslag te behandelen).
- Als u fenytoïne of carbamazepine (geneesmiddelen tegen epilepsie) gebruikt Uw arts zal uw bloeddruk vaker dan normaal willen controleren.
Waarop moet u letten met eten, drinken en alcohol
- Drink geen alcohol terwijl u Lercadip-tabletten gebruikt, omdat dit het effect van het geneesmiddel kan versterken.
- Neem Lercadip-tabletten niet in met grapefruit of grapefruitsap.
Waarschuwingen Het is belangrijk om te weten dat:
Zwangerschap, borstvoeding en vruchtbaarheid
Lercadip mag niet worden gebruikt als u zwanger bent, denkt zwanger te zijn of van plan bent zwanger te worden, of als u borstvoeding geeft of geen voorbehoedsmiddelen gebruikt.
Vraag uw arts of apotheker om advies voordat u dit geneesmiddel inneemt.
Rijvaardigheid en het gebruik van machines
Voorzichtigheid is geboden aangezien duizeligheid, zwakte, vermoeidheid en zelden slaperigheid kunnen optreden. Rijd niet en bedien geen machines totdat u weet welke invloed Lercadip op u heeft.
Lercadip bevat lactose
Als uw arts u heeft verteld dat u bepaalde suikers niet verdraagt, neem dan contact op met uw arts voordat u dit geneesmiddel inneemt.
Dosis, wijze en tijdstip van toediening Hoe Lercadip te gebruiken: Dosering
Gebruik dit geneesmiddel altijd precies zoals uw arts u dat heeft verteld. Raadpleeg bij twijfel uw arts of apotheker.
Volwassenen: De aanbevolen dosis is 10 mg eenmaal per dag, elke dag op hetzelfde tijdstip ingenomen, bij voorkeur 's morgens ten minste 15 minuten voor het ontbijt, aangezien een vetrijke maaltijd de bloedspiegels van het geneesmiddel aanzienlijk verhoogt. Indien nodig kan uw arts u adviseren de dosis te verhogen door over te schakelen op Lercadip 20 mg eenmaal per dag. De tabletten moeten bij voorkeur heel worden doorgeslikt met wat water.
Gebruik bij kinderen: Dit geneesmiddel mag niet worden gebruikt bij kinderen jonger dan 18 jaar.
Oudere patiënten: Er is geen dagelijkse dosisaanpassing nodig. Er moet echter bijzondere aandacht worden besteed aan het starten van de behandeling.
Patiënten met lever- of nierproblemen: Bij het starten van de behandeling bij deze patiënten is bijzondere aandacht nodig en een verhoging van de dagelijkse dosis tot 20 mg dient zorgvuldig te worden overwogen.
Wat u moet doen wanneer u bent vergeten Lercadip in te nemen
Als u vergeten bent een tablet in te nemen, sla dan gewoon de gemiste dosis over en ga de volgende dag verder met het innemen zoals voorgeschreven.
Neem geen dubbele dosis om een vergeten dosis in te halen.
Als u stopt met het innemen van Lercadip
Als u stopt met het innemen van Lercadip, kan uw bloeddruk weer stijgen Raadpleeg uw arts voordat u stopt met de behandeling.
Als u nog vragen heeft over het gebruik van dit geneesmiddel, neem dan contact op met uw arts of apotheker.
Overdosering Wat moet u doen als u te veel Lercadip heeft ingenomen?
Overschrijd de dosis die aan u is voorgeschreven niet.
Als u een hogere dosis inneemt dan voorgeschreven of als u een overdosis heeft, raadpleeg dan onmiddellijk uw arts en neem indien mogelijk uw tabletten en/of de verpakking mee.
Inname van meer dan de aanbevolen dosis kan een overmatige verlaging van de bloeddruk en het optreden van onregelmatige hartritmes of tachycardie veroorzaken. Dit kan ook leiden tot bewusteloosheid.
Bijwerkingen Wat zijn de bijwerkingen van Lercadip
Zoals alle geneesmiddelen kan ook dit geneesmiddel bijwerkingen hebben, al krijgt niet iedereen daarmee te maken.
Sommige bijwerkingen kunnen ernstig zijn:
Als u een van de volgende bijwerkingen ervaart, raadpleeg dan onmiddellijk uw arts.
Zelden (komen voor bij minder dan 1 op de 1.000 gebruikers):
angina pectoris (pijn op de borst veroorzaakt door onvoldoende bloedtoevoer naar het hart).
Zeer zelden (komen voor bij minder dan 1 op de 10.000 gebruikers):
pijn op de borst, lage bloeddruk, flauwvallen en allergische reacties (symptomen zijn jeuk, huiduitslag, netelroos).
Als u reeds bestaande angina pectoris heeft, kan een toename van de frequentie, duur en ernst van angina-aanvallen optreden bij de groep geneesmiddelen waartoe Lercadip behoort. Er kunnen geïsoleerde gevallen van een myocardinfarct worden waargenomen.
Andere mogelijke bijwerkingen:
Soms (komen voor bij minder dan 1 op de 100 gebruikers):
hoofdpijn, duizeligheid, snelle hartslag, hartkloppingen (wanorde of versnelde hartslag), plotselinge roodheid van het gezicht, de nek en de bovenborst, gezwollen enkels.
Zelden (komen voor bij minder dan 1 op de 1.000 gebruikers):
slaperigheid, misselijkheid, braken, brandend maagzuur, maagpijn, diarree, roodheid van de huid, pijn in het lichaam, verhoogde hoeveelheid urine, vermoeidheid.
Zeer zelden (komen voor bij minder dan 1 op de 10.000 gebruikers):
zwelling van het tandvlees, abnormale leverfunctiewaarden (opgespoord door bloedonderzoek), frequente aandrang om te urineren.
Melding van bijwerkingen
Krijgt u last van bijwerkingen, neem dan contact op met uw arts of apotheker.Dit geldt ook voor mogelijke bijwerkingen die niet in deze bijsluiter staan. U kunt bijwerkingen ook rechtstreeks melden via het nationale meldsysteem op www.agenziafarmaco.gov.it/it/responsabili Door bijwerkingen te melden, kunt u ons helpen meer informatie te verkrijgen over de veiligheid van dit geneesmiddel.
Vervaldatum en retentie
Buiten het zicht en bereik van kinderen houden.
Gebruik dit geneesmiddel niet meer na de uiterste houdbaarheidsdatum. Die is te vinden op de doos en de blister na Vervaldatum. De vervaldatum verwijst naar de laatste dag van die maand.
Bewaren in de oorspronkelijke verpakking om het geneesmiddel tegen licht te beschermen.
Gooi geneesmiddelen niet weg via het afvalwater of met huishoudelijk afval. Vraag uw apotheker wat u met geneesmiddelen moet doen die u niet meer gebruikt. Dit helpt het milieu te beschermen.
Deadline "> Overige informatie
Wat bevat Lercadip
Het werkzame bestanddeel is lercanidipinehydrochloride.
Elke filmomhulde tablet bevat 10 mg lercanidipinehydrochloride (overeenkomend met 9,4 mg lercanidipine) of 20 mg lercanidipinehydrochloride (overeenkomend met 18,8 mg lercanidipine).
De andere ingrediënten zijn:
- Tabletkern: lactosemonohydraat, microkristallijne cellulose, natriumcarboxymethylzetmeel, povidon K30, magnesiumstearaat.
- Filmomhulling: hypromellose, talk, titaniumdioxide (E171), macrogol 6000, ijzeroxide (E172).
Hoe ziet Lercadip er uit en wat is de inhoud van de verpakking
Lercadip 10 mg: gele, ronde, biconvexe, filmomhulde tablet met een breukstreep aan één zijde. De breukstreep op de tablet is bedoeld om het breken van de tablet gemakkelijker te maken, zodat de tablet gemakkelijker kan worden doorgeslikt en niet om deze in gelijke doses te verdelen.
Lercadip 20 mg: roze, ronde, biconvexe, filmomhulde tablet met een breukstreep aan één kant. De tablet kan in twee gelijke doses worden verdeeld.
Lercadip is verkrijgbaar in blisterverpakkingen, in verpakkingen van 7, 14, 28, 35, 42, 50, 56, 98 en 100 tabletten.
Mogelijk worden niet alle verpakkingsgrootten in de handel gebracht.
Bron Bijsluiter: AIFA (Italiaans Geneesmiddelenbureau). Inhoud gepubliceerd in januari 2016. De aanwezige informatie is mogelijk niet up-to-date.
Om toegang te hebben tot de meest actuele versie, is het raadzaam om de website van AIFA (Italian Medicines Agency) te bezoeken. Disclaimer en nuttige informatie.
01.0 NAAM VAN HET GENEESMIDDEL -
LERCADIP 10 MG TABLETTEN
02.0 KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING -
Eén tablet bevat 10 mg lercanidipinehydrochloride, wat overeenkomt met 9,4 mg lercanidipine.
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1
03.0 FARMACEUTISCHE VORM -
Filmomhulde tablet.
Gele, ronde, biconvexe tablet, aan één kant in tweeën gedeeld.
04.0 KLINISCHE INFORMATIE -
04.1 Therapeutische indicaties -
LERCADIP is geïndiceerd voor de behandeling van lichte tot matige essentiële hypertensie.
04.2 Dosering en wijze van toediening -
De aanbevolen dosering is 10 mg eenmaal daags oraal, ten minste 15 minuten voor de maaltijd; de dosis kan worden verhoogd tot 20 mg, afhankelijk van de individuele respons van de patiënt.
De dosisaanpassing dient geleidelijk te gebeuren aangezien het maximale antihypertensieve effect binnen ongeveer 2 weken optreedt.
In het geval van patiënten die niet voldoende onder controle zijn met antihypertensieve monotherapie, is het mogelijk om de toediening van LERCADIP te combineren met bètablokkers (atenolol), diuretica (hydrochloorthiazide) of ACE-remmers (captopril of enalapril).
Aangezien de dosis-responscurve steil is en een "plateau" heeft bij doses tussen 20 en 30 mg, is het onwaarschijnlijk dat hogere doses een grotere werkzaamheid zullen induceren, terwijl omgekeerd een toename van bijwerkingen kan optreden.
Gebruik bij ouderen : Hoewel farmacokinetische studies en specifieke klinische ervaring niet hebben uitgewezen dat de dagelijkse dosis moet worden aangepast, wordt toch bijzondere aandacht aanbevolen bij het starten van de behandeling bij ouderen.
Gebruik bij kinderen : aangezien er geen klinische onderzoeken zijn uitgevoerd bij patiënten jonger dan 18 jaar, wordt toediening op pediatrische leeftijd niet aanbevolen.
Gebruik bij patiënten met lever- of nierdisfunctie : Bijzondere voorzichtigheid is geboden bij het starten van de behandeling van patiënten met een lichte tot matige lever- of nierfunctiestoornis. De aanbevolen dosering werd door deze patiënten goed verdragen, maar verhoging van de dagelijkse dosis tot 20 mg moet zorgvuldig worden overwogen. Bij patiënten met leverinsufficiëntie kan het antihypertensieve effect worden versterkt en daarom moet een dosisaanpassing worden overwogen.
Behandeling met LERCADIP wordt niet aanbevolen bij patiënten met een ernstige leverfunctiestoornis of bij patiënten met een ernstige nierfunctiestoornis (glomerulaire filtratiesnelheid
04.3 Contra-indicaties -
Overgevoeligheid voor de werkzame stof "lercanidipine", voor dihydropyridines in het algemeen of voor één van de in het geneesmiddel aanwezige hulpstoffen.
Zwangerschap en borstvoeding (zie rubriek 4.6).
Vrouwen in de vruchtbare leeftijd die geen effectieve anticonceptiedekking gebruiken.
Obstructie van de linkerventrikelejectie.
Onbehandeld congestief hartfalen.
Instabiele angina pectoris.
Ernstige veranderingen in de lever- of nierfunctie.
Patiënten die minder dan een maand een hartaanval hebben gehad.
Gelijktijdige behandeling met:
krachtige CYP3A4-remmers (zie rubriek 4.5);
ciclosporine (zie rubriek 4.5);
grapefruitsap (zie rubriek 4.5).
04.4 Bijzondere waarschuwingen en passende voorzorgen bij gebruik -
Bijzondere voorzichtigheid is geboden bij toediening van LERCADIP aan patiënten met sinusknoopdisfunctiesyndromen (als er geen pacemaker is geïmplanteerd). Hoewel gecontroleerde hemodynamische onderzoeken geen verslechtering van de ventriculaire functie hebben aangetoond, is voorzichtigheid geboden bij patiënten met linkerventrikeldisfunctie. Er is gesuggereerd dat sommige kortwerkende dihydropyridines het risico op cardiovasculaire morbiditeit bij patiënten met cardiale ischemie kunnen verhogen.Hoewel LERCADIP een langwerkend geneesmiddel is bij dergelijke patiënten, is voorzichtigheid geboden.
Sommige dihydropyridines kunnen in zeldzame gevallen precordiale pijn of angina pectoris veroorzaken. In zeer zeldzame gevallen kan er een toename zijn in de frequentie, duur en ernst van acute angina-episodes bij patiënten met reeds bestaande angina pectoris. Er kunnen geïsoleerde gevallen van een myocardinfarct worden waargenomen (zie rubriek 4.8).
Gebruik bij patiënten met lever- of nierdisfunctie : Bijzondere voorzichtigheid is geboden bij het starten van de behandeling van patiënten met een lichte tot matige lever- of nierfunctiestoornis. De aanbevolen dosering werd door deze patiënten goed verdragen, maar verhoging van de dagelijkse dosis tot 20 mg moet zorgvuldig worden overwogen. Bij patiënten met leverinsufficiëntie kan het antihypertensieve effect worden versterkt en daarom moet een dosisaanpassing worden overwogen.
Behandeling met LERCADIP wordt niet aanbevolen bij patiënten met een ernstige leverfunctiestoornis of bij patiënten met een ernstige nierfunctiestoornis (glomerulaire filtratiesnelheid
Alcoholgebruik dient vermeden te worden aangezien dit het vaatverwijdende effect van antihypertensiva kan versterken (zie rubriek 4.5).
CYP3A4-inductoren zoals anticonvulsiva (bijv. fenytoïne, carbamazepine) en rifampicine kunnen de plasmaspiegels van lercanidipine verlagen en daarom kan de werkzaamheid van lercanidipine minder zijn dan verwacht (zie rubriek 4.5).
1 tablet bevat 30 mg lactose en mag daarom niet worden toegediend aan patiënten met Lapp-lactasedeficiëntie, galactosemie of glucose/galactose malabsorptiesyndroom.
04.5 Interacties met andere geneesmiddelen en andere vormen van interactie -
Aangezien lercanidipine wordt gemetaboliseerd door het CYP3A4-enzym, kunnen gelijktijdig toegediende remmers en inductoren van CYP3A4 een interactie aangaan met het metabolisme en de eliminatie van lercanidipine.
Gelijktijdige toediening van LERCADIP met CYP3A4-remmers (bijv. ketoconazol, itraconazol, ritonavir, erytromycine, troleandomycine) moet worden vermeden (zie rubriek 4.3).
Een interactiestudie met ketoconazol, een krachtige CYP3A4-remmer, toonde een aanzienlijke toename van de plasmaconcentraties van lercanidipine aan (een 15-voudige toename van de AUC en een 8-voudige toename van de Cmax voor het eutomeer S-lercanidipine).
Ciclosporine en lercanidipine mogen niet samen worden toegediend (zie rubriek 4.3).
Na gelijktijdige toediening van lercanidipine en ciclosporine werd een verhoging van de plasmaspiegels van beide werkzame stoffen waargenomen. Een onderzoek bij jonge gezonde vrijwilligers heeft aangetoond dat wanneer ciclosporine 3 uur na inname van lercanidipine wordt toegediend, de plasmaspiegels van lercanidipine niet veranderen, terwijl de AUC van ciclosporine met 27% stijgt. Gelijktijdige toediening van LERCADIP met ciclosporine veroorzaakte echter een drievoudige verhoging van de plasmaspiegels van lercanidipine en een verhoging van 21% van de AUC van ciclosporine.
Lercanidipine mag niet worden ingenomen met grapefruitsap (zie rubriek 4.3).
Zoals met andere dihydropyridines, is lercanidipine gevoelig voor de metabole remming veroorzaakt door grapefruitsap, wat resulteert in een toename van de systemische beschikbaarheid en een toename van het hypotensieve effect.
Wanneer een dosis van 20 mg gelijktijdig met midazolam oraal wordt toegediend aan oudere proefpersonen, wordt de absorptie van lercanidipine verhoogd (met ongeveer 40%) en neemt de absorptiesnelheid af (tmax wordt vertraagd met 1,75 tot 3 uur). .
Voorzichtigheid is geboden wanneer LERCADIP samen met andere CYP3A4-substraten wordt voorgeschreven, zoals: terfenadine, astemizol, klasse III-antiaritmica zoals amiodaron en kinidine.
Gelijktijdige toediening van LERCADIP met inductoren van CYP3A4 zoals anti-epileptica (bijv. fenytoïne, carbamazepine) en rifampicine moet met voorzichtigheid gebeuren, aangezien het antihypertensieve effect kan worden verminderd en de bloeddruk vaker dan normaal moet worden gecontroleerd.
Wanneer LERCADIP wordt toegediend met metoprolol, een bètablokker die voornamelijk door de lever wordt geëlimineerd, verandert de biologische beschikbaarheid van metoprolol niet, terwijl die van lercanidipine met 50% wordt verminderd. Dit effect kan te wijten zijn aan de vermindering van de hepatische bloedstroom veroorzaakt door bètablokkers en kan daarom optreden bij andere geneesmiddelen van deze klasse. Bijgevolg kan lercanidipine worden toegediend met bèta-adrenerge receptorblokkers, maar het kan zijn dat de dosis moet worden aangepast.
Een interactiestudie met fluoxetine (een remmer van CYP2D6 en CYP3A4), uitgevoerd bij vrijwilligers van 65 ± 7 jaar (gemiddelde ± s.d.), toonde geen klinisch relevante veranderingen in de farmacokinetiek van lercanidipine.
De plasmaspiegels van lercanidipine zijn niet significant veranderd bij patiënten die gelijktijdig cimetidine 800 mg/dag krijgen, maar voorzichtigheid is geboden bij hogere doses aangezien de biologische beschikbaarheid en het hypotensieve effect van lercanidipine kunnen toenemen.
Bij patiënten die een chronische behandeling met b-methyldigoxine ondergingen, resulteerde gelijktijdige toediening van 20 mg lercanidipine niet in enige farmacokinetische interactie. Gezonde vrijwilligers die met digoxine werden behandeld, vertoonden na een dosis van 20 mg lercanidipine, toegediend in nuchtere toestand, een gemiddelde toename van 33% van de Cmax van digoxine, terwijl de AUC en de renale klaring niet significant veranderden. Patiënten dienen zorgvuldig te worden gecontroleerd. Gelijktijdige behandeling met digoxine om tekenen van digoxinetoxiciteit op te sporen.
Na herhaalde gelijktijdige toediening van een dosis van 20 mg LERCADIP met 40 mg simvastatine, was de AUC van lercanidipine niet significant veranderd, terwijl de AUC van simvastatine met 56% toenam en die van zijn actieve metaboliet - 28% hydroxyzuur. Het is onwaarschijnlijk dat deze veranderingen klinisch relevant zijn. Er wordt geen interactie verwacht wanneer lercanidipine 's ochtends wordt toegediend en simvastatine 's avonds, zoals aangegeven voor deze geneesmiddelen.
Gelijktijdige toediening van 20 mg lercanidipine door nuchtere gezonde vrijwilligers verandert de farmacokinetiek van warfarine niet.
LERCADIP toegediend met diuretica en ACE-remmers werd goed verdragen.
Alcoholgebruik dient vermeden te worden aangezien dit het vaatverwijdende effect van antihypertensiva kan versterken (zie rubriek 4.4).
04.6 Zwangerschap en borstvoeding -
De resultaten van onderzoeken bij ratten en konijnen lieten geen teratogeen effect van lercanidipine bij deze diersoorten zien, en er was geen verslechtering van de voortplantingsfunctie bij ratten. Vanwege het gebrek aan klinische gegevens over het gebruik van lercanidipine tijdens zwangerschap en borstvoeding, en het is echter aangetoond dat andere verbindingen die tot de dihydropyridine-klasse behoren teratogeen zijn bij dieren, mag LERCADIP niet worden toegediend tijdens de zwangerschap of aan vrouwen in de vruchtbare leeftijd die gebruik geen effectieve anticonceptiedekking. Vanwege de hoge lipofiliciteit van lercanidipine kan excretie in de moedermelk optreden, daarom mag het niet worden toegediend tijdens het geven van borstvoeding.
04.7 Beïnvloeding van de rijvaardigheid en het vermogen om machines te bedienen -
Klinische ervaring met lercanidipine heeft aangetoond dat het gebruik van het geneesmiddel geen invloed heeft op de rijvaardigheid of het vermogen om machines te bedienen. Voorzichtigheid is echter geboden aangezien duizeligheid, asthenie, een gevoel van vermoeidheid en, zeldzamer, slaperigheid kunnen optreden.
04.8 Bijwerkingen -
Bijwerkingen traden op bij ongeveer 1,8% van de behandelde patiënten.
De onderstaande tabel toont de incidentie van bijwerkingen, met op zijn minst mogelijke oorzaken, gegroepeerd per MedDRA-systeem/orgaanklasse en gesorteerd op frequentie (soms, zelden).
Zoals weergegeven in de tabel, zijn de vaakst waargenomen bijwerkingen die zijn gemeld in gecontroleerde klinische onderzoeken hoofdpijn, duizeligheid, perifeer oedeem, tachycardie, hartkloppingen, blozen, elk optredend bij minder dan 1% van de patiënten.
Tijdens de postmarketingervaring zijn uit de spontane meldingen die zijn ontvangen, de volgende bijwerkingen zeer zelden gemeld (gingivale hypertrofie, reversibele verhoging van de serumspiegels van levertransaminasen, hypotensie, urinaire frequentie en pijn op de borst.
Sommige dihydropyridines kunnen in zeldzame gevallen precordiale pijn of angina pectoris veroorzaken. In zeer zeldzame gevallen kan er een toename zijn in de frequentie, duur en ernst van acute angina-episodes bij patiënten met reeds bestaande angina pectoris. Er kunnen geïsoleerde gevallen van een myocardinfarct worden waargenomen.
Er zijn geen negatieve effecten van lercanidipine op de bloedglucose of lipemie.
04.9 Overdosering -
Tijdens postmarketingervaring zijn drie gevallen van overdosering gemeld (respectievelijk 150 mg, 280 mg en 800 mg lercanidipine werden ingenomen in een poging tot zelfmoord).
Zoals met andere dihydropyridines, wordt aangenomen dat een overdosis kan leiden tot overmatige perifere vasodilatatie, vergezeld van duidelijke hypotensie en reflextachycardie. In geval van ernstige hypotensie, bradycardie en bewustzijnsverlies kan cardiovasculaire ondersteunende therapie nodig zijn, met intraveneuze toediening van atropine in geval van bradycardie.
Gezien het langdurige farmacologische effect van lercanidipine, is het essentieel om de cardiovasculaire functie van de patiënt die een overmatige dosis van het geneesmiddel heeft ingenomen gedurende ten minste 24 uur te controleren.Er is geen informatie beschikbaar over de mogelijke gunstige effecten van dialyse.Gezien de hoge lipofiliciteit van het geneesmiddel, is het zeer waarschijnlijk dat plasmaspiegels niet kunnen worden gebruikt als maatstaf voor de duur van de risicoperiode en dat dialyse geen werkzaamheid heeft.
05.0 FARMACOLOGISCHE EIGENSCHAPPEN -
05.1 "Farmacodynamische eigenschappen -
Farmacotherapeutische categorie: selectieve calciumkanaalblokkers met overwegend vasculair effect.
ATC-code: C08CA13
Lercanidipine is een calciumantagonist die behoort tot de dihydropyridinegroep en die de calciumstroom door het celmembraan van gladde spieren en het hart remt. Het mechanisme van zijn antihypertensieve werking is te wijten aan een direct ontspannend effect op vasculaire gladde spieren, met als gevolg een verlaging van de totale perifere weerstand. Ondanks zijn korte plasmahalfwaardetijd heeft lercanidipine een langdurige antihypertensieve activiteit, dankzij de hoge verdelingscoëfficiënt in het membraan, en veroorzaakt het geen negatieve inotrope effecten dankzij zijn hoge vasculaire selectiviteit.
Aangezien de door LERCADIP geïnduceerde vasodilatatie wordt gekenmerkt door een geleidelijk begin van het effect, is acute hypotensie met reflextachycardie slechts zelden opgetreden bij hypertensieve patiënten.
Net als bij andere asymmetrische 1,4-dihydropyridines is de antihypertensieve activiteit van lercanidipine voornamelijk te danken aan zijn (S)-enantiomeer.
Naast klinische onderzoeken die zijn uitgevoerd ter ondersteuning van de therapeutische indicatie, bleek uit een ander gerandomiseerd onderzoek bij patiënten met ernstige hypertensie (gemiddelde diastolische bloeddruk ± sd van 114,5 ± 3,7 mmHg) dat de bloeddruk normaliseerde bij 40% van de 25 patiënten die werden behandeld met een dosering van 20 mg, in een enkele dagelijkse toediening van LERCADIP, en bij 56% van de 25 patiënten die werden behandeld met een dosering van 10 mg tweemaal daags. In een gerandomiseerde, dubbelblinde, placebogecontroleerde klinische studie bij patiënten met geïsoleerde systolische hypertensie, bleek LERCADIP effectief te zijn bij het verlagen van de systolische bloeddruk van een initiële gemiddelde waarde van 172,6 ± 5,6 mmHg tot 140,2 ± 8,7 mmHg.
05.2 "Farmacokinetische eigenschappen -
LERCADIP wordt volledig geabsorbeerd na orale toediening van 10-20 mg en plasmapieken van respectievelijk 3,30 ng/ml ± 2,09 s.d. en 7,66 ng/ml ± 5,90 d.s., worden ongeveer 1,5-3 uur na toediening bereikt.
De twee enantiomeren van lercanidipine vertonen een vergelijkbaar plasmaspiegelprofiel: de tijd om de maximale plasmaconcentratie te verkrijgen is identiek, de maximale plasmaconcentratie en AUC zijn gemiddeld 1,2 keer hoger voor de (S)-enantiomeer en de eliminatiehalfwaardetijd van de twee enantiomeren is in wezen hetzelfde.Er werd geen "in vivo" onderlinge omzetting van de enantiomeren waargenomen.
Na een hoog presystemisch metabolisme is de absolute biologische beschikbaarheid van LERCADIP bij orale toediening aan patiënten met voedsel ongeveer 10% en neemt af tot een derde (1/3) wanneer het wordt toegediend aan gezonde vrijwilligers in nuchtere toestand.
De beschikbaarheid van lercanidipine, oraal toegediend, verviervoudigt wanneer LERCADIP tot 2 uur na een vetrijke maaltijd wordt ingenomen. Daarom moet LERCADIP vóór de maaltijd worden toegediend.
Distributie van plasma naar weefsels en organen is snel en uitgebreid.
De plasma-eiwitbinding van lercanidipine is hoger dan 98%. Bij patiënten met ernstige nier- of leverdisfunctie zijn de plasma-eiwitspiegels verlaagd en kan de vrije fractie van het geneesmiddel toenemen.
LERCADIP wordt uitgebreid gemetaboliseerd door CYP3A4; het medicijn werd niet gedetecteerd in de urine of ontlasting. Het wordt voornamelijk omgezet in inactieve metabolieten en ongeveer 50% van de dosis wordt uitgescheiden in de urine.
"In vitro"-experimenten met humane levermicrosomen hebben aangetoond dat lercanidipine enige mate van remming van CYP3A4 en CYP2D6 uitoefent, maar bij concentraties die respectievelijk 160 en 40 keer hoger zijn dan die welke worden bereikt op de piek in plasma na toediening van een dosis van 20 mg.
Bovendien hebben interactiestudies bij mensen aangetoond dat lercanidipine de plasmaspiegels van midazolam, een typisch substraat van CYP3A4, of van metoprolol, een typisch substraat van CYP2D6, niet wijzigt.Daarom wordt bij therapeutische doses niet verwacht dat LERCADIP de biotransformatie van geneesmiddelen die worden gemetaboliseerd door CYP3A4 en CYP2D6.
Eliminatie vindt hoofdzakelijk plaats door biotransformatie.
De gemiddelde plasmahalfwaardetijd die kan worden berekend vanaf de terminale eliminatiefase is 8-10 uur en de therapeutische activiteit duurt 24 uur dankzij de hoge binding aan de lipidemembranen.Er werd geen accumulatie gevonden na herhaalde toediening.
Orale toediening van LERCADIP leidt tot plasmaspiegels van lercanidipine die niet recht evenredig zijn met de dosering (niet-lineaire kinetiek).Na inname van 10, 20 of 40 mg waren de waargenomen maximale plasmaconcentraties in een verhouding van 1: 3: 8 en de AUC's van de plasmaconcentratie in de loop van de tijd in een verhouding van 1: 4: 18, wat wijst op een progressieve verzadiging van de presystemische metabolisme Bijgevolg neemt de beschikbaarheid toe met toenemende dosering.
Bij oudere patiënten en bij patiënten met lichte tot matige nierfunctiestoornis of lichte tot matige leverfunctiestoornis was het farmacokinetische gedrag van lercanidipine vergelijkbaar met dat waargenomen bij de algemene patiëntenpopulatie; hogere concentraties (van ongeveer 70%) van het geneesmiddel werden gevonden bij patiënten met ernstige nierfunctiestoornissen of bij dialysepatiënten. Bij patiënten met een matige tot ernstige leverfunctiestoornis is een toename van de systemische biologische beschikbaarheid van lercanidipine waarschijnlijk, aangezien het geneesmiddel normaal gesproken uitgebreid wordt gemetaboliseerd in de lever.
05.3 Gegevens uit het preklinisch veiligheidsonderzoek -
Farmacotoxicologische studies bij dieren hebben geen effect aangetoond op het autonome zenuwstelsel, het centrale zenuwstelsel of de gastro-intestinale functie bij de doses die gewoonlijk worden gebruikt om het antihypertensieve effect te verkrijgen.
De relevante effecten die zijn waargenomen in langetermijnonderzoeken bij ratten en honden moeten worden beschouwd als direct of indirect gerelateerd aan de reeds bekende effecten na het gebruik van hoge doses calciumkanaalblokkers en weerspiegelen voornamelijk een overmatige farmacodynamische activiteit.
Lercanidipine is niet genotoxisch en er is aangetoond dat het geen carcinogeen potentieel heeft.
Vruchtbaarheid en voortplantingsfunctie bij ratten werden niet beïnvloed door behandeling met lercanidipine.
Er werden geen teratogene effecten gevonden bij ratten en konijnen; lercanidipine, gegeven in hoge doses bij ratten, veroorzaakte echter pre- en post-implantatieverliezen en vertraagde de ontwikkeling van de foetus.
Bij toediening in hoge doses (12 mg/kg/dag hydrochloride) tijdens de bevalling veroorzaakte lercanidipine dystokie.
De distributie van lercanidipine en/of zijn metabolieten bij drachtige dieren en hun uitscheiding in de moedermelk zijn niet geëvalueerd.
De metabolieten zijn niet afzonderlijk beoordeeld in toxiciteitsonderzoeken.
06.0 FARMACEUTISCHE INFORMATIE -
06.1 Hulpstoffen -
Lijst van hulpstoffen
Kern van de tablet:
Lactosemonohydraat
Microkristallijne cellulose
Natriumcarboxymethylzetmeel
Povidon K30
Magnesium stearaat.
Coatingfilm:
Hypromellose
Talk
Titaandioxide (E171)
Macrogol 6000
IJzeroxide (E172).
06.2 Incompatibiliteit "-
Niet relevant.
06.3 Geldigheidsduur "-
3 jaar.
06.4 Speciale voorzorgsmaatregelen bij bewaren -
Bewaar in de originele verpakking.
06.5 Aard van de primaire verpakking en inhoud van de verpakking -
Ondoorzichtige PVC en aluminium blisters.
Verpakkingen van 7, 14, 28, 35, 50, 56, 98 en 100 tabletten *.
* Mogelijk worden niet alle verpakkingsgrootten in de handel gebracht
06.6 Instructies voor gebruik en verwerking -
Geen speciale instructies.
07.0 HOUDER VAN DE "VERGUNNING VOOR HET IN DE HANDEL BRENGEN" -
INNOVA PHARMA S.p.A. - Via Matteo Civitali, 1 - 20148 Milaan, ITALI.
08.0 NUMMER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN -
LERCADIP 14 filmomhulde tabletten van 10 mg A.I.C. N. 033225018 / M
LERCADIP 28 filmomhulde tabletten van 10 mg A.I.C. N. 033225020 / M
LERCADIP 35 filmomhulde tabletten van 10 mg A.I.C. N. 033225032 / M
LERCADIP 50 10 mg filmomhulde tabletten A.I.C. N. 033225044 / M
LERCADIP 100 filmomhulde tabletten 10 mg A.I.C. N. 033225057 / M
09.0 DATUM VAN EERSTE VERGUNNING OF VERLENGING VAN DE VERGUNNING -
Datum van eerste vergunning: 22 maart 1996 (VK). 18 maart 1997 (IT). Datum eerste marketing: februari 1998 in de SSN.
Verlenging van de vergunning: 05 juli 2006
10.0 DATUM VAN HERZIENING VAN DE TEKST -
mei 2008