Algemeenheid
Osmolariteit drukt de concentratie van een oplossing uit en onderstreept het aantal opgeloste deeltjes, ongeacht de elektrische lading en grootte.

Een liter oplossing die één mol glucose bevat, zal dus dezelfde osmolariteit hebben als een liter oplossing die één mol natrium bevat (omdat een mol per definitie een vast aantal deeltjes - atomen, ionen of moleculen - bevat, gelijk aan 6 , 02x1023). De osmolariteit van de twee zal echter verschillen van één liter van een derde oplossing, die één mol keukenzout bevat; de laatste (waarvan de molecuulformule NaCl is), dissocieert in een waterige omgeving in feite in Na + en Cl-, dus resulterend in een oplossing die twee keer zoveel deeltjes bevat.
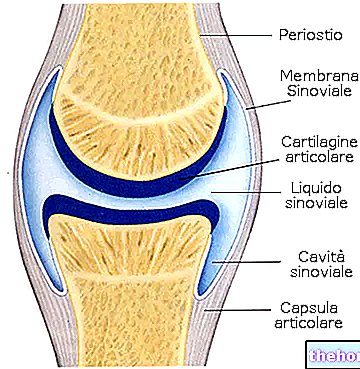
Onder normale omstandigheden is de osmolariteit identiek voor alle vloeistoffen die aanwezig zijn in de verschillende compartimenten van het organisme en is de waarde ongeveer 300 mOsM (alle gradiënten worden opgeheven door waterbewegingen). Deze compartimenten kunnen worden onderverdeeld in intra- en extracellulair, die respectievelijk een hoeveelheid water bevatten die gelijk is aan 40% en 20% van het lichaamsgewicht; het extracellulaire compartiment is verder onderverdeeld in twee compartimenten: het plasma-compartiment (1/3) en het interstitiële compartiment (2/3).
Het is erg belangrijk dat de osmolariteit van de verschillende compartimenten gelijk is; in feite, als de concentratie van opgeloste stoffen in de extracellulaire vloeistof toeneemt, verlaat het water de cel door osmose (en rimpels), terwijl in de tegenovergestelde situatie de cel water aanzuigt totdat het barst.
Opmerking: hoewel het het aantal osmol per kg (osmolaliteit) en niet dat per liter (osmolariteit) is dat de "eenheid van osmose" bepaalt, zijn voor zeer verdunde oplossingen - zoals lichaamsoplossingen - de kwantitatieve verschillen tussen osmolariteit en osmolaliteit hieronder van 1% (omdat slechts een klein deel van hun gewicht afkomstig is van de opgeloste stof) Om deze reden worden de twee termen vaak door elkaar gebruikt als synoniemen.
De belangrijkste regulator van plasma-osmolariteit is de nier, die min of meer verdunde urine produceert volgens de homeostatische behoeften van het organisme.
In het extracellulaire watercompartiment is natrium de belangrijkste osmol, terwijl in het intracellulaire kalium de overhand heeft.
* Het moet echter gezegd worden dat de effectieve plasma-osmolariteit (of toniciteit) niet overeenkomt met de totale.In feite veroorzaken alleen de moleculen die de semipermeabele membranen niet vrij kunnen passeren waterbewegingen van de meer geconcentreerde oplossing naar de minder geconcentreerde oplossing. een. tussengevoegd. Integendeel, er zijn andere, zoals ureum, die, hoewel ze bijdragen aan de bepaling van de osmolariteit, vrij permeabel zijn (ze passeren membranen) en als zodanig geen watergradiënten kunnen creëren.
Ureum passeert daardoor probleemloos de celbarrière en kan daardoor de waterbewegingen aan beide zijden van het membraan niet beïnvloeden.

Voor dit doel activeren de hypothalamische osmoreceptoren - gestimuleerd door hypersodemie - de prikkel van dorst en de daaropvolgende introductie van water brengt de plasma-osmolariteit weer in balans.Tegelijkertijd wordt het antidiuretisch hormoon (of ADH of vasopressine) afgegeven, dat werkt op hetzelfde niveau renaal door de reabsorptie van water te verhogen en bijgevolg de eliminatie ervan in de urine te verminderen. Deze verhogen op hun beurt hun osmolariteit (omdat ze meer geconcentreerd zijn). De nier heeft het vermogen om deze parameter te verhogen tot 1200 mOsM / L, of te verlagen tot 50 mOsM / L, afhankelijk van de verschillende organische behoeften.
Wat is dit
- Osmolariteit is de maat voor het aantal opgeloste deeltjes in een vloeistof (volume uitgedrukt in liters).
- De osmolariteitstest weerspiegelt de concentratie van stoffen zoals natrium, kalium, chloor, glucose en ureum in een monster van bloed, urine of soms ontlasting.
- Plasma-osmolariteit wordt gebruikt om de balans tussen water en opgeloste deeltjes in het bloed te evalueren en om de aanwezigheid van stoffen te bepalen die een onbalans van deze toestand kunnen veroorzaken.
Omdat het wordt gemeten
Plasma-osmolariteit wordt gebruikt om de water-zoutbalans van het lichaam te beoordelen en de oorzaak van aanzienlijk verhoogde of verminderde urineproductie te identificeren. De test wordt ook gebruikt om toestanden van hyponatriëmie (lage natriumconcentraties) als gevolg van uitputting van de urine of verhoogde bloedvloeistoffen te bepalen.
Plasma-osmolariteit is nuttig als hulpmiddel bij het bepalen van de oorzaak van chronische diarree en maakt het mogelijk om de behandeling met osmotisch actieve geneesmiddelen te volgen (zoals in het geval van mannitol, een diureticum dat wordt gebruikt voor de therapeutische behandeling van hersenoedeem).
Daarnaast kan het onderzoek worden gebruikt als toxicologische test als inname van methanol, ethyleenglycol, isopropylalcohol, aceton en drugs, zoals acetylsalicylzuur (aspirine), waarschijnlijk in grote hoeveelheden is.
Normale waarden
Normale osmolariteitswaarden liggen tussen 275 en 295 mOsm/L.
Opmerking: het referentiebereik van de test kan veranderen afhankelijk van leeftijd, geslacht en apparatuur die in het laboratorium wordt gebruikt. Om deze reden verdient het de voorkeur om de bereiken die rechtstreeks in het rapport worden vermeld, te raadplegen. Er moet ook aan worden herinnerd dat de resultaten van de analyses als geheel moeten worden beoordeeld door de huisarts die de medische geschiedenis van de patiënt kent.
Hoge osmolariteit - Oorzaken
Osmolariteitswaarden die hoger zijn dan de norm, kunnen afhankelijk zijn van de volgende aandoeningen of pathologieën.
- Hyperglykemie;
- Uremie;
- Hypernatriëmie;
- Smakeloze diabetes;
- Hyperlactacidemie (melkzuuracidose).
Verhoogde waarden zijn ook te vinden in het geval van:
- Suikerziekte;
- Mannitol therapie
- Diabetische ketoacidose;
- Alcoholische ketoacidose;
- Nierfalen;
- uitdroging;
- Leverziekte;
- Trauma;
- Schok;
- Vergiftiging door ethanol, ethyleenglycol, isopropylalcohol en methanol.
Lage osmolariteit - Oorzaken
Een afname van de osmolariteit kan het gevolg zijn van:
- Hyponatriëmie;
- Ongepaste ADH-secretie
Hoe het wordt gemeten
De plasma-osmolariteit wordt gemeten na een bloedmonster uit een ader in de arm.Deze parameter kan ook worden bepaald op een willekeurig urinemonster of, in sommige gevallen, op verse vloeibare ontlasting (gekoeld of ingevroren binnen 30 minuten na afname).
Voorbereiding
Soms vereist de plasma-osmolariteitstest geen voorbereiding; in andere gevallen is het noodzakelijk om ten minste 6 uur te vasten (geen eten of drinken behalve water) voordat de test wordt uitgevoerd.De arts zal de meest geschikte instructies voor het geval kunnen geven.
Interpretatie van resultaten
Plasma-osmolariteit is een dynamische parameter, die fluctueert naargelang hoe het lichaam reageert op de tijdelijke onbalans tussen water en zout en hoe het deze corrigeert. Het testresultaat moet samen met het klinische beeld van de patiënt en het resultaat van andere tests, zoals natrium, glucose en azotemie, worden geëvalueerd.
Osmolariteit is niet diagnostisch: het suggereert dat de patiënt een disbalans heeft, maar wijst niet op de oorzaak.In het algemeen, wanneer de waarde hoog is, betekent dit dat het water in het bloed is afgenomen en/of de opgeloste stoffen zijn toegenomen. Als de osmolariteit echter wordt verlaagd, is een toename van vloeistoffen waarschijnlijk.
Onder de verschillende ziekten die verantwoordelijk kunnen zijn voor een toename van de plasma-osmolariteit, worden meestal uremie, hyperglykemie, diabetes insipidus, hyperlactacidemie en hypernatriëmie gevonden.
Een afname van de osmolariteit kan echter vooral het gevolg zijn van de aanwezigheid bij de patiënt van een toestand van hyponatriëmie.