Actieve ingrediënten: Podofyllotoxine
Condyline 0,5% oplossing voor de huid
Indicaties Waarom wordt Condyline gebruikt? Waar is het voor?
Condyline bevat de werkzame stof podofyllotoxine, een extract dat afkomstig is van een plant en behoort tot een groep geneesmiddelen die "antivirale middelen" worden genoemd.
Condyline is een actueel geneesmiddel, geïndiceerd voor de behandeling van sommige soorten wratten die zich vormen op de uitwendige huid in het genitale gebied (uitwendige scherpe wratten).
Neem contact op met uw arts als u zich niet beter voelt of als u zich slechter voelt na de geplande behandelingsperiode.
Contra-indicaties Wanneer Condyline niet mag worden gebruikt
Gebruik geen Condyline
- als u allergisch bent voor podofyllotoxine of voor één van de andere bestanddelen van dit geneesmiddel (vermeld in rubriek 6)
- bij kinderen
- als u zwanger bent (zie rubriek "Zwangerschap en borstvoeding")
- als u borstvoeding geeft (zie rubriek "Zwangerschap en borstvoeding")
- als u andere geneesmiddelen gebruikt die podofylline bevatten.
Voorzorgsmaatregelen bij gebruik Wat u moet weten voordat u Condyline inneemt
Neem contact op met uw arts of apotheker voordat u Condyline gebruikt.
- Vermijd contact van de Condyline-oplossing met het slijmvlies of een gezonde huid nabij of aan de basis van de wratten, aangezien dit lokale irritatie en/of schade aan het slijmvlies of een gezonde huid kan veroorzaken. Om onbedoeld contact van de gezonde zone met de Condyline-oplossing te vermijden voordat u met de behandeling begint, kunt u de gezonde zone beschermen door een neutrale zalf of crème op basis van vaseline of zinkoxide aan te brengen.
- Vermijd contact van dit geneesmiddel met uw ogen, aangezien dit ernstige irritatie kan veroorzaken. Als dit per ongeluk gebeurt, spoel dan onmiddellijk uw ogen lang met water uit en raadpleeg uw arts.
- Vermijd het aanbrengen van dit geneesmiddel op grote oppervlakken, omdat dit bijwerkingen kan veroorzaken die verschillende organen in het lichaam aantasten.
- Als u een vrouw bent en het gebruik van dit geneesmiddel moeilijk is, omdat de wond niet toegankelijk is voor zelfmedicatie, neem dan contact op met uw arts voor het aanbrengen van Condyline.
- Als het effect van dit geneesmiddel niet zichtbaar is na de voorgeschreven behandelingsperiode, zal uw arts alternatieve therapieën overwegen.
Kinderen
Condyline is niet bedoeld voor gebruik bij kinderen.
Interacties Welke medicijnen of voedingsmiddelen kunnen het effect van Condyline veranderen
Andere medicijnen en Condyline
Vertel het uw arts of apotheker als u andere geneesmiddelen gebruikt, kort geleden heeft gebruikt of in de nabije toekomst gaat gebruiken. Vertel het uw arts in het bijzonder als u andere geneesmiddelen gebruikt die podofylline bevatten, aangezien u dit geneesmiddel in dit geval niet kunt gebruiken (zie rubriek "Gebruik Condyline niet").
Waarschuwingen Het is belangrijk om te weten dat:
Zwangerschap en borstvoeding
Gebruik Condyline niet als u zwanger bent, denkt zwanger te zijn of borstvoeding geeft.
Rijvaardigheid en het gebruik van machines
Dit geneesmiddel heeft geen invloed op de rijvaardigheid en het vermogen om machines te bedienen.
Dosis, wijze en tijdstip van toediening Hoe gebruikt u Condyline: Dosering
Gebruik dit geneesmiddel altijd precies zoals uw arts of apotheker u dat heeft verteld. Raadpleeg bij twijfel uw arts of apotheker.
volwassenen
De aanbevolen dosering is tweemaal daags één applicatie, 's morgens en' s avonds.
Duur van de behandeling
Breng dit geneesmiddel 's morgens en' s avonds aan gedurende 3 opeenvolgende dagen. Het behandelschema kan wekelijks worden herhaald tot een maximum van 5 opeenvolgende weken, met een interval van 4 dagen tussen de ene week en de andere zonder behandeling Het product dient voor korte perioden en onder medisch toezicht te worden gebruikt.
Instructies voor correct gebruik
- De fles heeft een "kindveilige" veiligheidssluiting. Om de fles te openen, drukt u op de dop en draait u deze tegelijkertijd los in de richting die wordt aangegeven door de pijl (zoals weergegeven in de afbeelding).
- Breng de oplossing aan op het te behandelen gebied van de huid met behulp van een van de applicators in de verpakking, vermijd contact met een gezonde huid (zie paragraaf "Waarschuwingen en voorzorgsmaatregelen).
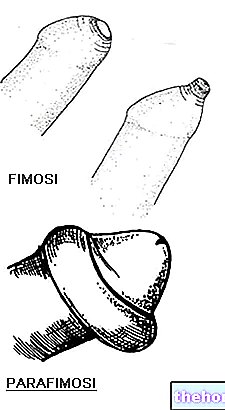
- Laat de oplossing na het aanbrengen aan de lucht drogen om te voorkomen dat de oplossing in contact komt met gezonde gebieden, vooral wanneer er wratten op de voorhuid zitten (huidplooi die de punt van de penis bij mannen bedekt).
- Gooi na het aanbrengen de gebruikte applicator weg en was uw handen zorgvuldig.
- Sluit na gebruik de dop.De fles is kindveilig gesloten als u een klik hoort wanneer u de dop losdraait zonder erop te drukken.
Overdosering Wat moet u doen als u te veel Condyline heeft ingenomen?
Wat u moet doen als u meer van Condyline heeft gebruikt dan u zou mogen
Er zijn geen bijwerkingen gemeld van het gebruik van te veel Condyline.Als u echter per ongeluk meer Condyline heeft gebruikt dan u zou mogen en u krijgt last van bijwerkingen, neem dan onmiddellijk contact op met uw arts of het dichtstbijzijnde ziekenhuis. Uw arts zal dit voor u doen.
Wat u moet doen wanneer u bent vergeten Condyline te gebruiken
Gebruik geen dubbele dosis om een vergeten dosis in te halen.
Als u stopt met het gebruik van Condyline
Als u nog vragen heeft over het gebruik van dit geneesmiddel, neem dan contact op met uw arts of apotheker.
Bijwerkingen Wat zijn de bijwerkingen van Condyline
Zoals elk geneesmiddel kan ook dit geneesmiddel bijwerkingen hebben, al krijgt niet iedereen daarmee te maken.
Lokale bijwerkingen treden meestal op de tweede of derde dag van de behandeling op wanneer de dood van de wratten begint. Over het algemeen zijn de bijwerkingen mild en worden ze goed verdragen.
De frequentie van de volgende bijwerkingen is niet bekend.
Bijwerkingen aan de huid en slijmvliezen
- erytheem (huidirritatie) met lichte pijn en/of oppervlakkige huidlaesies in het behandelde gebied. In dit geval kan het aanbrengen van Condyline pijnlijk zijn
- oedeem (zwelling) en balanoposthitis (infectie van het uiteinde van de penis) Dit effect treedt op bij grote wratten in de holte van de voorhuid
Bij onjuiste toepassing van het product kan ook het volgende optreden:
- maag- en darmaandoeningen
- leukopenie (vermindering van het aantal witte bloedcellen in het bloed)
- trombocytopenie (vermindering van het aantal bloedplaatjes in het bloed)
- veranderingen in de leverfunctie
- veranderingen in de nierfunctie
- perifere neuropathieën (ziekte van het perifere zenuwstelsel)
- meestal bescheiden sensorische stoornissen (lichte mentale verwarring), deze effecten kunnen toenemen en gecompliceerd worden met ernstigere beelden die het centrale zenuwstelsel aantasten.
Melding van bijwerkingen
Krijgt u last van bijwerkingen, neem dan contact op met uw arts.Dit geldt ook voor mogelijke bijwerkingen die niet in deze bijsluiter staan. U kunt bijwerkingen ook rechtstreeks melden via het nationale meldsysteem op www.agenziafarmaco.gov.it/it/responsabili. Door bijwerkingen te melden, kunt u ons helpen meer informatie te verkrijgen over de veiligheid van dit geneesmiddel.
Vervaldatum en retentie
Buiten het zicht en bereik van kinderen houden.
Bewaren beneden 25°C.
Gebruik dit geneesmiddel niet meer na de uiterste houdbaarheidsdatum. Die is te vinden op de doos na EXP. De vervaldatum verwijst naar de laatste dag van die maand.
Gooi geneesmiddelen niet weg via het afvalwater of met het huisvuil.Vraag uw apotheker wat u met geneesmiddelen moet doen die u niet meer gebruikt.Dit helpt het milieu te beschermen.
Samenstelling en farmaceutische vorm
Inhoud van de verpakking en andere informatie
- de werkzame stof is: podofyllotoxine (1 ml oplossing bevat 5 mg podofyllotoxine)
- de andere stoffen in dit middel zijn: melkzuur, natriumlactaat, watervrije ethanol, water.
Beschrijving van hoe Condyline eruit ziet en de inhoud van de verpakking
Condyline wordt aangeboden in een oplossing voor lokaal gebruik, verpakt in een fles van 3,5 ml oplossing.
De doos bevat twee verpakkingen van 15 applicators die nodig zijn voor therapie.
Bron Bijsluiter: AIFA (Italiaans Geneesmiddelenbureau). Inhoud gepubliceerd in januari 2016. De aanwezige informatie is mogelijk niet up-to-date.
Om toegang te hebben tot de meest actuele versie, is het raadzaam om de website van AIFA (Italian Medicines Agency) te bezoeken. Disclaimer en nuttige informatie.
01.0 NAAM VAN HET GENEESMIDDEL
CONDYLINE® 0,5% HUIDOPLOSSING
02.0 KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
1 ml bevat: podofyllotoxine 5 mg.
03.0 FARMACEUTISCHE VORM
Huid oplossing.
04.0 KLINISCHE INFORMATIE
04.1 Therapeutische indicaties
Topische behandeling van externe toegespitste wratten.
04.2 Dosering en wijze van toediening
Breng de oplossing op de wratten aan met een van de applicators in de verpakking, vermijd contact met een gezonde huid.
De toepassing moet tweemaal per dag worden uitgevoerd, 's morgens en' s avonds, gedurende 3 opeenvolgende dagen. Dit behandelschema kan wekelijks worden herhaald tot een maximum van 5 opeenvolgende weken, met een interval van 4 dagen zonder behandeling tussen de ene week en de andere.
Laat de oplossing na het aanbrengen goed aan de lucht drogen om te voorkomen dat deze zich verspreidt naar gebieden die niet door de ziekte zijn aangetast; vooral wanneer de wratten zich op de voorhuid bevinden.
Gooi na het aanbrengen de gebruikte applicator weg en was uw handen zorgvuldig.
04.3 Contra-indicaties
Bekende overgevoeligheid voor de componenten.
Het gebruik van Condyline is gecontra-indiceerd bij kinderen en bij vrouwen tijdens zwangerschap en borstvoeding. Het gebruik ervan is ook gecontra-indiceerd in combinatie met producten op basis van podofylline.
04.4 Bijzondere waarschuwingen en passende voorzorgen bij gebruik
Het product dient voor korte perioden en onder medisch toezicht te worden gebruikt.
Het aanbrengen van het preparaat op relatief grote slijmvliezen kan systemische reacties veroorzaken en moet daarom worden vermeden.
De Condyline mag niet in contact komen met de ogen, omdat dit ernstige irritatieverschijnselen kan veroorzaken. Als dit per ongeluk gebeurt, spoel dan onmiddellijk uw ogen met veel water en raadpleeg uw arts.
Buiten het bereik en zicht van kinderen houden.
Bij vrouwelijke patiënten voor wie de laesie niet toegankelijk is voor zelfmedicatie, dient de behandeling plaats te vinden onder direct medisch toezicht.
Lokale irritatieverschijnselen en/of zweren van het slijmvlies of van de gezonde huid in de buurt of aan de basis van de wratten, onbedoeld veroorzaakt door contact met de Condyline oplossing, kunnen worden voorkomen door de gezonde plek te beschermen met een neutrale zalf of crème , op basis van vaseline of zinkoxide, aan te brengen vóór de behandeling met Condyline.
Als de werkzaamheid van het preparaat na de geplande behandelingsperiode niet duidelijk is, moeten alternatieve therapieën worden overwogen.
04.5 Interacties met andere geneesmiddelen en andere vormen van interactie
Gebruik Condyline niet tijdens behandeling met producten die podofylline bevatten.
04.6 Zwangerschap en borstvoeding
Gebruik Condyline niet tijdens zwangerschap en borstvoeding.
04.7 Beïnvloeding van de rijvaardigheid en het vermogen om machines te bedienen
Het product brengt de rijvaardigheid en het vermogen om machines te bedienen niet in gevaar.
04.8 Bijwerkingen
Lokale secundaire reacties treden voornamelijk op in combinatie met het optimale therapeutische effect, meestal op de tweede of derde dag van de behandeling wanneer wrattennecrose begint.Deze secundaire reacties treden meestal licht op en worden door patiënten goed verdragen als ze door de arts worden gewaarschuwd voordat de therapie wordt gestart Het is te voorzien dat in het behandelde gebied erytheem verschijnt met lichte gevoeligheid en/of oppervlakkige ulceratie van het epitheel en daarom kan het aanbrengen van Condyline pijnlijk zijn.
Oedeem en balanoposthitis zijn waargenomen bij sommige patiënten met grote wratten in de voorhuidholte.
Onjuiste toepassing van het product kan leiden tot manifestaties van systemische absorptie, zoals gastro-intestinale stoornissen, leukopenie, trombocytopenie, lever- of nierfunctiestoornissen, perifere neuropathieën, over het algemeen bescheiden sensorische stoornissen (lichte mentale verwarring), maar die kunnen verergeren en compliceren met meer ernstige gevallen die het CZS aantasten.
04.9 Overdosering
Er zijn geen bijwerkingen gemeld als gevolg van een overdosis podofyllotoxine. Dergelijke effecten zijn niet te verwachten bij correct gebruik van Condyline gezien de grote veiligheidsmarge van het preparaat.
Mochten zich echter systemische effecten van een overdosis voordoen, neem dan therapeutische maatregelen die vergelijkbaar zijn met die welke worden overwogen in het geval van een overdosis podofylline, gericht op het beheersen van de symptomen (braken en convulsies); druk en diurese moeten nauwlettend in de gaten worden gehouden, rekening houdend met het feit dat bij acute podofyllinevergiftiging vochtherstel en hemoperfusie geïndiceerd kunnen zijn.
05.0 FARMACOLOGISCHE EIGENSCHAPPEN
05.1 Farmacodynamische eigenschappen
Podofyllotoxine, het actieve ingrediënt van Condyline, behoort chemisch tot de groep van lignanen.
ATC-code: D06BB04.
Het is het belangrijkste therapeutische bestanddeel van podofylline waaruit het wordt verkregen via een bepaald extractieproces dat zorgt voor een hoge mate van zuiverheid en standaardisatie van het product. Podofyllotoxine heeft een duidelijke antimitotische en cytolytische activiteit die snel necrose van toegespitste wratten veroorzaakt. De activiteit van podofyllotoxine wordt sneller en effectiever uitgevoerd dan die van podofylline vanwege de hoge mate van zuiverheid en standaardisatie. Dit maakt de toediening van geschikte doses mogelijk met een lager risico op bijwerkingen en maakt het mogelijk om de patiënt thuis te behandelen met hoge genezingspercentages.
05.2 "Farmacokinetische eigenschappen
Acute giftigheid
Acute toxiciteitsstudies hebben aangetoond dat orale toediening van een enkele dosis podofyllotoxine van minder dan 25 mg/kg, bij ratten en muizen, niet toxisch is.
De acute toxiciteit van podofyllotoxine is onderzocht bij talrijke diersoorten en via verschillende toedieningswegen.
De LD50 bij muizen is 40 mg/kg (orale weg), 19 tot 33 mg/kg intraveneus, 31 mg/kg subcutaan en 4,6 mg/kg intraveneus; bij de rat is het 14 mg/kg subcutaan, 3 mg/kg intramusculair en 15 mg/kg intramusculair; bij konijnen 5 mg / kg intraveneus; bij de hond subcutaan van 10 tot 30 mg afhankelijk van het lichaamsgewicht.
Acute toxiciteitsstudies voor langdurige epicutane toediening gedurende 24 uur (limiettesten) van Condyline in een dosis van 2 ml / kg lichaamsgewicht (overeenkomend met podofyllotoxine 10 mg / kg), op de geschoren rug van muizen en ratten (in de laatste hieronder occlusie), hebben aangetoond dat het product geen systemische toxiciteit vertoont.
Subacute of chronische toxiciteitsstudies
Na epicutane toediening bij muizen, tweemaal per week gedurende 74 weken, van een oplossing van 2,5% podofyllotoxine in polyethyleenglycol, op een dorsaal gebied van 2,5 cm2, werd vastgesteld dat na 29 weken behandeling het aantal sterfgevallen 0 was. 25, na 50 weken was het 5/25 en na 74 weken steeg het tot 12/25 (48%).
De gebruikte dosering was 50 mcl, wat overeenkomt met ongeveer 1,25 mg per muis.
Rekening houdend met het lichaamsgewicht van 20 g, is de gebruikte lokale dosis gelijk aan 62,5 mg/kg.
Bij mensen is Condyline 0,5% toegepast in doses van ongeveer 10-100 mcl, overeenkomend met 0,0007-0,007 mg/kg.
Aangezien Condyline een actueel product is, werd de Magnusson-Klingman "maximalisatietest" uitgevoerd op cavia's met 0,5% podofyllotoxine in propyleenglycol en 0,01% tot 0,5% oplossingen in de inductiefase.
De provocatietest met concentraties van 0,1% en 0,5% veroorzaakte een niet-allergische irritatiereactie.
Er waren geen allergische reacties in een van de experimenten.
Het plaatselijke irriterende effect na herhaalde toediening (2 keer per dag gedurende 10 dagen) van 0,01%, 0,05%, 0,1% en 0,5% oplossingen van podofyllotoxine in 70% ethanol werd bestudeerd bij konijnen (versus een controlegroep behandeld met alleen 70% ethanol ), zowel door de dikte van de huidplooi te meten als door parameters zoals erytheem, exsudatie en aanwezigheid van korsten visueel te evalueren.
De resultaten toonden een lineaire correlatie aan tussen de toename van de concentratie van podofyllotoxine en de toename van de dikte van de plooi, evenals een exponentiële relatie tussen de toename van de geneesmiddelconcentratie en de huidreactie.
Podofyllotoxine is embryotoxisch, terwijl het geen carcinogene of mutagene activiteit vertoont.
05.3 Gegevens uit het preklinisch veiligheidsonderzoek
Farmacokinetische onderzoeken met gelabeld podofyllotoxine werden uitgevoerd bij gezonde en tumordragende muizen. Na 4 uur subcutane toediening was de meeste radioactiviteit gelijkmatig verdeeld tussen darm en urine, terwijl er slechts sporen aanwezig waren in de lever, galblaas en nieren, evenals in de hersenen, bijnierschors en testikels. Bij muizen met sarcoom 180 werd de meeste radioactiviteit in de urine aangetroffen.
De eliminatie van podofyllotoxine was veel sneller bij deze laatste dieren. De tumor bevatte geen significante hoeveelheid radioactiviteit. De niveaus van radioactiviteit die uit de urine werden teruggevonden, waren veel lager bij muizen met het ascitescarcinoom van Ehrlich. Bij alle dieren werd een relatief hoge concentratie van radioactiviteit werd gevonden in de gal, die samen met het nieremunctorium de belangrijkste uitscheidingsroute van podofyllotoxine en zijn metabolieten lijkt te zijn.
In onderzoeken naar percutane absorptie bij patiënten die werden behandeld met 0,5% podofyllotoxine toegediend in een dosis van 0,01-0,05 ml gedurende 3 dagen, was het niet mogelijk om het geneesmiddel in serum te detecteren in de ½-1 uur na de dag van toediening.
Bij gebruik van doses van 0,1 ml (op wratten met een totale oppervlakte> 4 cm2) werden de serumspiegels van podofyllotoxine
Bij een dosis van 0,15 ml waren de serumspiegels ongeveer gelijk, terwijl ze bij 5 patiënten 12 uur na toediening ≤ 1 ng/ml waren.
Bij patiënten die werden behandeld met 0,1-1,5 ml voor zeer uitgebreide laesies, waren de maximale niveaus na 1-12 uur 1-17 ng / ml. Het is echter aangetoond dat hoeveelheden van meer dan 0,1 ml oplossing in de klinische praktijk zelden nodig zijn. Een relatief lange klaring na tweemaal daags aanbrengen van 0,1 ml 0,5% oplossing kan erop wijzen dat de verdeling plaatsvindt volgens een 2-compartimentenmodel Uit de uitgevoerde onderzoeken kan een serumhalfwaardetijd van 1 op 1 worden geëxtrapoleerd 4½ uur Er werd geen accumulatie van podofyllotoxine waargenomen.
06.0 FARMACEUTISCHE INFORMATIE
06.1 Hulpstoffen
Melkzuur, natriumlactaat, watervrije ethanol, water.
06.2 Incompatibiliteit
Ze zijn niet bekend.
06.3 Geldigheidsduur
3 jaar.
06.4 Speciale voorzorgsmaatregelen bij bewaren
Bewaren beneden 25°C
06.5 Aard van de primaire verpakking en inhoud van de verpakking
Doos met 3,5 ml fles met veiligheidsslot.
06.6 Instructies voor gebruik en verwerking
Niet relevant.
07.0 HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Astellas Pharma S.p.A. - Via delle Industrie 1 - 20061 Carugate (Milaan)
08.0 NUMMER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
027136011
09.0 DATUM VAN EERSTE VERGUNNING OF VERLENGING VAN DE VERGUNNING
Registratie 2 mei 1990 - Verlenging van de vergunning 1 juni 2010
10.0 DATUM VAN HERZIENING VAN DE TEKST
september 2011